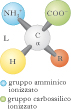
amminoacido (o aminoacido)
amminoacido (o aminoacido)
Composto organico caratterizzato dalla presenza nella molecola di un gruppo acido, carbossilico, −COOH e di un gruppo basico, amminico, −NH2. Gli amminoacidi si possono trovare presenti allo stato libero nei tessuti e nei liquidi dell’organismo, oppure legati in peptidi a basso peso molecolare, di grande importanza dal punto di vista biologico. Soprattutto però gli a. si trovano in natura come costituenti delle proteine, uniti l’uno all’altro in un arrangiamento tipo testa-coda con legame ammidico, detto legame peptidico, che si forma per reazione fra un gruppo carbossilico di un a. e il gruppo amminico di quello successivo con liberazione di una molecola d’acqua; si vengono così a formare lunghi polimeri lineari chiamati catene polipeptidiche. Gli a. delle proteine sono tutti α-a., cioè il gruppo amminico si trova legato allo stesso carbonio a cui è legato il gruppo carbossilico. Le catene laterali degli a. hanno una fondamentale importanza biologica in quanto determinano le proprietà funzionali e strutturali delle proteine stesse. Ad eccezione della glicina tutti gli a. hanno quattro raggruppamenti atomici differenti legati al carbonio a cui è unito il gruppo amminico, che risulta così asimmetrico; per ogni a. possono esistere due stereoisomeri L e D. Solo gli L-amminoacidi sono composti biologicamente attivi e possono essere utilizzati dagli organismi viventi. Gli amminoacidi sono sostanze otticamente attive: uno stereoisomero della serie L può essere destrogiro (+) o levogiro (−). Gli a. costituenti le proteine sono 20, dei quali 8 sono considerati a. essenziali per l’uomo, poiché non possono essere sintetizzati nell’organismo umano: isoleucina, leucina, lisina, fenilalanina, metionina, treonina, triptofano, valina. Gli a. sono componenti indispensabili nella dieta di tutti gli animali, compreso l’uomo. La maggior sorgente degli a. per i Mammiferi è rappresentata dalle proteine che vengono idrolizzate in piccoli peptidi dagli enzimi proteolitici dello stomaco e dell’intestino.