BIOSENSORE
Biosensore
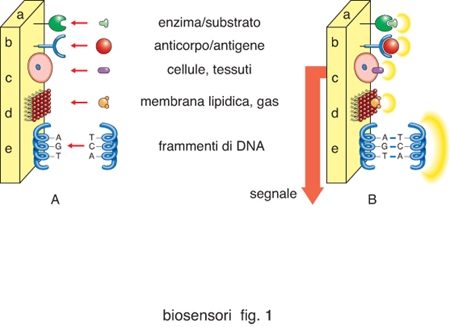
I b. sono sistemi formati da un trasduttore di segnale e da un sistema biologico: enzima, anticorpo, tessuti, cellule, ecc., in intimo contatto fra loro. Lo studio dei b. è una delle più promettenti linee di ricerca in chimica analitica, in quanto consente, in molti casi, una determinazione rapida, diretta e selettiva di una particolare specie chimica, anche in presenza di molecole complesse e di altre specie chimicamente simili (fig. 1). In questo caso si parla di biosensori chimici, ma si sottolinea a questo punto, senza entrare nel merito, l'esistenza di b. biologici e di b. fisici, i primi sensibili a specie biologiche i secondi a grandezze fisiche come, per es., la temperatuta, la pressione, ecc. La specificità della risposta di questi dispositivi, inoltre, in genere minimizza o elimina la necessità di manipolazioni preliminari del campione, richieste invece nel caso in cui si usino tecniche tradizionali, quali la gas-cromatografia (GC) o la cromatografia ad alte prestazioni (HPLC, High Performance Liquid Chromatography), e rappresenta un'alternativa all'uso di sistemi analitici costosi e sofisticati, quali, per es., la spettrometria di massa (MS).
In particolare, sono sempre più studiati sistemi in cui l'elemento biologico è costituito da un anticorpo oppure da una sostanza a esso complementare (antigene) per la determinazione di piccole quantità di analiti in campo medico, ambientale e alimentare. Tali sistemi prendono il nome di immunosensori, e sono definiti come dispositivi analitici costituiti da un opportuno trasduttore ricoperto di un antigene adatto alla cattura selettiva di un anticorpo (formazione complesso antigene-anticorpo) che rappresenta l'analita, producendo un segnale correlato alla sua concentrazione. Questi sistemi, in generale, si basano sullo stesso principio dei saggi immunologici, ossia sul riconoscimento di una data specie chimica da parte del corrispettivo anticorpo e sull'affinità di quest'ultimo.
Gli immunosensori, a cui molta attenzione verrà dedicata nel prossimo futuro, possono essere raggruppati in due categorie principali: di tipo diretto (non marcati) o indiretto (marcati).
Immunosensori non marcati o diretti
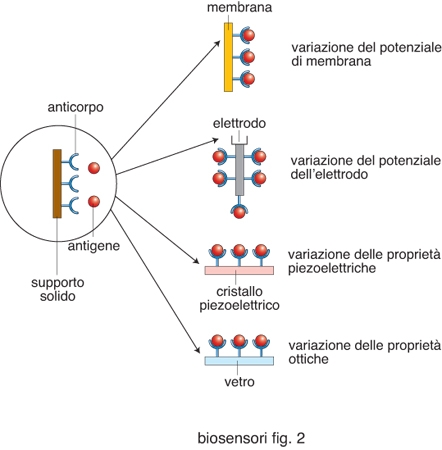
In questo tipo di immunosensori, il trasduttore scelto è in grado di determinare direttamente la specie in esame in base alla variazione del parametro chimico-fisico misurato (corrente, potenziale, massa, temperatura, proprietà ottiche) associato alla formazione del complesso antigene-anticorpo; esso è utilizzabile in continuo e per misure in tempo reale. La sensibilità ottenuta dipende dal tipo di trasduttore impiegato e dall'affinità dei biocomponenti utilizzati; a tal fine vengono usati materiali otticamente attivi, materiali piezoelettrici, elettrodi, membrane come sistemi di rivelazione diretta (fig. 2).
Immunosensore piezoelettrico
Un immunosensore piezoelettrico può essere realizzato depositando sulla superficie del cristallo di quarzo un biorecettore, o una membrana biologica, selettiva per la sostanza chimica da analizzare, che, venendo adsorbita sulla superficie del materiale, produce, tramite una variazione di massa, una variazione della frequenza di oscillazione del cristallo stesso.
Uno degli esempi è rappresentato dalla misura, in fase gassosa, del coronavirus della SARS (SARS-CoV, Severe Acute Respiratory Syndrome - Corona virus) nell'espettorato. Un anticorpo contro SARS-CoV (antigene) viene immobilizzato su un cristallo di quarzo piezoelettrico e orientato in maniera opportuna mediante la proteina A preimmobilizzata. Il campione, contenente il coronavirus, viene successivamente atomizzato sul cristallo via aerosol. L'anticorpo, presente sul cristallo, si lega per affinità all'analita in maniera specifica. La formazione del complesso immunologico genera una variazione di frequenza che viene messa in relazione alla variazione di massa, e di conseguenza alla concentrazione della specie da analizzare.
Immunosensore potenziometrico
Misure potenziometriche dirette sono state effettuate per la determinazione dell'encefalite B giapponese. L'immobilizzazione dell'anticorpo primario (sviluppato contro l'analita in esame) avviene su un film di o-fenilenediamine/nano Au su un elettrodo di platino. La formazione del complesso antigene-anticorpo genera una variazione del potenziale di membrana che è direttamente proporzionale alla concentrazione dell'analita in esame.
Immunosensori marcati o indiretti
Gli immunosensori marcati prevedono l'utilizzo di una molecola tracciante (per fare qualche esempio, enzima, molecola fluorescente, isotopo radioattivo, ecc.), legata a un biocomponente (antigene o anticorpo), in grado di evidenziare la formazione dell'immunocomplesso. I traccianti più utilizzati sono gli enzimi, quali la perossidasi (HRP, Hydrogen Peroxide Oxidireductase) e la fosfatasi alcalina (FA), i cui prodotti possono essere misurati sia spettrofotometricamente sia elettrochimicamente.
Tutti gli immunosensori indiretti sono progettati in modo tale da consentire la formazione del complesso antigene-anticorpo direttamente sulla superficie del sensore. L'immobilizzazione dei biocomponenti può avvenire per adsorbimento, legame covalente, cross-linking e intrappolamento. Una volta che il tracciante viene incorporato nell'immunocomplesso, questo può essere determinato potenziometricamente, amperometricamente, oppure mediante misure ottiche. In generale, tali sistemi possono essere classificati in base al tipo di rivelazione scelto per la misura dell'analita; si distinguono, infatti, immunosensori elettrochimici, ottici, piezometrici e termometrici. Prescindendo dal tipo di trasduttore utilizzato, essi rappresentano la diretta applicazione dei saggi ELISA (Enzyme Linked Immunosorbent Assay), saggi immunologici in cui la determinazione della quantità di tracciante rappresenta una misura indiretta dell'analita di interesse.
Gli immunosensori indiretti, tra quelli citati, che offrono migliori garanzie per le applicazioni analitiche in termini di sensibilità, riproducibilità, selettività e ampio intervallo di lavoro, sono quelli elettrochimici (amperometrici e potenziometrici).
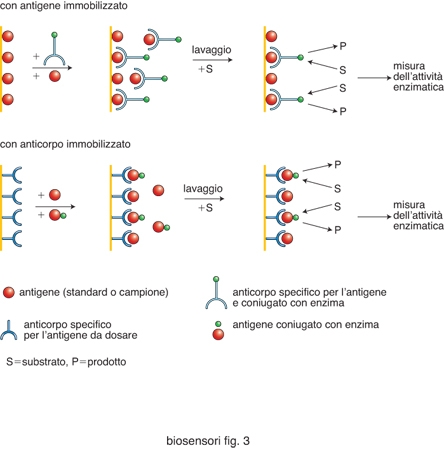
Prima di citare alcuni esempi, verranno descritti sinteticamente i principi su cui si basano i metodi ELISA. Occorre innanzitutto distinguerli in saggi immunologici competitivi (antigene o anticorpo immobilizzati) e non competitivi (sandwich). I saggi competitivi prevedono l'immobilizzazione dell'antigene o dell'anticorpo su supporto solido (fig. 3A). Quando è l'antigene a essere immobilizzato l'addizione di anticorpi specifici coniugati con un enzima che funge da marcatore e di campioni, contenenti l'antigene da dosare, comporta una competizione tra l'antigene immobilizzato e quello libero (standard o campione) per l'anticorpo marcato. Dopo un periodo di incubazione, gli eccessi di analita e di anticorpo vengono rimossi mediante lavaggio. Viene quindi aggiunto il substrato enzimatico e viene misurato il segnale generato dal prodotto di reazione. Tale segnale è inversamente proporzionale alla quantità di antigene presente nel campione. Nel caso in cui sia l'anticorpo a essere immobilizzato su un supporto solido la competizione avverrà tra l'antigene libero e quello marcato. Per aumentare la sensibilità del saggio, piuttosto che marcare l'anticorpo primario, come descritto, spesso si fa ricorso a un anticorpo secondario (specifico per le γ-globuline dell'animale impiegato per ottenere l'anticorpo primario) coniugato con l'enzima.
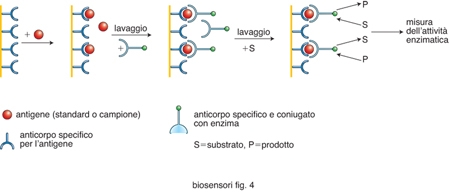
I saggi immunoenzimatici con una configurazione a sandwich (per la determinazione di analiti ad alto peso molecolare, ovvero verso i quali esistono più anticorpi primari) prevedono l'immobilizzazione dell'anticorpo e la successiva addizione sia del campione (contenente l'antigene da dosare) sia di un secondo anticorpo coniugato con l'enzima marcatore. In questo caso il segnale generato dal prodotto della reazione sarà direttamente proporzionale alla concentrazione dell'analita presente nel campione (fig. 3B).
Immunosensori elettrochimici monouso
I sensori monouso hanno suscitato un notevole interesse in campo clinico, ambientale e alimentare, grazie alla possibilità di effettuare misure in maniera semplice, rapida ma soprattutto a costi limitati. I b. monouso più comuni sono quelli prodotti mediante la tecnologia a film spesso (thick film), basata su una deposizione sequenziale del film su di un supporto con processo serigrafico. Gli elettrodi stampati o SPE (Screen Printed Electrodes), rappresentano un'intera cella elettrochimica, in pochi centimetri, con un elettrodo di lavoro, che funge sia da trasduttore di segnale sia da supporto per l'immobilizzazione dei biocomponenti, un elettrodo di riferimento e un controelettrodo, il tutto stampato su un sottile film di poliestere.
Immunosensori amperometrici per le micotossine (ocratossina A- OTA -, aflatossina B1 - AFB1 - e aflatossina M1- AFM1) sono stati realizzati utilizzando gli elettrodi SPE. Gli enzimi HRP e AP, coniugati con l'anticorpo (oppure l'antigene), sono stati utilizzati come traccianti e impiegati come co-substrati rispettivamente l'H2O2 e la 3,3',5,5'-tetrametilbenzidina (TMB) e l'1-naftilfosfato (1-NPP). Saggi ELISA di tipo competitivo sono stati sviluppati ottenendo limiti di rilevabilità dell'ordine di 200, 90 e 30 ppt, per l'OTA, l'AFB1 e l'AFM1. Il vantaggio di tale approccio risulta nella velocità dell'analisi (solo 60 min) rispetto a un analogo test spettrofotometrico in piastra (14 ore); in più l'uso degli elettrodi stampati elimina i problemi relativi all'avvelenamento e rigenerazione della superficie necessaria per gli elettrodi convenzionali.
Un immunosensore monouso per i PCB (Polychlorinated Biphenyls) è stato realizzato basandosi sul principio delle tecniche immunologiche. La perossidasi, coniugata con l'anticorpo primario, è stata utilizzata come tracciante e sono stati impiegati come suoi co-substrati l'H2O2 e l'acido ferrocenemonocarbossilico (FCA). Sono stati realizzati saggi competitivi secondo il metodo dell'anticorpo immobilizzato con un limite di rilevabilità dell'ordine di 10 ng/ml.
Sono stati sviluppati immunosensori elettrochimici non competitivi per la determinazione di batteri patogeni, quali Salmonella typhimurium ed Escherichia coli. In particolare si è fatto uso, per il supporto della catena immunologica, di particelle immunomagnetiche (IMBs, Immunomagnetic Beads). Tale tecnica, denominata ELIME (Enzyme Linked Immunomagnetic lectrochemistry), riesce a combinare la selettività degli anticorpi, immobilizzati sulle particelle magnetiche, con la rapidità e la sensibilità della rivelazione elettrochimica. Tali particelle (1-5 μm di diametro) sono costituite da una dispersione di materiale magnetico (Fe2O3 e Fe3O4) ricoperta da un sottile guscio polimerico che provvede a definire l'area superficiale per l'adsorbimento o per l'accoppiamento con una grande varietà di molecole. Queste particelle possono essere ricoperte con anticorpi selezionati e funzionare come reagenti di immunoriconoscimento selettivo. Al termine della catena immunologica le particelle immunomagnetiche sono state concentrate, con l'aiuto di un piccolo magnete, sulla superficie di uno SPE. In seguito, pochi μl di substrato enzimatico sono depositati sul sensore. L'attività enzimatica è misurata mediante tecniche elettrochimiche estremamente sensibili e rapide quali la voltammetria a onda quadra (SWV, Square Wave Voltammetry) e la voltammetria differenziale a impulsi (DPV, Differential Pulse Voltammetry).
Immunosensore potenziometrico
Tra gli immunosensori potenziometrici, si ricorda quello sviluppato per la determinazione della simazina (2, cloro-4,6-bis-etilammino-1,3,5-triazina), erbicida utilizzato per il mais e il sorgo, che metabolizzano rapidamente il principio attivo trasformandolo nel suo idrossiderivato, non tossico. Il monitoraggio dell'erbicida viene effettuato secondo un metodo ELISA competitivo, utilizzando come tracciante HRP coniugato alla simazina stessa. L'immunosensore è realizzato elettrodepositando l'anticorpo su un elettrodo di oro planare, su cui era stata precedentemente immobilizzata la proteina A. La variazione di potenziale registrata, dovuta all'interazione antigene-anticorpo, risulta inversamente proporzionale alla concentrazione della simazina nel campione.
Immunosensore ottico
Un immunosensore a fibra ottica è stato sviluppato per determinare le concentrazioni della micotossina fumonisina B1 (FB1) in campioni di granturco. Anticorpi monoclonali prodotti contro la FB1 sono stati legati covalentemente per mezzo di un silano eterobifunzionale a una fibra ottica. È stato usato un effetto di onda evanescente per eccitare le molecole di FB1 marcate con isotiocianato di fluoresceina (FB1-FITC) in prossimità della superficie della fibra. Per determinare le concentrazioni di FB1 è stato effettuato un dosaggio competitivo con saturazione dei siti di legame dell'anticorpo con FB1-FITC e successiva addizione di FB1 con spiazzamento della tossina marcata. Il segnale generato nel dosaggio è risultato inversamente proporzionale alla concentrazione di FB1, con un limite di rilevabilità di 10 ng/ml.
Un metodo ottico molto sensibile, di ultima generazione, si basa sull'uso di una pellicola di oro metallico depositata su una superficie di vetro sottile, che funge da guida per la luce.
La Surface Plasmon Resonance (SPR) si verifica quando la luce, che attraversa il mezzo (vetro) con un certo indice di rifrazione, si riflette sulla superficie di un sottile strato di metallo (oro o argento), che è in contatto con un mezzo a indice di rifrazione minore (soluzione tampone). A un certo angolo di incidenza corrisponde un minimo dell'intensità di riflessione, che viene fortemente influenzato dall'indice di rifrazione del mezzo nell'immediata vicinanza dello strato del metallo. Tale tecnica può quindi essere usata per realizzare un immunosensore senza l'uso di molecole marcate, immobilizzando direttamente gli anticorpi sulla superficie del dispositivo per monitorare un'immunoreazione. Il metodo della SPR può essere impiegato per studiare un'ampia varietà di sostanze ed è stato sviluppato un sistema (Biacore®) destinato inizialmente ai laboratori di ricerca, che incorpora generici sensori a SPR, sui quali si depositano i biorecettori specifici per la reazione che si vuole studiare.
Biosensori a DNA
Come sistemi di riconoscimento molecolare, oltre agli anticorpi, possono anche essere usati microrganismi, cellule, porzioni di tessuto animale oppure vegetale, enzimi, anticorpi, membrane e acidi nucleici.
In base al sistema di riconoscimento molecolare i b. si dividono in due categorie: catalitici e ad affinità. Al primo gruppo appartengono sensori che utilizzano un elemento biologico che catalizza una reazione di trasformazione di un substrato in un prodotto in grado di generare un segnale. A tale categoria appartengono i biosensori enzimatici. In questo caso si giunge pertanto a uno stato stazionario nella produzione della molecola rilevabile e il segnale generato è continuo. Un esempio di b. catalitico è il sensore per la misura di glucosio; esso prevede l'impiego dell'enzima glucosio ossidasi (GOD, Glucose Oxidase) che catalizza la reazione fra glucosio e ossigeno per dare acido gluconico e acqua ossigenata, che viene rilevata per via amperometrica. Invece, i sensori ad affinità impiegano molecole, come recettori, anticorpi e acidi nucleici, in grado di legare specificamente l'analita. Dalla loro interazione si origina un complesso, che non provoca la continua conversione di un substrato in un prodotto, ma una modificazione del sistema. In altri termini, a causa della reazione di affinità, lo stato finale differisce da quello iniziale ed è questa differenza che viene rilevata. La facilità con cui il DNA viene adsorbito sulla superficie di vari tipi di elettrodi ha suggerito la possibilità di impiegare tali elettrodi, opportunamente modificati, per realizzare b. a uso analitico.
I costituenti dello scheletro del DNA non sono elettroattivi e pertanto le proprietà elettrochimiche della macromolecola sono dovute alle basi azotate: l'adenina e la guanina possono subire reazioni di ossidazione sulla superficie di elettrodi di grafite. La fig. 4 mostra gli atomi che sono coinvolti nelle reazioni di ossidazione e riduzione delle basi nella doppia elica del DNA.
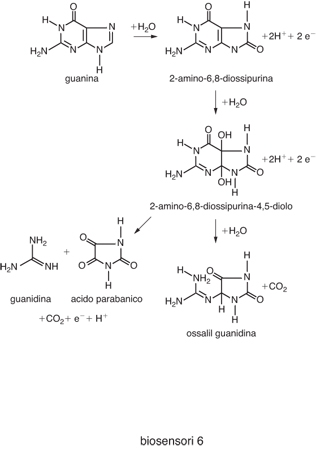
L'ossidazione della guanina (2-amino-6-ossipurina) avviene in più fasi successive: si ha un processo bielettronico che coinvolge il doppio legame N(7)=C(8), seguito da un'altra ossidazione a due elettroni del doppio legame C(4)=C(5) per originare il 2-amino-6,8-diossipurina-4,5-diolo. Questo composto è instabile e può andare incontro a una ulteriore ossidazione all'elettrodo generando acido parabanico, guanidina e anidride carbonica; in alternativa può idrolizzarsi a ossalilguanidina e anidride carbonica (fig. 5).
Molte molecole a basso peso molecolare di interesse clinico e ambientale presentano un'elevata affinità per il DNA e possono perciò interagire con lo strato di acidi nucleici immobilizzato sulla superficie di un elettrodo. Tali interazioni, che possono essere di natura elettrostatica o idrofobica a seconda delle condizioni di pH e forza ionica determinano negli acidi nucleici modificazioni chimiche, conformazionali o di semplice ingombro sterico. Queste, a loro volta, determinano una variazione delle proprietà elettrochimiche del DNA che possono quindi essere utilizzate per verificare l'avvenuta interazione.
I b. elettrochimici a base di DNA caratterizzati da rapidità di risposta, semplicità, sensibilità, economicità, rappresentano un interessante metodo per la determinazione non specifica della tossicità.
Tale tipo di b. è preparato impiegando elettrodi stampati monouso a base di grafite, in quanto, l'uso di trasduttori di questo tipo, permette, per es., di evitare la contaminazione tra i campioni da analizzare. Su tali elettrodi è immobilizzato uno strato superficiale di DNA (a singolo o a doppio filamento); il b. risultante è messo a contatto con soluzioni di varia natura, contenenti molecole di interesse ambientale. Le modificazioni apportate allo strato superficiale di DNA dall'interazione con queste soluzioni possono quindi essere rilevate tramite una misura elettrochimica. L'effetto delle sostanze a basso peso molecolare che presentano affinità per il DNA è infatti quello di complessare la guanina, riducendone la disponibilità all'ossidazione. Per la fase di misura sono impiegate le tecniche cronopotenziometria a corrente costante (PSA, Potentiometric Stripping Analysis) e SWV.
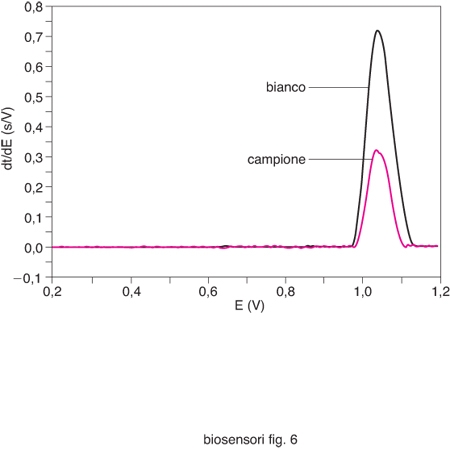
Il parametro scelto quale indice della tossicità di un campione è la riduzione percentuale R% dell'area del picco di ossidazione della guanina (G) rispetto a un bianco: R%=[(Area del picco G sul campione/Area del picco G sul bianco)-1]100. La misura di questo parametro permette quindi di attribuire a ciascun campione un certo livello di tossicità, sulla base di uno schema simile a quello riportato per i saggi che fanno uso delle cellule batteriche: R%〈20%, bassa tossicità; 20%〈R%〈40% , moderata tossicità; R%>40%, elevata tossicità.
In genere una R(%) del 20% corrisponde al doppio della deviazione standard che si ha sul bianco. Tale risposta è pertanto la più piccola effettivamente rilevata dal b. a DNA e tutti i campioni che ne determinano una inferiore possono essere considerati scarsamente tossici. Il limite superiore del 40% è stato invece scelto (in base all'esperienza) a indicare la pericolosità di quei campioni che, evidentemente, contengono sostanze con un'alta affinità per il DNA.
La fig. 6 mostra un tipico risultato sperimentale dal quale estrarre le aree dei picchi.
bibliografia
G. Volpe, E. Delibato, L. Orefice et al., Tossinfezioni alimentari e metodiche recenti ed innovative per la ricerca dei batteri patogeni, in Caleidoscopio, 2005, 190.