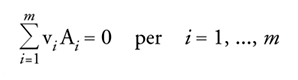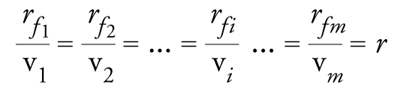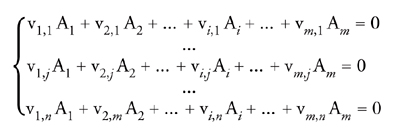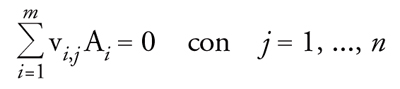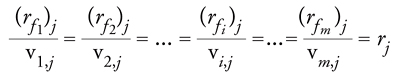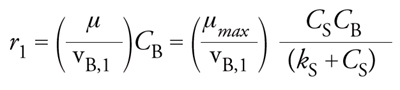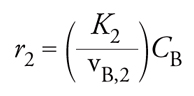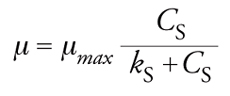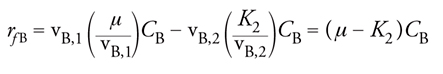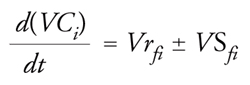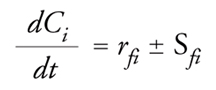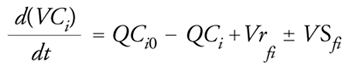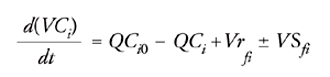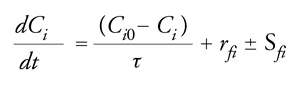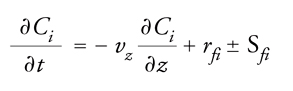Depurazione biologica
Depurazione biologica
La depurazione biologica, ovvero l’eliminazione mediante processi biologici di sostanze contaminanti indesiderate da liquidi, solidi o gas, si verifica sia in natura sia in sistemi appositamente progettati. Utilizzando il carbonio e le fonti di energia presenti nell’ambiente, i microorganismi (quali batteri e funghi) convertono sia le sostanze inquinanti sia quelle non inquinanti in diossido di carbonio, acqua, massa cellulare e in una serie di altri composti che entrano a far parte dell’ambiente naturale. Se i processi biologici naturali non tengono il passo con la velocità con cui le sostanze inquinanti vengono introdotte nell’ambiente, l’acqua che si usa, l’aria che si respira e la terra sulla quale viviamo risulteranno inquinate.
Benché le sostanze che contaminano l’ambiente vengano prodotte da tutte le forme di vita, oltre che dai fenomeni geologici e meteorologici (per es., l’attività vulcanica), l’attenzione di solito è puntata su quelle che derivano dall’attività umana a livello industriale, agricolo, minerario e domestico. Indipendentemente dalla loro origine, le sostanze contaminanti idonee a essere distrutte forniscono energia o nutrimento (o entrambi) a un’associazione microbica preesistente o predisposta nell’impianto di trattamento degli scarichi. In entrambi i casi, praticamente tutte le sostanze inquinanti che possono essere consumate dai microorganismi vengono definite biodegradabili o leggere. Nello specifico, questo significa che l’associazione microbica contiene l’informazione genetica necessaria per produrre enzimi catabolici che estraggono energia dalle sostanze inquinanti convertendole in prodotti biochimici intermedi. Gli enzimi delle vie anaboliche utilizzano l’energia estratta e i prodotti intermedi per sintetizzare i composti necessari affinché i microbi possano riprodursi. L’associazione microbica presente deve, quindi, possedere tutte le informazioni genetiche necessarie affinché le opportune reazioni biochimiche abbiano luogo, altrimenti la sostanza inquinante rimarrà nell’ambiente. In questo caso tale sostanza non è biodegradabile e viene conseguentemente definita resistente o dura.
Le sostanze inquinanti vengono giudicate pericolose o non pericolose indipendentemente dalla loro biodegradabilità. Una sostanza pericolosa per un gruppo di microorganismi può costituire una preziosa fonte di nutrimento per un altro gruppo. Di conseguenza, molti composti pericolosi possono essere biodegradati nell’ambiente. Considerando tempi abbastanza lunghi, la natura può svolgere la funzione di autodepurazione rispetto a tutti i composti biodegradabili, che siano pericolosi o meno. Per vari motivi, tra cui, da non trascurare, le esigenze dettate dalla struttura sociale dell’uomo (per es., impiego del tempo libero, trasporto, problemi di salute pubblica) non si può attendere che siano i processi biologici naturali a depurare l’acqua, l’aria o il terreno dai contaminanti presenti; pertanto questi composti devono essere rimossi mediante impianti di trattamento degli scarichi.
In seguito si illustrerà il modo in cui vengono progettati i sistemi biologici che utilizzano i microorganismi per aumentare la velocità con cui le sostanze inquinanti indesiderate sono rimosse dall’ambiente. Attraverso l’applicazione di soluzioni e di dispositivi a tecnologia avanzata, è possibile potenziare le condizioni naturali in grado di fornire un sostegno a tutte le forme viventi presenti nella biosfera terrestre.
Caratteristiche dei microorganismi
La microbiologia è quella branca della biologia che studia la fisiologia, la riproduzione, la simbiosi, l’impatto sugli ecosistemi, la presenza in natura e l’importanza in campo scientifico e industriale di piccoli organismi viventi non visibili a occhio nudo. Essa comprende lo studio dei batteri (batteriologia), dei funghi (micologia), dei protozoi (protozoologia) e dei virus (virologia). A causa della loro versatilità biochimica e ambientale, i batteri sono gli organismi più comunemente usati nei sistemi progettati per distruggere le sostanze inquinanti biodegradabili. Essi sono utilizzati frequentemente anche nella ricerca biologica e nelle trasformazioni biochimiche.
Gli organismi multicellulari, come le piante e gli animali, sono costituiti da cellule eucariotiche. Le cellule delle forme di vita inferiori, come i batteri e le alghe blu-verdi, sono procariotiche. A differenza delle cellule procariotiche, che non contengono organuli circondati da membrane, quelle eucariotiche contengono nel loro citoplasma organuli intracellulari quali i vacuoli, i mitocondri, il reticolo endoplasmatico e il nucleo, che sono separati dal citoplasma mediante membrane proprie. Una membrana plasmatica semipermeabile separa il citoplasma dall’ambiente extracellulare.
I Procarioti sono da 1000 a 10.000 volte più piccoli degli Eucarioti e molti di loro sono mobili. I batteri possono essere sferici, a bastoncino o spiraliformi e sono i più piccoli tra i microbi unicellulari, con dimensioni tipiche che variano da 0,5 a 3 μm. Essi possono essere larghi anche 0,1 μm e lunghi 50 μm; la loro forma è definita da una parete cellulare strutturale e sono dotati di un unico cromosoma circolare a doppio filamento. Molti batteri importanti dal punto di vista ambientale contengono ulteriori informazioni genetiche su un plasmide. Essi si riproducono a velocità estremamente elevate con tempi di divisione che comunemente possono richiedere da 1 a 4 ore; ciò li rende particolarmente utili per tutti i processi di trattamento biologico. Non tutti i microorganismi importanti per l’ambiente sono Procarioti. I funghi e le alghe sono Eucarioti e sono stati utilizzati, anche se meno estesamente, nei sistemi progettati per l’eliminazione di sostanze inquinanti. Sia i funghi sia le alghe sono, ovviamente, ubiquitari nell’ambiente e danno contributi significativi ai processi naturali di depurazione biologica.
Alcuni batteri crescono in strato sottile (biofilm) attaccati a superfici, altri crescono meglio senza attaccarsi (cioè in sospensione come organismi separati, in grappoli o in fiocchi). Gli aerobi stretti proliferano solo in presenza di ossigeno; gli anaerobi stretti non possono sopravvivere in presenza di ossigeno, mentre gli anaerobi facoltativi crescono sia in presenza che in assenza di ossigeno. I microorganismi convertono le sostanze inquinanti in nuova massa cellulare, diossido di carbonio, acqua e altri prodotti finali che variano a seconda della natura delle sostanze inquinanti e degli specifici microorganismi presenti.
Per la crescita, i microorganismi necessitano di una fonte di energia, di una fonte di carbonio e di nutrienti. Gli organismi fotoautotrofi, come le alghe, utilizzano la luce del Sole come fonte di energia e il diossido di carbonio come fonte di carbonio; gli organismi chemoautotrofi usano una sostanza inorganica ridotta come l’ammoniaca o il ferro a numero di ossidazione +2 quale fonte di energia e il diossido di carbonio come fonte di carbonio; gli organismi eterotrofi utilizzano sostanze organiche come fonte sia di energia sia di carbonio. I nutrienti sono gli elementi che non si trovano né nella fonte di carbonio né in quella energetica, e sono necessari alle cellule viventi per produrre proteine, carboidrati, grassi, acidi nucleici, che contengono un’ampia varietà di elementi tra cui carbonio, idrogeno, ossigeno, azoto, fosforo e zolfo. Inoltre le proteine, se utilizzate come enzimi, hanno bisogno di metalli in tracce quali sodio, potassio, ferro, manganese, magnesio e calcio. I nutrienti richiesti a concentrazioni relativamente elevate sono detti macronutrienti (per es., azoto e fosforo), quelli necessari a basse concentrazioni prendono il nome di micronutrienti (per es., metalli presenti in tracce). Alcune cellule non contengono l’informazione genetica per sintetizzare determinate sostanze organiche intracellulari necessarie, come alcuni amminoacidi e vitamine. Sia i nutrienti inorganici sia questi essenziali intermedi organici preformati devono essere presenti nell’ambiente oppure devono essere forniti agli organismi affinché questi possano crescere.
Una popolazione microbica s’instaura nell’ambiente o in un sistema progettato per l’eliminazione delle sostanze inquinanti se sono disponibili tutti i nutrienti necessari, una fonte di carbonio e una di energia, e se i suoi membri contengono l’informazione genetica per produrre gli enzimi catabolici che estraggono energia dalle sostanze inquinanti. L’informazione genetica per la maggior parte degli enzimi catabolici e per tutti quelli anabolici è presente nel cromosoma. Ulteriori informazioni genetiche, specialmente per la produzione di enzimi che catalizzano la degradazione delle sostanze xenobiotiche, si trovano di solito nei plasmidi. Di conseguenza, i geni dei plasmidi spesso forniscono all’associazione microbica le informazioni necessarie per liberare l’ambiente da sostanze inquinanti indesiderate.
Gli impianti progettati per il trattamento dei liquami domestici sono basati quasi sempre su processi biologici; il flusso delle acque di scarico contiene tutti i nutrienti essenziali per lo scopo. Questi sistemi impiegano di solito colture miste di batteri (piuttosto che una coltura pura); anche se sono presenti altri microorganismi (per es., protozoi), i batteri sono i principali responsabili della demolizione aerobica delle sostanze organiche e dell’eliminazione dell’azoto e del fosforo. Nel trattamento biologico delle acque di scarico domestiche vengono impiegati sia sistemi a biofilm fisso (per es., filtri percolatori), sia sistemi in cui si ha una crescita a biomassa sospesa (per es., fanghi attivi). La maggior parte dei sistemi moderni è del tipo a biomassa sospesa. I composti solidi di origine biologica prodotti in tali sistemi contengono biomassa vivente e morta insieme con sostanze solide sospese che sono parzialmente decomposte dai batteri presenti nell’impianto di trattamento. Questi fanghi di depurazione di solito vengono ulteriormente trattati in digestori aerobici o anaerobici. I primi stabilizzano i fanghi di depurazione mineralizzando le sostanze organiche biodegradabili (cioè producendo diossido di carbonio e acqua) e riducendo così la massa di fanghi di depurazione che deve essere eliminata negli inceneritori o smaltita sul terreno come ammendante del suolo o come fertilizzante. I digestori anaerobici ottengono risultati simili producendo metano e idrogeno, gas spesso utilizzati per produrre elettricità.
In passato, le acque di scarico industriali erano trattate più frequentemente utilizzando procedimenti chimici e fisici invece che sistemi basati su processi biologici. Poiché i sistemi biologici sono di solito meno costosi dei loro equivalenti fisici e chimici e a causa dell’alto costo associato alle attuali stringenti necessità di rispetto ambientale, molte industrie sono impegnate nello sviluppo intensivo di impianti di trattamento biologico, quando possibile. Le sostanze contaminanti presenti nelle acque di scarico industriali spesso costituiscono un problema più complesso rispetto a quelle presenti negli scarichi domestici. La maggiore varietà di sostanze xenobiotiche a concentrazioni superiori, la carenza di nutrienti, le temperature, il pH, la salinità e i livelli di metalli pesanti, nonché le più basse velocità di crescita batterica, richiedono una maggiore attenzione negli studi di trattabilità tesi a determinare i parametri necessari al progetto. Tuttavia, una volta scelti, i bioreattori aerobici (e talvolta anche gli anaerobici) possono essere progettati e fatti funzionare così da soddisfare i limiti determinati dalle normative vigenti.
Trasformazioni biochimiche
Per catalizzare una data reazione biochimica è richiesto un enzima specifico, che è composto da una o più proteine. Una proteina necessita di almeno un gene impegnato a dirigere la sua sintesi e di coenzimi (molecole organiche non proteiche) e/o cofattori (ioni inorganici) che si legano o si associano alla proteina per consentire l’attività catalitica desiderata. L’informazione genetica specifica (ovvero il DNA, di un microorganismo o di una cellulla) determina quali enzimi verranno prodotti. Nei batteri l’informazione genetica è localizzata nel cromosoma o in un plasmide.
Perché si verifichi la crescita, la fonte di nutrimento o substrato (ovvero la sostanza inquinante) deve essere in grado di passare attivamente attraverso la membrana cellulare. Per i batteri eterotrofi il substrato può essere un carboidrato, una proteina, un lipide o qualche altro composto organico di origine biologica o xenobiotica. I substrati costituiti da molecole grandi devono essere parzialmente degradati (per es., mediante enzimi) nell’ambiente extracellulare, cosicché i prodotti possono essere attivamente trasportati attraverso la membrana cellulare. Una volta trasportati, questi composti devono costituire un substrato per gli enzimi intracellulari. Tali composti sono considerati biodegradabili quando si verifica una serie di reazioni che si conclude con la formazione di prodotti finali innocui. Se si ottiene la loro completa mineralizzazione, i prodotti finali sono ioni inorganici semplici (per es., Cl− e NH4+), diossido di carbonio e acqua.
In generale, i substrati e le fonti di energia sono composti organici ridotti per gli eterotrofi e composti inorganici ridotti per gli autotrofi e vengono di solito chiamati elettrondonatori. L’energia o gli elettroni sono estratti dai substrati e trasferiti a elettronaccettori extracellulari e intracellulari. I comuni elettronaccettori extracellulari comprendono l’ossigeno, le forme ossidate dell’azoto (nitriti e nitrati) e i solfati. Durante il catabolismo una parte degli elettroni immagazzinati originariamente nel substrato viene trasferita per via enzimatica alle forme ossidate dei nucleotidi flavina e nicotinammide, producendo le forme ridotte di essi, per l’esattezza un flavinadenindinucleotide ridotto (FADH2) e due nucleotidi nicotinammidici ridotti (NADH + H+ e NADPH + H+). Altri importanti prodotti del catabolismo sono l’energia chimica immagazzinata (per es., l’adenosintrifosfato, ATP) e gli intermedi a bassa massa molecolare. Durante i processi anabolici i nucleotidi ridotti vengono utilizzati insieme all’energia chimica per trasformare i prodotti intermedi in macromolecole. In questi processi i nucleotidi ridotti aiutano a ridurre i precursori intracellulari e vengono ossidati a FAD, NAD+ e NADP+, che verranno poi riutilizzati durante i processi catabolici. I nucleotidi ridotti vengono ossidati anche utilizzando elettronaccettori extracellulari o esogeni. Queste reazioni producono grandi quantità di ATP e aumentano significativamente la velocità con cui gli elettrondonatori vengono convertiti in biomassa, diossido di carbonio, acqua e altri sottoprodotti innocui.
Considerare gli impianti biologici di trattamento come dispositivi di trasferimento di elettroni fornisce le basi necessarie a progettarli e farli funzionare. Nel linguaggio degli ingegneri ambientali ciò diventa chiaro facendo un bilancio di massa riferito alla richiesta chimica di ossigeno (COD, Chemical oxygen demand) in tutto il sistema. Il COD di un campione è la quantità di ossigeno necessaria a convertire tutte le sostanze organiche presenti nel campione in diossido di carbonio e acqua. Questa misurazione di solito si ottiene utilizzando un forte agente ossidante quale il dicromato o il permanganato. In un sistema biologico aerobico o in sistemi anaerobici che hanno elettronaccettori esogeni alternativi, quali i nitriti e i nitrati (questi sistemi vengono chiamati anossici), la quantità totale di ossigeno o dell’elettronaccettore esogeno alternativo (espressa come equivalenti di ossigeno) consumata dalla biomassa deve essere uguale alla massa di COD che entra nel sistema meno la massa di COD che esce dal sistema (cioè nelle acque di scarico trattate e nei fanghi di depurazione di scarico). Nei sistemi anaerobici senza elettronaccettori esogeni alternativi, la quantità totale di COD che entra deve essere uguale alla quantità di COD che esce dal sistema. Perciò la somma delle quantità di idrogeno e di metano (espresse come COD) generate deve essere uguale alla quantità di COD che entra, meno la quantità di COD che esce dal sistema nelle acque di scarico trattate e nei fanghi di depurazione.
Stechiometria e cinetica
La velocità con la quale gli elettrondonatori (cioè i prodotti inquinanti) si accumulano nell’ambiente dipende da più fattori, tra i quali la loro natura, l’informazione genetica nell’associazione microbica presente nel punto di contaminazione, la disponibilità di nutrienti, la presenza di tossine inorganiche e organiche, l’adeguatezza delle condizioni ambientali quali pH, salinità e temperatura, la velocità con cui viene fornito ossigeno come elettronaccettore esogeno.
Per poter integrare questi fattori in uno schema teorico che permetta di calcolare la velocità con cui ha luogo la depurazione biologica in natura o in sistemi progettati a tale scopo, i dati devono essere raccolti e tradotti in termini stechiometrici e cinetici. Gli schemi di reazione così sviluppati possono poi essere usati mediante modelli matematici basati sul principio di conservazione (per es., bilancio di massa) per stabilire la distribuzione delle sostanze inquinanti nell’ambiente.
Una reazione semplice può essere scritta nel seguente modo:
[1] v1 A1 + v2 A2 + ... + vi Ai + ... + vm Am = 0
[2] ovvero formula
dove A1, A2 …. Am sono gli m componenti di questa reazione e v1, v2 … vm sono i rispettivi coefficienti stechiometrici con vi 〈 0 per i reagenti e vi > 0 per i prodotti. La velocità di reazione r è una funzione definita dalla velocità di formazione di ciascun componente (per es., rji per l’i-esimo componente) ed è data dalla relazione:
[3] formula.
Questa notazione può essere facilmente estesa a sistemi in cui sono coinvolte più reazioni, come di seguito indicato:
[4] formula
ovvero
[5] formula
dove vi,j è il coefficiente per il componente Ai nella j-esima reazione, vi,j 〈 0 per i reagenti e vi,j > 0 per i prodotti, n è il numero delle reazioni e m il numero dei componenti. Come per il sistema a singola reazione, la velocità di ciascuna reazione j-esima in un sistema a reazioni multiple, rj, è una funzione definita dalla velocità di formazione di ciascun componente nella specifica reazione considerata ed è data dalla relazione:
[6] formula
[7] (rfi )j = vi,j rj
[8] rfi = (rfi )1 + (rfi )2 + ... + (rfi )n
dove (rfi)j è la velocità di formazione del componente i-esimo nella reazione j-esima e rfi è la velocità complessiva di formazione del componente i-esimo nel sistema a n reazioni, semplicemente uguale alla somma delle velocità di formazione del componente i-esimo in ciascuna di esse.
Descriviamo ora un esempio di relazioni stechiometriche e cinetiche comunemente utilizzate nella progettazione dei sistemi di trattamento biologico dei liquami. In questo esempio due reazioni, una di crescita e una di morte cellulare, sono presentate in relazione alla massa:
[9] (−1 )S + (−0,58 )O2 + (+0,3 )B = 0
(−1 )B + (−0,9 )O2 + (+0,11 )CD = 0.
La prima reazione descrive la crescita di una coltura mista di batteri aerobi; essa comprende due reagenti, il substrato (S) e l’ossigeno (O2) e, come unico prodotto, la biomassa (B). Il coefficiente stechiometrico della biomassa nella prima reazione (vB,1) rappresenta il rendimento in biomassa per ciascuna unità di massa di substrato o di sostanza inquinante consumata. In questa reazione per ciascun chilogrammo di substrato utilizzato verrebbero prodotti 0,3 kg di biomassa. La seconda reazione, quella di morte cellulare, rappresenta la respirazione endogena. In pratica, per ciascun chilogrammo di biomassa consumata vengono consumati 0,9 kg di ossigeno e prodotti 0,11 kg di detriti cellulari (CD, Cellular debris) o biomassa morta. Le equazioni che esprimono la velocità di reazione sono rispettivamente:
[10] formula
[11] formula
dove CB è la concentrazione della biomassa, K2 è il coefficiente di respirazione endogena e μ, ossia la velocità di crescita specifica della biomassa espressa in chilogrammi di biomassa prodotta per chilogrammo di biomassa presente per unità di tempo, è data dall’espressione classica di Monod:
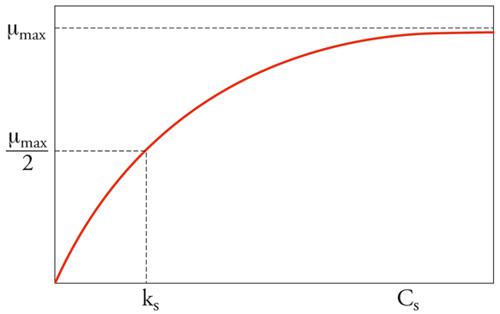
[12] formula.
In questa relazione μmax è la velocità massima di crescita specifica della biomassa, kS è la costante di semisaturazione, CS è la concentrazione del substrato. La forma funzionale dell’espressione di Monod è mostrata graficamente nella fig. 2. L’esame della curva e della sua forma matematica mostra che l’espressione cinetica è approssimativamente del primo ordine rispetto al substrato a basse concentrazioni (cioè quando CS≪kS), ed è di ordine zero (cioè indipendente dalla concentrazione di substrato) per concentrazioni di substrato elevate (cioè quando CS≫kS); ha un valore massimo asintotico μmax ed è uguale a μmax/2 quando la concentrazione del substrato è numericamente uguale a kS. Nei sistemi biologici di trattamento dei liquami i tipici valori medi di μ variano tra 0,05÷0,3 giorno−1.
La funzione della velocità per l’equazione di morte cellulare di solito viene considerata di primo ordine rispetto alla concentrazione della biomassa, come mostrato. Un valore tipico del coefficiente di respirazione endogena K2 è 0,05 giorno−1. Ciò suggerisce che circa il 5% della biomassa verrà perso ogni giorno per morte o respirazione endogena.
Il valore rfB per questo sistema a due reazioni è dato da:
[13] formula.
Perciò, la velocità specifica di formazione della biomassa per entrambe le reazioni, rfB/CB, è uguale a μ − K2. Di conseguenza, la quantità netta di biomassa prodotta è data dalla differenza tra la quantità di biomassa prodotta nella reazione di crescita e la quantità di biomassa consumata per effetto della respirazione endogena definita dalla seconda reazione. Questa è una considerazione importante nella progettazione, perché i costi operativi e di capitale associati al trattamento dei fanghi di depurazione costituiscono frazioni apprezzabili dei corrispondenti costi totali.
A causa dell’alto costo dell’energia, e considerato l’impatto critico che l’inadeguato apporto di ossigeno ha sul rendimento complessivo, particolare attenzione deve essere prestata anche alla velocità di formazione dell’ossigeno, rfO, data da vO,1r1+vO,2r2. La velocità specifica di formazione dell’ossigeno per entrambe le reazioni, rfO/CB, viene di solito indicata come velocità specifica di consumo di ossigeno (SOUR, Specific oxygen uptake rate) e, a eccezione della velocità di consumo di ossigeno dovuto a respirazione endogena, che ha luogo a concentrazione di substrato pari a zero, presenta un andamento simile a quello della espressione di Monod nella fig. 2.
Il processo di depurazione biologica
I sistemi di trattamento biologico utilizzano comunità di microbi per rimuovere o eliminare sostanze organiche e inorganiche, pericolose o meno, presenti nei liquami domestici, nei liquami industriali, nei percolati, nell’aria e nei terreni. Questi sistemi, appositamente studiati, riproducono la situazione ambientale e superano i limiti della natura, soprattutto quelli che derivano da squilibri locali che rallentano la velocità di autopurificazione.
Le caratteristiche delle comunità di microbi selezionate e arricchite nei sistemi artificiali dipendono da numerosi fattori, tra cui: (a) il tipo di sostanza inquinante e il modo in cui essa varia nel tempo; (b) la portata massima delle singole sostanze inquinanti; (c) la presenza o l’assenza di elettronaccettori (cioè la presenza di condizioni aerobiche, anossiche o anaerobiche); (d) la frequenza di cambiamento delle condizioni aerobiche, anossiche o anaerobiche; (e) la presenza delle condizioni di abbondanza e carestia (per es., la frequenza con cui si passa da elevati a bassi tassi di crescita); (f ) la natura dei vari prodotti secondari che si formano; (g) la tendenza all’adesione della biomassa (cioè, crescita in condizioni di biomassa sospesa o di biomassa adesa).
Sistemi di trattamento biologico appositamente studiati e adeguatamente funzionanti possono selezionare e arricchire l’associazione microbica e poi modificare il suo stato fisiologico per gestire le normali variazioni del carico inquinante. Questo livello di controllo è molto difficile da raggiungere in natura.
Sistemi per la depurazione biologica delle acque di scarico
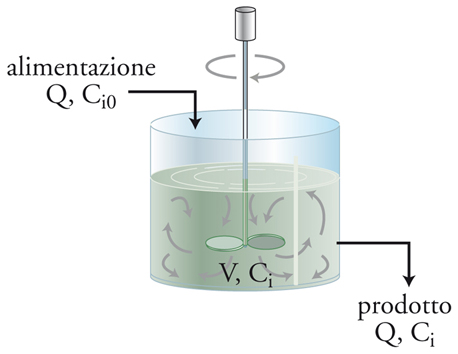
Convenzionalmente i reattori biologici vengono progettati utilizzando configurazioni ideali per modellare o rappresentare sistemi reali. Comunemente vengono impiegate due configurazioni ideali: quella a mescolamento completo (a flusso discontinuo, semidiscontinuo o continuo: batch, semibatch o continuous flow) o quella con flusso a pistone (con flusso continuo con grado di retromescolamento nullo). I reattori a flusso continuo possono essere a riciclo o senza riciclo. Da queste rappresentazioni ideali di reattori vengono facilmente sviluppati bilanci di massa o modelli matematici. I bilanci di massa che risultano dall’applicazione dei principi di conservazione sono gruppi di equazioni algebriche e/o equazioni differenziali ordinarie e/o equazioni differenziali alle derivate parziali. I gruppi di reazioni o modelli che si ottengono sono usati per la progettazione dei reattori e/o per la loro analisi.
Una generalizzazione della legge di conservazione è la seguente: la velocità con cui Ai si accumula nel sistema è data dalla somma algebrica della velocità (positiva) con cui entra nel sistema, della velocità (negativa) con cui esce dal sistema, della velocità (positiva) con cui si forma nel sistema e della velocità (positiva o negativa) con cui Ai entra o esce dal sistema tramite altre sorgenti o altri pozzi. Quindi, un componente Ai si accumula nel sistema quando la sua velocità netta d’ingresso eccede la sua velocità netta di uscita da esso. In condizioni stazionarie, nel sistema non si verifica accumulo e le velocità nette di ingresso e di uscita sono uguali. Le relazioni sviluppate precedentemente per esprimere la stechiometria e la cinetica di reazione sono indipendenti dal sistema preso a modello. Poiché i coefficienti stechiometrici dei reagenti sono negativi, la loro velocità di formazione è negativa. In un sistema a reazioni multiple, alcuni componenti sono sia reagenti sia prodotti, a seconda della reazione che viene presa in considerazione. In questo caso la velocità finale di formazione può essere sia positiva sia negativa durante il corso della reazione. La nitrificazione, cioè l’ossidazione sequenziale dell’ammoniaca a nitrito e del nitrito a nitrato a opera di due diversi batteri autotrofi, fornisce un eccellente esempio di tale evento. In un reattore batch spesso si osserva che il nitrito aumenta durante le prime fasi della nitrificazione, via via che l’ammoniaca viene ossidata a nitrito, e poi diminuisce dopo che tutta l’ammoniaca è stata ossidata e, quindi, la produzione di nitrito cessa. Nel seguito saranno decritti cinque tipi di reattori: (a) il reattore batch a mescolamento completo (CMBR, Completely mixed batch reactor); (b) il reattore a flusso continuo a mescolamento completo (CMFR, Completely mixed flow reactor); (c) il reattore batch sequenziale (SBR, Sequencing batch reactor); (d) il reattore con flusso a pistone (PFR, Plug flow reactor); (e) il reattore con flusso a pistone con dispersione (PFDR, Plug flow reactor with dispersion).
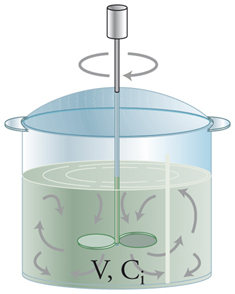
CMBR. Una semplice rappresentazione schematica di un reattore batch è mostrata nella fig. 3, dove V rappresenta il volume del liquido e Ci è la concentrazione dell’i-esimo componente, Ai. Poiché il reattore è a mescolamento completo, Ci rappresenta la concentrazione del componente i-esimo in qualunque punto del reattore. Il bilancio di massa di un CMBR può essere scritto:
[14] formula
in cui Ci(0) è noto, oppure, per V costante:
[15] formula
in cui Ci(0) è noto. Nel bilancio di massa la concentrazione iniziale dell’i-esimo componente è Ci(0) e qualunque ingresso (per es., il rifornimento di ossigeno mediante rimescolamento o aerazione) o uscita (per es., la volatilizzazione delle sostanze inquinanti con un’elevata pressione di vapore) è rappresentato da Si. Il segno + è usato per gli ingressi, il segno − per le uscite; naturalmente in questa espressione devono essere considerati tutti gli ingressi e tutte le uscite.
I bilanci di massa, come quello espresso dalla [15] sono spesso utilizzati per sviluppare le relazioni stechiometriche e cinetiche. Per il sistema a due reazioni precedentemente descritto, può essere usato un bilancio di massa del substrato per un CMBR a volume costante e nessun altro ingresso o uscita per valutare μmax e kS. Ciò si ottiene riportando nel grafico il reciproco della velocità di rimozione del substrato specifico, cambiato di segno
[16] formula
rispetto al reciproco della concentrazione del substrato. Questo grafico di doppi reciproci è praticamente identico a quello utilizzato per valutare i coefficienti della cinetica enzimatica di Michaelis-Menten.
I CMBR vengono impiegati piuttosto frequentemente nell’industria delle fermentazioni. Il loro utilizzo su vasta scala nei sistemi di trattamento biologico delle acque di scarico è meno diffuso. Il sistema SBR, tuttavia, prevede un periodo di trattamento batch durante la sua normale attività.
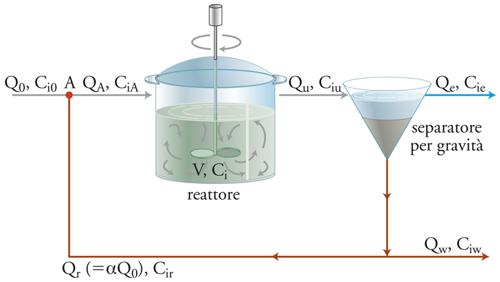
CMFR. Tali reattori sono comunemente utilizzati nel trattamento biologico di acque di scarico con colture miste che crescono in fase sospesa in sistemi chiamati a fanghi attivi. Spesso questi sistemi vengono fatti funzionare con riciclo, talvolta senza. I sistemi senza riciclo comprendono una tipologia di reattori per trattamenti biologici di acque di scarico utilizzate nelle comunità rurali. Questi sistemi sono stati chiamati fossi di ossidazione, stagni di stabilizzazione, lagune, e così via. Lo schema per un CMFR senza riciclo è rappresentato nella fig. 4. La portata volumetrica e la concentrazione del componente i-esimo nella corrente di alimentazione vengono indicate rispettivamente come Q e Ci0. Il bilancio di massa di un CMFR può essere scritto:
[17] formula
dove Ci(0) noto, per V costante:
[18] formula
dove Ci(0) è noto.
Il tempo di permanenza idraulica (HRT, Hydraulic residence time) τ è uguale al volume del reattore diviso la portata volumetrica. L’HRT per tali sistemi può essere breve (1 giorno) o lungo (10 giorni). Questi stagni o lagune sono spesso progettati per utilizzare le alghe come fonte di ossigeno. Poiché durante i mesi estivi le alghe crescono molto, se l’HRT è maggiore di 2 giorni, gli effluenti da questi sistemi sono considerati essi stessi una fonte d’inquinamento.
I microbiologi e i biochimici che usano i CMFR da laboratorio senza riciclo li chiamano chemostati e di solito utilizzano colture pure, piuttosto che colture miste. Il modello dei CFMR senza riciclo è stato utilizzato anche per descrivere il comportamento di bacini idrici naturali come stagni o laghi. I progettisti spesso utilizzano i CMFR con riciclo per gli studi di trattabilità su scala di laboratorio e su scala pilota. Lo schema semplificato di tale sistema è rappresentato nella fig. 5. Poiché il reattore biologico è a mescolamento completo, la concentrazione del componente i-esimo nel reattore è identica alla concentrazione dello stesso componente nell’effluente da reattore.
La concentrazione della biomassa nei CMFR con riciclo è di molto superiore rispetto a quella di un CMFR senza riciclo e di solito varia da circa 1,5 g/l a circa 4 g/l. L’HRT che ne risulta è corrispondentemente inferiore: per esempio quello per gli impianti di trattamento dei liquami domestici varia da 0,25 a 1 giorno, mentre quello per i sistemi di trattamento dei liquami industriali varia da 0,25 a 10 giorni.
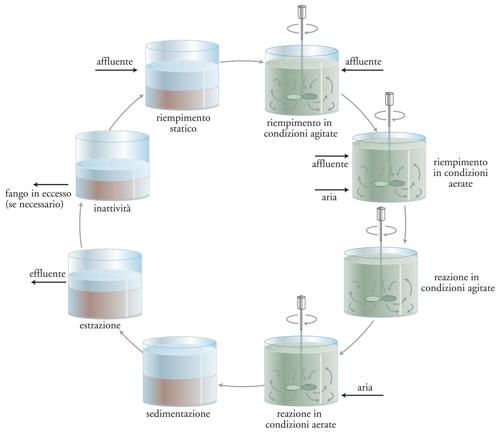
SBR. Si tratta di un sistema di crescita in sospensione di colture miste che viene fatto funzionare periodicamente. Anche se è chiaramente un sistema a fanghi attivi, l’SBR differisce da un sistema a flusso continuo convenzionale. L’SBR è un sistema regolato nel tempo (time-oriented system) nel quale il flusso materiale, l’input energetico e il volume utile delle vasche variano a seconda di una certa strategia operativa periodica e predeterminata. Poiché si tratta di un sistema a fanghi attivi non stazionario, l’operatore può impiegare un’ampia varietà di strategie operative per selezionare e arricchire l’associazione microbica desiderata.
Come si può vedere dalla fig. 6, ciascun reattore in un sistema SBR ha cinque modalità operative fondamentali, o periodi, ciascuna dei quali prende il nome dalla sua funzione primaria: (a) riempimento; (b) reazione; (c) sedimentazione; (d) estrazione; (e) inattività. I periodi di riempimento, nei quali i liquami contaminati vengono ricevuti e hanno inizio le reazioni, e quelli di estrazione, nei quali l’effluente trattato viene scaricato, sono necessari per ciascun ciclo di un dato reattore. I periodi di reazione (durante i quali le reazioni volute vengono portate a termine), di sedimentazione (in cui i fanghi di depurazione vengono separati dall’effluente trattato), e di inattività (un periodo di inoperosità tra quelli di estrazione e riempimento) vengono inclusi o esclusi a seconda delle necessità. Per esempio, la semplice regolazione del tempo concesso per la reazione in condizioni di aerazione e per la reazione in condizioni di mescolamento controlla l’efficacia della rimozione biologica delle forme inorganiche di azoto e fosforo, il grado di rigonfiamento (bulking) dei fanghi (cioè le caratteristiche di sedimentazione della biomassa), e la rimozione dei composti organici pericolosi che si trovano negli scarichi industriali e nei percolati di discariche. L’SBR si comporta formalmente come un CMFR a volume variabile affiancato in serie da un CMBR.
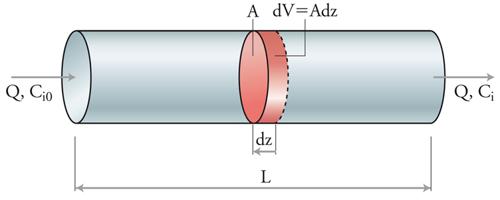
PFR e PFDR. Questi reattori possono essere rappresentati semplicemente con lo schema illustrato nella fig. 7. In essi l’HRT è definito nello stesso modo che nel CMFR, ma rappresenta il tempo di transito nel reattore. Il bilancio di massa per un PFR può essere scritto:
[19] formula.
Le condizioni iniziali sono: Ci(0,z)=Fi(z)=funzione nota; quelle al contorno sono: Ci(t,0) noto; vz è la velocità nella direzione z(vz= Q/A). Il bilancio di massa per un PFDR può essere scritto:
∂Ci ∂Ci ∂2Ci
[20] ____ = − vz ___ − Di ____ rfi ± Sfi .
∂t ∂z ∂z2
Le condizioni generali sono: Ci(0,z)=Fi(z)=funzione nota; quelle al contorno sono: Ci(t,0) e ∂Ci(t,L)/∂z noti. Le equazioni di bilancio di massa sopra riportate sono basate sull’assunzione che A, Q e Di siano costanti.
La differenza tra i due modelli sta nel coefficiente di dispersione, Di. Come si può vedere dal confronto dei modelli unidimensionali del PFR e del PFDR, il termine convettivo (che comprende la velocità vz), la velocità di formazione, le sorgenti e i pozzi sono uguali. Poiché il meccanismo della dispersione appare espresso come una derivata seconda, per il PFDR sono necessarie due condizioni limite, mentre ne è necessaria solo una per il PFR. Si noti che il modello per un PFR unidimensionale in condizioni stazionarie è identico a quello per un CMBR. La differenza sta nel fatto che il tempo nel PFR è il tempo di percorrenza lungo la coordinata spaziale (HRT) mentre nel CMBR il tempo è quello effettivo. Da questa rappresentazione riferita a un corso d’acqua si ottiene la classica equazione di Streeter-Phelps che esprime l’abbassamento del tenore di ossigeno disciolto. Va notato, inoltre, che un numero infinito di CMFR di dimensione infinitesimale posti in serie equivale a un PFR e che un PFR con riciclo infinito equivale a un CMFR.
Poiché le condizioni di funzionamento dei PFR sono praticamente impossibili da riprodurre a causa dell’energia richiesta per l’aerazione e per il rimescolamento, e tenuto conto della necessità di controllare il rigonfiamento dei fanghi e la rimozione dei nutrienti, i progettisti solitamente utilizzano o i CMFR in serie o gli SBR al posto dei PFR. Il numero dei CMFR in serie dipende dalle necessità del sistema. Per esempio, il controllo sulle caratteristiche di sedimentazione dei fanghi può essere ottenuto con 2 vasche in serie, mentre la rimozione del fosforo biologico richiede ben 5 vasche in serie.
Sistemi per la depurazione biologica dei terreni
La depurazione biologica dei terreni contaminati con composti organici è un problema di grande interesse poiché la natura non è in grado di autodepurarsi in modo tempestivo anche quando i contaminanti da eliminare siano biodegradabili. Per poter accelerare la velocità di disinquinamento bisogna migliorare le condizioni più propizie biologicamente, in termini di disponibilità di nutrienti, di concentrazione di ossigeno, di pH e di tasso di umidità. Quando i problemi determinati da sostanze inquinanti introdotte nei terreni dall’attività umana (per es., metodi impropri di smaltimento, spargimenti accidentali sulla superficie o serbatoi che perdono sottoterra) vengono affrontati con determinazione, si accorcia il tempo richiesto per risanare e vengono diminuiti i costi specialmente se si utilizzano metodi biologici.
I metodi fisico-chimici per eliminare le sostanze inquinanti dal suolo comprendono, di solito, l’incenerimento, l’ossidazione chimica, l’estrazione con vapore, il desorbimento termico a bassa temperatura, il lavaggio del suolo. Questi metodi, tuttavia, possono essere relativamente costosi, perché il contaminante estratto o il terreno incenerito spesso devono essere poi ulteriormente trattati o smaltiti, e ciò va aggiunto al costo complessivo del trattamento. In alternativa molte sostanze inquinanti organiche possono essere facilmente biodegradate dai microbi indigeni del suolo, rendendo così possibile il biorisanamento. Il trattamento biologico è di solito l’opzione meno costosa per i suoli contaminati. Durante il biorisanamento, le sostanze inquinanti sono convertite in acqua, diossido di carbonio, biomassa e prodotti organici stabili che vengono incorporati nel materiale umico del terreno originario (umificazione). Queste reazioni biologiche possono essere promosse nel suolo (in situ) lasciandolo indisturbato o, previa escavazione, in reattori fuori terra (ex situ). Il trattamento ex situ è più costoso rispetto alle tecniche in situ, a causa del costo di movimentazione del terreno, ma permette un migliore controllo del processo e un miglior trattamento. In entrambi i casi molte delle tecnologie basate su principî biologici sono aerobiche e si fondano sullo sviluppo di metodi per fornire ossigeno alla popolazione microbica responsabile del risanamento.
Il trattamento ex situ
Le tecniche ex situ trattano la terra di scavo contaminata in bioreattori fuori terra, che permettono un controllo maggiore del processo, velocità maggiori di reazione e la distribuzione più uniforme dei reagenti rispetto a quanto possibile con le tecniche in situ. Il biorisanamento ex situ avviene di solito in fase solida o in sospensione. Nel biorisanamento in fase solida, un apposito sistema spesso prende la forma di bacini confinati (per es., nel cosiddetto landfarming) o di cumuli (per es., nelle cosiddette biopiles o soil-heaping) costituiti dal terreno contaminato. Nel landfarming l’aerazione è di solito passiva in quanto la quantità complessiva di ossigeno trasferita cresce semplicemente per incremento della superficie esposta all’atmosfera. Nelle biopile l’aria viene immessa per aerazione forzata attraverso il suolo contaminato. L’acqua viene fatta gocciolare o viene spruzzata sul terreno contaminato per ottenere un grado di umidità adatto alla biodegradazione (normalmente tra il 45% e il 65%). Le sostanze nutrienti possono essere fornite in forma solida (per es., come fertilizzanti, letame o compost) o aggiunte in forma disciolta. Spesso ai terreni a grana fine vengono aggiunti materiali di riempimento (paglia e pezzetti di legno) in modo da aumentarne la permeabilità all’aria. L’energia consumata nel landfarming o con l’aerazione forzata è di modesta entità, e ciò rende il biorisanamento in fase solida uno dei metodi meno costosi di trattamento ex situ dei terreni contaminati. Tuttavia, l’efficacia di questo metodo è spesso limitata dall’etero-geneità insita nel sistema di rimozione delle sostanzeinquinanti, dalla bassa velocità e dalla scarsa resa della biodegradazione. Nel biorisanamento in sospensione(chiamato trattamento bioslurry) la decontaminazione di terreni o fanghi inquinati è effettuata mediante l’aggiunta di acqua (di solito 5÷40%) per formare una torbida acquosa, che viene poi mescolata e aerata in una vasca o in una laguna al fine di ottenere la biodegradazione delle sostanze inquinanti.
Il biorisanamento in sospensione è più costoso del trattamento in fase solida a causa dell’energia necessaria a mantenere le particelle di terreno nella condizione di torbida acquosa. Tuttavia, il rimescolamento nei reattori bioslurry diminuisce le resistenze di trasferimento di massa perché disperde le sacche isolate di contaminanti e rompe gli aggregati di argilla e le particelle di limo. L’omogeneizzazione facilita lo stretto contatto tra le sostanze nutrienti aggiunte, i composti inquinanti, i microorganismi e l’ossigeno. Il risultato consiste in maggiori velocità, resa e uniformità della biodegradazione dei composti inquinanti rispetto a quanto di solito si ottiene nei sistemi in fase solida.
L’utilizzazione dei reattori bioslurry seguita dal biorisanamento in fase solida permette di combinare i vantaggi e di minimizzare gli inconvenienti che ciascuno di questi metodi di trattamento presenta quando viene utilizzato singolarmente. In tali sistemi si utilizza una breve decontaminazione in sospensione per ottenere l’omogeneizzazione, seguita dal completamento del trattamento biologico in un sistema a fase solida (a bassa richiesta energetica).
Il trattamento in situ
Le tecniche in situ trattano il terreno contaminato sul posto togliendo l’acqua sotterranea e i gas contaminati e sostituendoli con acqua e gas non contaminati, carichi di ossigeno, nutrienti e altre sostanze necessarie alla biodegradazione degli inquinanti. A causa dei problemi di salute e di sicurezza connessi con lo spostamento di terreni contaminati, soprattutto se contaminati da materiali pericolosi, le varie autorità competenti hanno mostrato di preferire le tecnologie in situ. In tali sistemi il suolo funge da bioreattore. L’erogazione di ossigeno al di sotto della superficie è il passaggio che limita la velocità dei sistemi di biorisanamento in situ. Quattro tipi differenti di tecniche in situ hanno ricevuto le maggiori attenzioni: (a) il biorisanamento in situ (in situ bioremediation), nel quale viene stimolata la biodegradazione delle sostanze inquinanti nella zona satura; (b) la bioventilazione (bioventing), con la quale viene stimolata la biodegradazione delle sostanze inquinanti nella zona insatura (o zona vadosa); (c) la bioinsufflazione (biosparging), nella quale viene stimolata la biodegradazione delle sostanze inquinanti sia nella zona satura sia in quella vadosa; (d) il biorisanamento intrinseco (intrinsic bioremediation), in cui le sostanze inquinanti sono lasciate a biodegradarsi nella zona satura o nella zona vadosa senza particolari interventi attivi (a eccezione dei pozzi di controllo).
I sistemi di biorisanamento in situ consistono di solito in una combinazione di pozzi per l’iniezione di acqua sotterranea (o gallerie o fossi di infiltrazione) e in uno o più pozzi per il recupero delle acque sotterranee. Nella maggior parte dei casi l’acqua sotterranea raccolta viene dapprima trattata per eliminare le sostanze inquinanti, poi arricchita con nutrienti oppure con ossigeno o con entrambi, e, infine, iniettata di nuovo. Il trattamento dell’acqua sotterranea recuperata viene di solito effettuato in unità di stripping con aria, in adsorbitori su carbone attivo, in separatori di acqua dall’olio, in bioreattori, in unità di ossidazione avanzata (per es., con ozono), o in una loro combinazione. L’azoto e il fosforo vengono di solito forniti sotto forma di sali ammoniacali e ortofosfati. L’ossigeno normalmente viene somministrato insufflando aria o ossigeno puro nell’acqua prima di iniettarla di nuovo, oppure aggiungendo acqua ossigenata.
I sistemi di bioventilazione consistono in una serie di pozzi per l’estrazione o l’immissione di aria che si estendono attraverso la zona di contaminazione. I pozzi di estrazione sono più usati dei pozzi di iniezione poiché consentono di controllare meglio la perdita di contaminanti volatili nell’atmosfera. I nutrienti vengono di solito forniti sciogliendoli nell’acqua che viene fatta percolare sull’area contaminata. L’acqua è necessaria nella zona vadosa per evitare l’essiccamento causato dalla ventilazione. È interessante notare che questa tecnologia è derivata dai sistemi di estrazione con vapore dal suolo (SVE, Soil vapor extraction), in cui il principale metodo di rimozione si pensava fosse fisico. Gli utilizzatori dei sistemi SVE non erano in grado di spiegare completamente l’effetto di risanamento che risultava maggiore di quello prevedibile in base alle sostanze inquinanti estratte. La differenza in molti casi, risultò dovuta all’intervento di processi biologici.
La bioinsufflazione (talvolta chiamata air sparging, cioè immissione forzata di aria) è una tecnologia relativamente nuova sviluppata per superare i due processi che limitano maggiormente la velocità del biorisanamento in situ nella zona satura: la disponibilità di ossigeno e la dissoluzione di liquidi in fase non acquosa (NAPL, Non-aqueous phase liquids). Nella bioinsufflazione si inietta aria sotto pressione nella zona satura per fornire l’ossigeno necessario alla biodegradazione delle sostanze inquinanti presenti. Questa tecnica non solo determina una maggiore ossigenazione rispetto al biorisanamento in situ, ma favorisce la dissoluzione dei NAPL mediante l’agitazione e il rimescolamento prodotti dalle bolle d’aria insufflate. L’aumentata dissoluzione dei NAPL incrementa la biodisponibilità di questi nella zona di saturazione. Le bolle prodotte dall’insufflazione inducono un incremento della volatilizzazione delle sostanze organiche contaminanti dalla zona satura alla zona vadosa. Per questa ragione, la bioinsufflazione prevede di solito pozzi per l’estrazione di aria (cioè si combina con la bioventilazione), per il controllo dei composti organici volatili (VOC, Volatile organic compounds).
Il biorisanamento intrinseco (talvolta chiamato biorisanamento naturale o attenuazione naturale) è un processo di correzione nel quale la concentrazione delle sostanze inquinanti nelle falde acquifere contaminate viene ridotta senza interventi progettati ad hoc o manipolazioni dell’ecosistema. Il biorisanamento intrinseco è una tecnica passiva che semplicemente sfrutta la capacità naturale dei microbi adattati a un sito di biodegradare le sostanze contaminanti. Il requisito necessario è che in una falda acquifera contaminata è presente una zona attiva dal punto di vista biologico nella quale un’associazione stabile di microorganismi indigeni si sviluppi e degradi biologicamente le sostanze contaminanti. La zona biologicamente attiva può essere aerobica o anaerobica, a seconda delle condizioni richieste dalla biodegradazione delle sostanze contaminanti. La presenza di una zona biologicamente attiva dipende dal continuo rifornimento di materiali essenziali per la crescita (nutrienti ed elettronaccettori) e si verifica in modo naturale in quel sito. Le sostanze inquinanti, che attraversano la zona biologicamente attiva nelle normali condizioni di flusso in quel punto, vengono consumate dai microorganismi e ciò permette di controllare la corrente di sostanze inquinanti in modo che non si verifichi la migrazione di questa corrente fuori dal sito.
La biofiltrazione
La biofiltrazione è una tecnica per il controllo dell’inquinamento dell’aria ben consolidata in Europa, dove più di 500 installazioni sono state costruite prima del 1991. Negli Stati Uniti un forte interesse per la biofiltrazione è cominciato durante i primi anni Novanta, anche se una viva preoccupazione per l’inquinamento dell’aria c’era già negli anni Sessanta. La crescente consapevolezza ambientalista negli Stati Uniti è stata accompagnata dall’approvazione di norme sempre più severe riguardanti l’ambiente, come si può riscontrare dall’approvazione dell’Air quality act (legge sulla qualità dell’aria) del 1967, del Clean air act (legge per l’aria pulita) nel 1970 e dei Clean air act amendments (emendamenti alla legge per l’aria pulita) nel 1977 e nel 1990.
Il trattamento delle emissioni gassose mediante la biofiltrazione riduce i costi della depurazione ed elimina i flussi secondari e di scarico; tale metodica è altrettanto efficace nella rimozione delle sostanze inquinanti biodegradabili, se non più di altre tecnologie di trattamento. La biofiltrazione è significativamente meno costosa di qualunque altra tecnologia di trattamento. Tuttavia, molte questioni tecniche ne hanno limitato l’uso. Quattro sono i problemi comunemente riportati: (a) eccessiva crescita microbica: la biomassa prodotta in sistemi sovraccaricati o in sistemi fatti funzionare per lunghi periodi di tempo spesso ostruisce i biofiltri, provocando cammini preferenziali, cortocircuiti ed eccessiva perdita di carico attraverso il letto filtrante; (b) inadeguato controllo dell’umidità: l’eccesso di umidità riduce le velocità di trasporto dei VOC e di ossigeno, mentre un’umidità insufficiente limita l’attività microbica; (c) inadeguato controllo del pH e dei nutrienti: elevati o scarsi livelli di pH e un inadeguato rifornimento di nutrienti fanno diminuire o eliminano l’attività microbica; (d) rapidi aumenti del carico di sostanze contaminanti: variazioni rilevanti nelle caratteristiche dei gas di scarico, per esempio concentrazione di VOC e VIC (Volatile inorganic compounds), umidità relativa e temperatura, possono determinare carichi dinamici eccezionali che eccedono le capacità di reazione biologica.
I biofiltri sono nati più di quarant’anni fa per essere utilizzati nel controllo degli odori negli impianti industriali agricoli, di lavorazione degli alimenti e di trattamento delle acque di scarico. L’uso dei biofiltri impiegati in Europa consisteva nell’insufflare l’aria maleodorante attraverso strati di terreno o mucchi di compost. In generale, la biofiltrazione implica il passaggio dei gas contaminati attraverso un mezzo solido poroso che fa da supporto a uno strato biologicamente attivo di microorganismi. Quando i gas fluiscono attraverso il mezzo po-roso e vengono a contatto con il biofilm, le sostanzecontaminanti si trasferiscono dalla fase gassosa alle fasi acquosa e solida (cioè il mezzo di supporto e il biofilm) dove i microorganismi consumano le sostanze contaminanti proprio come operano negli impianti di trattamento biologico per le acque di scarico o per i terreni.
Le componenti fisiche fondamentali di un biofiltro sono un sistema di distribuzione delle emissioni gassose, un mezzo di supporto per la popolazione microbica e un sistema di umidificazione e drenaggio per controllare il tasso di umidità. Solitamente una soffiante forza i gas contaminati attraverso una rete di tubi forati. Questo sistema può essere umidificato in vari modi: (a) saturando l’aria di umidità prima che essa entri nel biofiltro; (b) cospargendo d’acqua la superficie del materiale di riempimento; (c) aggiungendo acqua al letto filtrante con un tubo flessibile; (d) con una combinazione di queste tecniche. Solitamente viene predisposto anche un sistema di drenaggio per eliminare l’acqua in eccesso.
Anche se i materiali di riempimento utilizzati nei letti filtranti convenzionali sono per lo più la torba e il compost, è stata utilizzata un’ampia varietà di altri materiali tra i quali: terra, sabbia, trucioli di legno, corteccia, segatura, carbone attivo, monoliti di ceramica, palline di ceramica, vetro sinterizzato, perline di polistirene e schiuma di poliuretano. Gli additivi tipici ai materiali di riempimento comprendono agenti volumizzanti, agenti tamponanti, nutrienti e microbi. Gli agenti volumizzanti, impedendo che i letti si compattino, aumentano la loro permeabilità per una migliore distribuzione dei gas, e diminuiscono la perdita di carico lungo il letto. Tali agenti includono sfere di polistirene, perlite, vermiculite, corteccia e trucioli di legno. I tamponi regolano il pH contrastando la produzione o il consumo di ioni idrogeno che derivano dall’attività microbica. Quando viene utilizzato un materiale di supporto inorganico i nutrienti vengono aggiunti o con il materiale di riempimento prima di assemblare il biofiltro, oppure in una soluzione nutriente che viene spruzzata sul materiale di riempimento o mescolata con esso dopo la costruzione. Qualunque sia il materiale di riempimento utilizzato, esso deve possedere alcune proprietà particolari, tra cui un’elevata porosità, un’appropriata dimensione dei pori, una bassa densità e la capacità di assorbire l’acqua.
Sistemi alternativi
La biofiltrazione è stato il primo sistema utilizzato per il trattamento biologico dei gas di scarico, ma in seguito sono stati studiati molti altri procedimenti per trattare biologicamente le sostanze inquinanti in fase gassosa. Questi sistemi sono conosciuti come biofiltri percolatori, biolavatori, reattori a insufflazione di gas e reattori a membrana porosa.
Un biofiltro percolatore ha una fase liquida che scorre liberamente. In questo sistema, un flusso contenente le sostanze nutrienti viene fatto continuamente ricircolare sul materiale di riempimento. I materiali di riempimento sono di solito inerti e rigidi e possono essere costituiti da ghiaia, plastica, ceramica o una varietà di altri prodotti. Un biolavatore utilizza una torre o una colonna per trasferire le sostanze inquinanti dal gas alla fase liquida che viene sottoposta a biodegradazione in un reattore separato. Alcune torri utilizzate per il trasferimento delle sostanze inquinanti sono a piatti, altre vengono riempite con materiale inerte, e alcune sono del tipo a spruzzo dove le sostanze inquinanti si trasferiscono nelle goccioline che ricadono nel flusso di gas contaminato. Un reattore a insufflazione di gas è un reattore a liquido (per es., un CMFR) in cui avviene un’intensa insufflazione di gas contaminato. Le sostanze inquinanti si trasferiscono dalla fase gassosa nella fase liquida, dove vengono biodegradate da una coltura di microorganismi che cresce in sospensione. Il reattore a membrana porosa utilizza una membrana idrofobica microporosa costituita da materiali quali il polipropilene, il polietilene o il silicone. Le sostanze inquinanti si trasferiscono attraverso la membrana dalla fase gassosa alla fase liquida, dove vengono degradate da una popolazione microbica che può crescere in sospensione (fanghi attivi) o formando un sottile strato fisso.
Bibliografia
Bailey, Ollis 1986: Bailey, James E. - Ollis, David P., Biochemical engineering fundamentals, New York, McGraw-Hill, 1986.
Baltzis 1998: Baltzis, Basil C., Biofiltration of VOC vapors, biological treatment of hazardous wastes, edited by Gordon A. Lewandowski, Louis J. De Filippi, New York, Wiley, 1998.
Bohn 1992: Bohn, Heinrich, Consider biofiltration for decontaminating gases, “Chemical engineering progress”, 88, 1992, pp. 34-40.
Breeze 1993: Breeze, Lawrence E., The British experience with river pollution, 1865-1876, New York, Lang, 1993.
Brimblecombe 1987: Brimblecombe, Peter, The big smoke: a history of air pollution in London since medieval times, London-New York, Methuen, 1987.
Brownell 1998: Brownell, F. William e altri, Clean air handbook, 3. ed., Rockwille (Md.), Government Institutes, 1998.
Cassidy 1995: Cassidy, David P., Bioremediation of soils contaminated with hydrophobic compounds using slurry and solid phase techniques, University of Notre Dame (tesi di dottorato), 1995.
Colten, Skinner 1996: Colten, Craig E. - Skinner, Peter N., The road to love canal: managing industrial waste before EPA, Austin, University of Texas Press, 1996.
Engels 1845: Engels, Friedrich, Die Lage der arbeitenden Klasse in England, Leipzig, Wigand, 1845 (trad. it.: La situazione della classe operaia in Inghilterra, Roma, Editori Riuniti, 1972).
EPA 1992: EPA, The superfund innovative technology evaluation program: technology profiles, EPA/540/R-92/0n, Washington D.C., U.S. Environmental Protection Agency, 1992.
EPA 1993: EPA, Bioremediation in the field, EPA/540/N-93/001, Washington D.C., U.S. Environmental Protection Agency, 1993.
Fitter 1945: Fitter, Richard S.R., London’s natural history, London, Collins, 1945.
Gottlieb 1993: Gottlieb, Robert, Forcing the spring: the transformation of the American Environmental Movement, Washington D.C., Island Press, 1993.
Hamlin 1987: Hamlin, Christopher, What becomes of pollution: adversary science and the controversy on the selfpurification of rivers in Britain, 1850-1900, New York, Garland, 1987.
Hays 1987: Hays, Samuel P., Beauty, health, and permanence: environmental politics in the United States, 1955-1985, Cambridge-New York, Cambridge University Press, 1987.
Irvine, Ketchum 1988: Irvine, Robert L. - Ketchum, Lloyd H. jr, Sequencing batch reactors for biological wastewater treatment, “CRC critical reviews in environmental control”, 18, 1988, pp. 255-294.
Janssens 1970: Janssens, Paul, Palaeopathology: diseases and injuries of prehistoric man, London, Baker, 1970.
Kehoe 1997: Kehoe, Terence, Cleaning up the great lakes: from cooperation to confrontation, Dekalb, Northern Illinois University Press, 1997.
Kinney 1998: Kinney, Kerry A. e altri, Biodegradation of vapor phase contaminants, in: Bioremediation: principles and practice, edited by Subhas K. Sikdar, Robert L. Irvine, Lancaster, Technomics Press, 1998, I, pp. 601-632.
Lerner 1997: Lerner, Steve, Eco-pioneers: practical visionaries solving today’s environmental problems, Cambridge (Mass.), MIT Press, 1997.
Lesson, Winer 1991: Lesson, G. - Winer, A.M., Biofiltration: an innovative air pollution control technology for VOC emissions, “Journal of the Air & Waste Management Association”, 41, 1991, pp. 1045-1054.
McNeill 1998: McNeill, William H., Plagues and people, New York, Anchor Books, 1998.
Mellanby 1972: Mellanby, Kenneth, The biology of pollution, London, Arnold, 1972.
Meybeck 1990: Global freshwater quality: a first assessment, edited by Michael Meybeck, Deborah V. Chapman, Richard Helmer, Oxford-Cambridge (Mass.), Blackwell, 1990.
Moe 1999: Moe, William M., Operation and performance of a periodically operated gas-phase biofilter using a novel polyure-thane foam medium, University of Notre Dame (tesi di dottorato), 1999.
Moe 1997: Moe, William M. - Irvine, Robert L. - Montemagno, Carlo D., Preliminary investigation of polyurethane foam medium for use in vapor phase biofiltration, in: Proceedings of the 1997 Canadian Society of Civil Engineers/American Society of Civil Engineers Environmental Engineering Conference: Protecting people and the environment, Edmonton, Alberta, Canada, July 23-25, 1997, edited by Stephen I. Stanley, C.I.W. Ward, Edmonton-Montreal, 1997, pp. 1755-1766.
Paehlke 1989: Paehlke, Robert C., Environmentalism and the future of progressive politics, London-New Haven, Yale University Press, 1989.
Ponting 1991: Ponting, Clive, A green history of the world, London, Sinclair-Stevenson, 1991.
Scheffer 1991: Scheffer, Victor B., The shaping of environmentalism in America, London-Seattle, University of Washington Press, 1991.
Tarr 1980: Tarr, Joel A. - McCurley, James - Yosie, Terry F., The development and impact of urban wastewater techno-logy: changing concepts of water quality control, 1850-1930, in: Pollution and reform in American cities 1870-1930, edited by Martin V. Melosi, Austin, University of Texas Press, 1980.
Tchobanoglous, Schroeder 1985: Tchobanoglous, George - Schroeder, Edward D., Water quality, Reading (Mass.), Addison-Wesley, 1985.
Weber, Di Giano 1995: Weber, Walter J. jr - Di Giano, Francis A., Process dynamics in environmental systems, New York, Wiley, 1995.
Wohl 1983: Wohl, Anthony S., Endangered lives: public health in Victorian Britain, London, Dent, 1983.
Zhu 1997: Zhu, Hongwei e altri, The effectiveness of aeration recirculation in controlling VOC emissions from publicly owned treatment works, “Journal of the Air & Waste Management Association”, 47, 1997, pp. 1259-1267.