Fisica medica
Fisica medica
L'espressione 'fisica medica' è una traduzione non corretta dell'inglese medical physics (letteralmente, fisica della medicina), e pertanto sarebbe preferibile usare la locuzione: 'fisica applicata alla medicina'. Storicamente, si potrebbe far risalire la nascita della fisica medica al 1616, quando William Harvey (1578-1657) espose al Royal College of Physicians una teoria sul moto del sangue quasi esclusivamente meccanica, che prescindeva da occulte facoltà innate nel sangue e negli spiriti, concludendo: "Cominciai quindi a riflettere se non potesse esservi un moto, per così dire, circolare". Già molti secoli prima, d'altronde, trovava impiego a fini terapeutici l'energia elettrica prodotta da alcuni tipi di pesci, come il malotteruro del Nilo raffigurato nelle tombe egizie ca. 2700 anni fa e la torpedine bruna, conosciuta nella Grecia e nella Roma antiche e usata dal medico Scribonio Largo nel I sec. a.C.; le scariche prodotte da questi pesci, costituite da correnti faradiche e correnti a basse e medie frequenze, sono affini a quelle erogate dagli apparecchi nei reparti di fisioterapia.
L'elettroterapia moderna può essere ricondotta alle celebri esperienze di Luigi Galvani sulle rane e alla sua disputa con Alessandro Volta. La stimolazione trofizzante dei muscoli scheletrici risale al secolo scorso: Jacques-Arsène d'Arsonval, Jean-Louis Prévost e Federico Battelli, André Djourno, Michel Mosinger e Guy de Bisschop hanno per primi sperimentato l'impiego delle correnti alternate sinusoidali nella stimolazione neuromuscolare; nella seconda metà del Novecento, Stanley Salmons e Greta Vrbova hanno introdotto l'uso di correnti alternate per aumentare la potenza muscolare totale, data dal prodotto della forza per la velocità di contrazione, dimostrando che per aumentare la potenza muscolare bisogna incrementare almeno uno di questi fattori. Oggi l'elettroterapia è diffusa come componente di tipo placebo nel trattamento del dolore. Per l'impiego terapeutico si possono utilizzare sia correnti continue sia correnti variabili.
La fisica medica come scienza nacque alla fine dell'Ottocento, con la scoperta dei raggi X e della radioattività. Nel 1912 fu pubblicato il volume Fisica medica di Carlo Paolo Goggia, primo testo in Italia dedicato a tale disciplina. L'espressione fisica medica indica oggi un ampio settore della fisica, che sviluppa la ricerca e la didattica in connessione con i problemi della salute dell'uomo e che, avvalendosi di principî e metodi della fisica, stabilisce un linguaggio comune per fisici e medici.
La fisica ha offerto alla medicina non solamente un solido complesso di leggi cui obbediscono anche gli organismi viventi, ma anche il concetto di struttura, inteso come ordine peculiare delle parti che costituiscono una cellula. Il fisico e il medico affrontano così insieme i problemi di carattere metodologico sorti con l'impiego di nuove tecniche e con i progressi a esso connessi. Soprattutto a livello di concetti e di metodi, la fisica medica apporta in medicina grandi vantaggi e consente l'impostazione e la soluzione di problemi clinici con mentalità strettamente scientifica. In Italia, il fisico medico è colui che insegna fisica o materie a essa correlate in una facoltà medica, oppure il fisico sanitario, inserito in un ambiente medico-ospedaliero in cui è considerato il professionista specializzato nelle applicazioni mediche della fisica.
Effetti della corrente elettrica sul corpo umano
Il passaggio della corrente elettrica attraverso il corpo umano può causare alterazioni e lesioni, che possono essere temporanee o permanenti. Produce un'azione diretta sui vasi sanguigni, sul sangue, sulle cellule nervose e può determinare alterazioni permanenti sul sistema cardiaco, sull'attività cerebrale e nel sistema nervoso centrale, nonché arrecare danno agli apparati visivo e uditivo. Gli effetti più frequenti e importanti prodotti dalla corrente elettrica sul corpo umano sono i seguenti.
Tetanizzazione. Quando si applica uno stimolo elettrico di intensità e durata opportune a una fibra nervosa collegata a un muscolo, quest'ultimo si contrae e poi torna allo stato di riposo. Se al primo stimolo ne segue un secondo, prima che il muscolo torni allo stato di riposo, gli effetti possono sommarsi; più stimoli opportunamente intervallati contraggono il muscolo in modo progressivo e provocano la cosiddetta contrazione tetanica. Anche la corrente continua, se di elevata intensità, può produrre la tetanizzazione.
Arresto della respirazione. Il valore più elevato di corrente per cui un soggetto è in grado di lasciare la presa della parte in tensione si chiama corrente di rilascio. Una corrente più intensa produce difficoltà di respirazione e asfissia, poiché il suo passaggio determina una contrazione dei muscoli addetti alla respirazione e una paralisi dei centri nervosi che sovraintendono alla funzione respiratoria.
Fibrillazione ventricolare. All'attività del cuore corrispondono un campo elettrico e uno magnetico rilevabili mediante elettrocardiogramma, con opportuni elettrodi posti sul corpo. Se alle correnti fisiologiche si sovrappone una corrente esterna molto più intensa, le fibrille riceveranno segnali elettrici irregolari ed eccessivi, che le faranno contrarre in maniera disordinata, indipendentemente le une dalle altre, e impediranno al cuore di svolgere la sua funzione, facendo insorgere la fibrillazione ventricolare. Questo fenomeno è la causa della stragrande maggioranza di morti per folgorazione.
Ustioni. Sono dovute al passaggio di corrente elettrica che genera calore per effetto Joule in un tratto di tessuto biologico. Le ustioni peggiori si hanno sui tessuti a più alta resistività, vale a dire sulla pelle, e in corrispondenza della densità di corrente massima, ossia nei punti di entrata e di uscita della corrente.
Fisica delle radiazioni
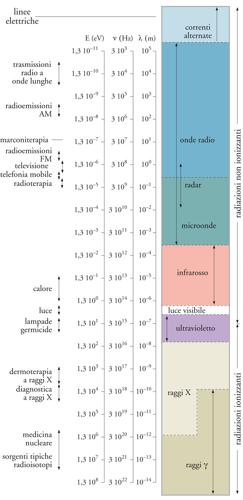
Storicamente, le prime ricerche nel campo della fisica medica erano volte allo studio dell'interazione della radiazione con la materia. Quando la radiazione colpisce i tessuti le particelle cariche, tipicamente alfa e beta, penetrano nel tessuto e perdono energia interagendo elettricamente con gli elettroni degli atomi vicino ai quali transitano. Radiazioni neutre di tipo gamma e X, non accompagnate dal passaggio di carica elettrica, trasferiscono energia in vari modi, ognuno dei quali comporta altresì un'interazione di natura elettrica: entro un decimillesimo di miliardesimo di secondo da quando colpisce un atomo nel tessuto, la radiazione strappa all'atomo un elettrone. Se un elettrone, che ha carica negativa, abbandona un atomo inizialmente neutro, quest'ultimo si carica positivamente (tale processo è chiamato ionizzazione); l'elettrone può produrre a sua volta successive ionizzazioni. L'elettrone libero e l'atomo ionizzato si trovano generalmente in stati molto instabili e prendono parte a una complessa catena di reazioni che implicano mutamenti fisico-chimici e creano nuove molecole, tra le quali alcune particolarmente reattive, chiamate radicali liberi; durante il milionesimo di secondo successivo all'irradiazione i radicali liberi possono interagire fra loro o con altre molecole e, attraverso processi non ancora completamente chiariti, provocare mutamenti chimici nelle molecole, determinanti dal punto di vista biologico per il funzionamento delle cellule. I mutamenti biologici, che possono avvenire in tempi che vanno da pochi secondi ad alcuni decenni dopo l'irradiazione, possono distruggere completamente le cellule, oppure alterarle in maniera tale da causare effetti genetici o il cancro. In fig.3 è riportato lo spettro elettromagnetico delle radiazioni ionizzanti e non ionizzanti.
La fisica delle radiazioni si occupa delle interazioni delle radiazioni ionizzanti con la materia vivente. In particolare, esegue stime o misurazioni della dose di radiazioni assorbite dall'organismo irradiato e mette a punto strumentazioni che riguardano la metrologia primaria delle radiazioni. Il fatto che le radiazioni ionizzanti, oltre agli effetti benefici, ne inducano anche di negativi ha portato alla nascita di una specializzazione, la radioprotezione, che si occupa della prevenzione degli effetti dannosi. L'impiego delle radiazioni ionizzanti, che in diagnostica e radioterapia costituiscono la parte più considerevole dell'esposizione dovuta all'uso di sorgenti artificiali, ha richiesto fin dalle origini che accanto al medico operasse il fisico, in una collaborazione che ha influito sullo sviluppo di nuove tecnologie impiegate in medicina. Si assiste infatti, tanto nel settore diagnostico quanto in quello terapeutico, a una continua evoluzione che negli ultimi anni ha portato alla diffusione di nuove strumentazioni e applicazioni. I fisici radioterapeuti giocano un ruolo centrale in questo campo, poiché sono i professionisti che predispongono i piani di trattamento per la cura del cancro. La normativa italiana prevede due figure professionali per le attività che comportano l'utilizzazione di sostanze radioattive o apparecchi a raggi X: l'esperto qualificato, che ha il compito di proteggere i lavoratori e la popolazione dai rischi derivanti dall'uso delle radiazioni ionizzanti, e l'esperto di fisica medica, che svolge l'attività di protezione delle persone e dei pazienti contro i pericoli derivanti dall'esposizione alle radiazioni ionizzanti per scopi terapeutici.
La radioterapia convenzionale utilizza nel trattamento delle neoplasie dosi massicce (≈100 Gy) di radiazioni ionizzanti di elevata energia (≈1 MeV). La somministrazione di dosi così elevate è resa necessaria dalla bassa probabilità d'interazione che questo tipo di radiazione ha con le strutture cellulari bersaglio: soltanto una piccola frazione della radiazione totale è in grado di produrre danni letali alle cellule tumorali e quindi, per ottenere l'efficacia terapeutica, occorre disporre di un fascio di grande intensità.
La radioterapia trova largo impiego e riveste ampio interesse, non solamente nella distruzione delle cellule tumorali, ma anche per il controllo locale del tumore irradiato. Al fine di incrementare la probabilità di successo senza contemporaneamente aumentare i danni ai tessuti sani, occorre aumentare la selettività dell'effetto biologico della radiazione sulle cellule tumorali, rispetto a quelle normali. Le radioterapie di più largo impiego sono la Curie-terapia, di tipo interstiziale o endocavitaria, in cui sorgenti radioattive sigillate sono inserite direttamente nei tessuti o introdotte in cavità corporee accessibili, e la teleradioterapia, in cui il focolaio neoplastico è irradiato dall'esterno mediante uno o più fasci di radiazioni prodotte da sorgenti radiogene. A causa dei gravi e inevitabili problemi connessi con tali trattamenti, da tempo si sono cercate altre vie per ottenere il medesimo risultato, evitando il più possibile gli effetti nocivi correlati.
Le problematiche connesse con le radiazioni hanno avuto rilevanza nell'inaugurare, tra fisica e medicina, nuovi e diversi rapporti di collaborazione. Da qui la nascita della fisica oncologica, la branca della fisica medica che studia l'interazione di varie radiazioni elettromagnetiche, ionizzanti e non, con i tessuti neoplastici, nel tentativo di distruggere le cellule maligne senza danneggiare i tessuti sani. Esempi ne sono la fototerapia, l'ipertermia e l'inattivazione cellulare mediante radiazioni ionizzanti. Nella fototerapia sono impiegati particolari composti, detti fotoattivatori, con la caratteristica di accumularsi principalmente nei tessuti patologici e, una volta esposti all'azione di radiazioni luminose, produrre reazioni chimiche letali per la cellula che li ospita. La radioterapia di fotoattivazione PAT (Photon activation therapy), utilizzata per la distruzione delle cellule tumorali, sta suscitando interesse crescente nella diagnosi e nella cura dei tumori.
Un posto particolare si è guadagnata l'ipertermia, che sfrutta l'azione del calore, generalmente radiazione infrarossa, per la distruzione delle cellule maligne. Le cellule neoplastiche hanno una maggiore sensibilità alle temperature elevate rispetto a quella delle cellule normali e presentano effetti biologici, come l'ipertermia oncologica esterna: il calore ha sulle cellule malate un effetto letale, che migliora l'efficacia di agenti chemioterapici di nuova e vecchia generazione. Il riscaldamento dei tessuti è realizzato anche sfruttando i campi elettromagnetici con sonde applicate nelle zone tumorali: si riscaldano gli strati, profondi o superficiali, fino a portarne la temperatura attorno a 42,5 °C, così da uccidere le cellule tumorali. Questa tecnica distrugge il tumore anche se non è in fase attiva, agendo su quelle cellule che non rispondono alla chemioterapia e che possono dare una ricomparsa del tumore anche dopo mesi dalla fine della chemioterapia. Con l'avvento di apparecchiature più sofisticate, l'ipertermia può essere oggi proposta come scelta terapeutica ottimale in campo oncologico, associandola alla chemioterapia e alla radioterapia. Per produrre un riscaldamento localizzato della regione dove ha sede la massa neoplastica possono essere utilizzate anche le microonde, che trasportano molta meno energia rispetto alla radiazione infrarossa e permettono una maggiore profondità di penetrazione.
Impieghi della radiazione laser
Tra i mezzi d'indagine che la fisica ha messo a disposizione della medicina, un posto di rilievo è occupato dal LASER (Light amplification by stimulated emission of radiation). Le sorgenti laser sfruttano il meccanismo dell'emissione stimolata ipotizzato nel 1917 da Albert Einstein, le cui prime applicazioni risalgono al 1960. Una radiazione elettromagnetica applicata dall'esterno, di frequenza molto vicina a quella propria della transizione tra due stati quantici, induce l'emissione di radiazione da parte di un atomo. In questo caso i fotoni emessi sono coerenti rispetto alla radiazione incidente, vale a dire i loro contributi si sommano alla radiazione incidente, con la stessa fase temporale e la stessa direzione di propagazione. Le caratteristiche principali di un laser sono: la coerenza spaziale, ossia l'estrema direzionalità del fascio, la coerenza temporale, cioè la monocromaticità della radiazione emessa, e la grande densità di energia che può essere concentrata su superfici molto piccole. La radiazione laser ha impieghi medici che dipendono dalla lunghezza d'onda, dall'intensità del fascio, dalla durata dell'irraggiamento e dal tipo di substrato irradiato. Essi sono riconducibili ai seguenti effetti: (a) effetto antalgico: può agire sulle terminazioni nervose e innalzare la soglia del dolore; (b) effetto antinfiammatorio; può inibire i mediatori chimici nella zona infiammata e aumentare il livello di endorfine nella zona trattata; (c) effetto cicatrizzante: colpendo un tessuto si trasforma in calore con un forte aumento di temperatura locale che porta a una bruciatura con conseguente cicatrizzazione; (d) effetto antiedemigeno: aumentando la velocità di circolo, varia la pressione nei capillari con conseguente assorbimento dei liquidi; (e) effetto biostimolante: stimolazione delle reazioni chimiche cellulari.
Sviluppi recenti
Le fibre ottiche, nel cui interno la luce si può propagare completamente da un estremo all'altro, sono state utilizzate già dagli anni Sessanta del XX sec. per la diagnostica endoscopica. La capacità di trasportare a distanza un'immagine ha permesso il consolidamento di varie tecniche endoscopiche in medicina. Le fibre ottiche, se associate alla luce laser, possono essere usate in vivo, con rilevante interesse diagnostico. Nell'ultimo ventennio, molti sviluppi della fisica applicata alla medicina sono stati realizzati nel campo delle immagini, dell'analisi di segnali, dei calcolatori per la diagnostica, della robotica, degli equipaggiamenti per la riabilitazione e per le articolazioni, delle valvole per il cuore, della produzione di biosensori, biomateriali e strumenti chirurgici. L'area delle bioimmagini comprende quelle metodiche in grado di misurare in vivo e di rappresentare, sotto forma di immagini, la distribuzione e la variazione spaziotemporale di variabili fisiche, funzionali o biochimiche. È suddivisa convenzionalmente in area delle tecniche ionizzanti (medicina nucleare, radiologia, TAC) e area delle tecniche non ionizzanti (NMR, ultrasuoni, termografia, bioelettromagnetismo).
L'introduzione della TAC (Tomografia assiale computerizzata) e le successive generazioni di scanner-TAC hanno comportato un profondo cambiamento nella diagnostica con raggi X, attraverso la produzione di immagini di elevata qualità per le sezioni assiali del corpo. La TAC permette di ricostruire immagini di sezioni trasverse con l'ausilio di un calcolatore. Si è rivoluzionata non soltanto la radiografia, ma anche l'andamento clinico dei pazienti, specie quelli d'interesse neurochirurgico. Altra tomografia è quella a emissione di positroni, detta PET (Positron emission tomography), che mediante l'uso di specifici traccianti radioattivi consente di visualizzare funzioni metaboliche dell'organismo; per esempio, permette la visualizzazione del metabolismo del glucosio e dell'ossigeno nelle regioni del cervello, in seguito a somministrazione di radiofarmaci. La PET ha anche consentito un avanzamento nelle conoscenze sulla demenza; può essere d'aiuto nello studio dei processi associati all'epilessia, ai tumori al cervello, alla malattia di Parkinson; combinata con elettroencefalografia e magnetoencefalografia permette di comprendere le complesse interazioni fra le attività metaboliche ed elettriche del cervello. La PET fornisce dunque informazioni diagnostiche di tipo funzionale complementari a quelle di tipo morfostrutturale fornite dall'ecografia, dalla TAC e dalla risonanza magnetica nucleare. La SPECT (Single photon emission computed tomography), è un'altra tecnica, meno costosa e meno complessa, utile per studiare i fenomeni di perfusione nel cervello e le alterazioni dei vasi sanguigni responsabili, in certe condizioni, dell'epilessia e dei tumori al cervello.
La risonanza magnetica nucleare NMR (Nuclear magnetic resonance), o MRI (Magnetic resonance imaging), trova applicazione nel caso di specie nucleari dotate di momento magnetico non nullo e prevede l'applicazione di un campo magnetico statico e di onde elettromagnetiche a radiofrequenza. Tra i molti elementi chimici d'interesse biologico analizzabili mediante NMR, di particolare importanza per l'applicazione in vivo è l'idrogeno, perché è abbondante nei tessuti biologici, possiede un momento magnetico elevato e ha spin 1/2, il che corrisponde a una sola riga di risonanza. L'utilizzazione in campo medico della NMR è relativamente recente: risale all'inizio degli anni Settanta, e già nel 1977 erano stati costruiti i primi prototipi capaci di contenere l'intero corpo umano all'interno dei magneti e di darne rappresentazioni assiali (NMR a corpo intero). Le immagini che si ottengono rappresentano la distribuzione dei protoni mobili, quali quelli contenuti nell'acqua presente nei vari tessuti: l'idrogeno è molto mobile nell'ambito dei tessuti molli, mentre lo è molto meno nelle strutture rigide, e per questa ragione i tessuti molli danno ottimi segnali e immagini soddisfacenti, mentre nelle ossa il segnale NMR non contribuisce alla formazione delle immagini.
Analisi NMR rivelano dettagliate informazioni anatomiche, specie del cervello, in modo particolare quando si utilizzano immagini eco planari. Recentemente si sono rese disponibili anche immagini di risonanza magnetica nucleare funzionale fMRI (functional Magnetic resonance imaging). La capacità della fMRI di dare informazioni su variazioni locali minime del flusso del sangue cerebrale e di altri parametri sensibili all'attività del cervello ha aperto importanti campi di ricerca su diversi problemi, quali la costruzione della mappa della parte laterale del cervello relativa alla parola, al linguaggio, alla percezione del dolore, all'evoluzione dell'epilessia e dell'apoplessia. La MRA (Magnetic resonance angiography) sta subentrando all'angiografia arteriosa come mezzo per fornire l'immagine dei vasi sanguigni del cervello. La MRS (Magnetic resonance spectroscopy) fornisce invece utili informazioni sui fenomeni che stanno alla base di importanti patologie. Nel caso di traumi o malattie, fornisce informazioni sui meccanismi delle alterazioni nella composizione chimica e nei livelli d'energia delle diverse regioni cerebrali. La MRI è stata usata con successo per individuare i tumori del cervello, proponendo un ruolo clinico più importante della MRS perché evita la necessità di un'ispezione cerebrale. Tuttavia, a parte gli alti costi, le tecniche di MRI continuano a presentare una serie di problemi che dovranno essere risolti.
Anche le onde sonore a frequenze molto più alte rispetto a quelle udibili dall'orecchio umano possono essere utilizzate in campo medico. L'ultrasonografia abbinata alle tecniche d'ecorivelazione si è rivelata molto preziosa. La strumentazione utilizzata è l'ecografia Doppler basata sull'effetto Doppler, e va sempre più raffinandosi. La più comune applicazione dell'eco-Doppler è il doppio analizzatore, mediante il quale sono acquisite in tempo reale due immagini bidimensionali, utilizzate per una visione tridimensionale che permette anche di fornire immagini fotografiche o film. Questo tipo di ecografia permette di valutare lo stato di salute del feto e di seguire, durante tutta la gravidanza, non solamente la sua anatomia, ma anche i suoi comportamenti e i movimenti. L'ecografia tridimensionale ha rivelato che il neonato sorride già nel pancione della mamma.
L'eco-Doppler è sempre più utilizzato anche in arteriografia, per valutare i pazienti con sospette lesioni dell'arteria carotide interna a livello cervicale. Altri usi sono lo studio del flusso sanguigno e la rilevazione dei movimenti del cuore fetale. Può inoltre essere impiegato per controllare il profilo della velocità del sangue attraverso i vasi sanguigni e per rilevare l'andamento di un vaso all'interno dell'addome. Un altro importante campo d'applicazione è quello della cardiologia vascolare.
A queste tecniche si è di recente aggiunta la radiazione di sincrotone, che offre possibilità uniche per applicazioni di diagnostica per immagini e garantisce un reale approccio terapeutico. È una tecnica ad ampio spettro, in quanto consente di adottare tecnologie innovative per numerose applicazioni in campo biomedico. In particolare, sono stati ottenuti risultati estremamente promettenti nel caso dell'angiografia a sottrazione digitale, della mammografia, della radioterapia e della diagnosi precoce di distribuzioni anomale del calcio nelle ossa. I risultati ottenuti nella mammografia hanno mostrato immagini ad alto contrasto, in grado di evidenziare noduli densi, di dimensioni molto inferiori a quelle osservate usando tecniche convenzionali. In ognuna di queste specifiche aree sono rilevanti le attività attinenti all'elaborazione o display delle immagini, indipendentemente dallo specifico contesto applicativo. Vi confluiscono apporti da vari settori: fisica, ingegneria, medicina, informatica, chimica, biologia, ed è difficile enucleare uno specifico contributo disciplinare. Si riscontra una compenetrazione di ruoli che, molto spesso, è il miglior indice del successo dell'integrazione interdisciplinare e, allo stesso tempo, fondamentale requisito dell'avanzamento e sviluppo di quest'area.
Ricerca nella lotta ai tumori
Nell'ultimo decennio si sono avuti notevoli progressi non soltanto per ciò che riguarda la diagnostica, ma anche per la ricerca nella lotta ai tumori. Già nel 1903 Albert Jesoniek e Hermann von Tappeiner fecero un tentativo di trattamento antitumorale, marcando colture cellulari con agenti sensibili alla luce visibile e poi irradiandole con quest'ultima. I risultati furono soddisfacenti, ma i tempi non erano, per così dire, maturi, sicché queste ricerche non ebbero seguito per decenni. Queste tecniche furono riprese solamente negli anni Settanta, e fino agli anni Novanta ci fu una vera e propria esplosione d'interesse per le terapie basate sulla fotoinattivazione PDT (Photo-dynamic therapy). Le terapie fotoinattivanti, tuttavia, per quanto efficaci, sono circoscritte al trattamento di tumori superficiali o alle cavità. Le sperimentazioni sono proseguite pertanto anche in altre direzioni.
Esistono tecniche che si propongono di inattivare le cellule tumorali mediante l'azione combinata di opportune sostanze sensibilizzanti e radiazioni di bassa energia, un approccio che ha avuto anche recentemente un intenso sviluppo. L'inattivazione cellulare accoppia la capacità distruttiva delle radiazioni ionizzanti, normalmente radiazioni gamma, con la selettività verso le cellule tumorali. La terapia consiste nel portare in modo selettivo sulle cellule neoplastiche i cosiddetti isotopi bersaglio e quindi nell'irraggiare la massa con radiazione gamma. Poiché l'effetto è rilevante soltanto per i siti che contengono i bersagli, cioè le cellule tumorali, si può avere in linea di principio la distruzione selettiva della massa neoplastica. Questa metodologia è molto recente e ancora in fase di sperimentazione.
È in atto negli Stati Uniti, in Russia, in Canada, in Svizzera e anche in Italia la sperimentazione dell'adroterapia, che fa uso di acceleratori di protoni e altre particelle adroniche, ossia particelle pesanti come neutroni, protoni e nuclei, prodotte da macchine acceleratrici come il sincrotrone. Il vantaggio principale di questo particolare tipo di radioterapia è che essa, oltre a consentire una migliore distribuzione della radiazione, dovrebbe permettere di aumentarne la dose indirizzata al tumore senza con ciò aumentare quella che colpisce i tessuti sani o gli organi critici vicini. Un secondo vantaggio dovrebbe venire dall'eliminazione, o riduzione, del fattore ossigeno, che è ancora un grave problema in radioterapia, in quanto correlato alle cellule ipossiche, quelle maggiormente radioresistenti. La situazione a livello mondiale, dal punto di vista sia della risposta terapeutica sia dell'efficacia, non è ancora chiara. I risultati finora ottenuti dimostrano che rispetto alla terapia convenzionale l'adroterapia presenta un sicuro vantaggio clinico nel caso dei tumori dell'occhio (melanomi uveali e condrosarcomi). Andrebbe poi valutato anche l'alto costo in funzione del numero di casi per i quali si prospetti un effettivo vantaggio clinico.
Una nuova e originale terapia nella cura del cancro è quella mediante cattura neutronica da parte del boro (BNCT, Boron neutron capture therapy), rivolta al cancro diffuso negli organi, una patologia priva di rimedi risolutivi. Questo studio, inaugurato nel 1987, sfrutta la grande capacità di assorbimento dell'isotopo 10 del boro da parte delle cellule tumorali. Il metodo consiste nell'irraggiare con neutroni l'organo espiantato, per esempio il fegato, dopo averne arricchito i tessuti con l'isotopo 10 del boro. Il fegato metastatico viene espiantato, posto entro un reattore nucleare e irradiato con un fascio omogeneo di neutroni, in grado di provocare la disintegrazione dei nuclei di boro e di conseguenza la completa distruzione delle cellule neoplastiche, pressoché senza danno per le cellule sane. Le dosi sono dovute al passaggio, nelle cellule, delle particelle α e dei nuclei di litio-7, prodottisi dalla disintegrazione del boro dopo che questo ha catturato i neutroni, secondo la reazione 10B(n, α)7Li. L'azione terapeutica non è dovuta alla radiazione proveniente dall'esterno sul paziente, ma alle particelle prodotte dentro la cellula tumorale: le particelle alfa e gli ioni litio si sprigionano dalla reazione fra i neutroni e il bersaglio contenente boro, che funziona come una microscopica 'mina' che esplode dentro la cellula. In un tempo compreso fra 2 e 3,5 ore dalla somministrazione della soluzione borata, sono cedute dosi letali (60÷70 Gy-Eq) nel tumore e dosi sotto il limite di tolleranza (8÷18 Gy-Eq) nel tessuto sano. I risultati sui pazienti trattati sono molto promettenti.
Bibliografia
D'Arsonval 1891: d'Arsonval, Jacques-Arsène, De l'injection des extraits liquides provenant des différents tissus de l'organisme, "Comptes rendus des séances de la Société de Biologie", n.s., 4, 1891, pp. 248-250.
Djourno 1949: Djourno, André, Excitation des muscles chez l'homme par des courants alternatifs sinusoïdaux de fréquence moyenne, "Comptes rendus des séances de la Société de Biologie", 1949, pp. 621-622.
Goggia 1912: Goggia, Carlo Paolo, Fisica medica, Milano, Hoepli, 1912.
Mosinger, De Bisschop 1960: Mosinger, Michel - de Bisschop, Guy, Étude expérimentale de la stimulation neuro-musculaire par les courants de moyenne fréquence, "Journal de physiologie", 41, 1960, pp. 211-212.
Pinelli 2001: Pinelli, Tazio e altri, Operative modalities and effects of BNCT on liver metastases of colon adenocarcinoma. A microscopical and ultrastructural study in the rat, in: Frontiers in neutron capture therapy, edited by M. Frederick Hawthorne e altri, New York-London, Kluwer Academic/Plenum, 2001.
Prévost, Battelli 1899: Prévost, Jean-Louis - Battelli, Federico, La mort par les décharges électriques, "Journal de physiologie et de pathologie générale", 1, 1899, p. 1085.
Prévost, Battelli 1900: Prévost, Jean-Louis - Battelli, Federico, Sur quelques effets des décharges électriques sur le coeur des mammifères, "Journal de physiologie et de pathologie générale", 2, 1900, p. 351.
Salmons, Vrbova 1969: Salmons, Stanley - Vrbova, Greta, The influence of activity on some contractile characteristics of mammalian fast and slow muscles, "Journal of physiology", 201, 1969, pp. 535-549.
Uzgiris, Kornberg 1983: Uzgiris, Egidijus E. - Kornberg, Roger D., Two-dimensional crystallization technique for imaging macromulecules, with an application to antigen-antibody-complement complexes, "Nature", 301, 1983, pp. 125-129.
Von Tappeiner, Jesoniek 1903: von Tappeiner, Hermann - Jesoniek, Albert, Therapeutische Versuche mit fluoreszierenden Stoffen, ‟Muenchner medizinische Wochenschrift", 1, 1903, pp. 2042-2044.
Wightman 1971: Wightman, William P.D., The emergence of scientific medicine, Edinburgh, Oliver and Boyd, 1971.