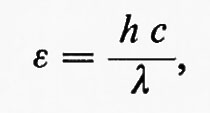Fotosintesi
Fotosintesi
di James A. Bassham
Fotosintesi
Sommario: 1. Introduzione. 2. Produttività del mare e della terraferma. 3. La reazione fotosintetica. 4. Velocità della fotosintesi. 5. Efficienza della fotosintesi. 6. Evoluzione delle cellule fotosintetiche. 7. Lo studio della fotosintesi. 8. Vie di fissazione del carbonio nella fotosintesi: a) metodi di studio; b) primi prodotti; c) la reazione di carbossilazione. 9. Il ciclo riduttivo dei pentosofosfati. 10. Biosintesi e regolazione metabolica. 11. Fotorespirazione. 12. Via degli acidi piruvico e malico. 13. Struttura dei cloroplasti. 14. Conversione primaria dell'energia fotochimica. 15. Via di trasporto dei fotoelettroni. 16. Prove dell'esistenza di due distinte reazioni fotochimiche. 17. Fotofosforilazione. 18. Future ricerche sulla fotosintesi. □ Bibliografia.
1. Introduzione
La fotosintesi consiste nell'ottenere delle sostanze complesse a partire da sostanze semplici, sfruttando l'energia luminosa. La fotosintesi biologica avviene in tutte le piante verdi e in alcuni batteri fotosintetici. Durante la fotosintesi nelle piante verdi, la luce assorbita dai pigmenti, tra cui la clorofilla, fornisce l'energia per trasformare acqua, diossido di carbonio (anidride carbonica) e sali minerali in ossigeno molecolare e composti organici che costituiscono cibi e fibre. Anche i batteri fotosintetici trasformano il diossido di carbonio e i minerali in composti organici, ma assorbono la luce per mezzo di batterioclorofilla e altri pigmenti; inoltre non formano ossigeno molecolare.
La fotosintesi nelle piante verdi fornisce tutto il cibo e l'ossigeno necessari per le forme di vita superiori. Queste ultime richiedono un costante apporto di energia per riprodursi, crescere e compiere le altre funzioni vitali. Questa energia deriva dalla combustione biologica, detta respirazione, dei cibi da parte dell'ossigeno nelle cellule aerobie (che richiedono ossigeno). A parte l'energia, le cellule devono usare il cibo come materiale di partenza per la costruzione di nuovo materiale cellulare. Anche quei batteri e lieviti che vivono con la fermentazione in assenza di ossigeno (organismi anaerobi) devono disporre di cibo come sorgente di energia e di materiali per la crescita. Se la fotosintesi delle piante verdi si fermasse, tutta la vita scomparirebbe in pochi anni dalla Terra, fatta eccezione per alcuni batteri anaerobi.
La fotosintesi delle piante verdi dà origine alla maggior parte dell'ossigeno nella nostra atmosfera e dei combustibili fossili nella Terra. Le riserve di carbone, petrolio e idrocarburi gassosi si sono formate nel fondo degli oceani, dei laghi, delle paludi nelle ere passate, quando le piante producevano molto più materiale organico di quanto gli organismi non fotosintetici potessero consumare. Questa maggiore produzione potrebbe essere stata causata da una maggiore concentrazione di CO2 rispetto a quella attuale (300 parti per milione) e dal clima più caldo risultante da tale maggiore concentrazione di CO2.
Attualmente la combustione di questi combustibili fossili fornisce la maggior parte dell'energia usata nella maggioranza dei paesi a tecnologia avanzata. Con la velocità di consumo prevista, questa fonte di energia, conservatasi attraverso le ere, sarà quasi esaurita in poche decine d'anni (v. energia: Fonti primarie di energia). Quindi se il genere umano vuole evitare un futuro di scarsa disponibilità energetica, deve sostituire entro circa trent'anni i combustibili fossili, che sono attualmente al primo posto come importanza, con altre fonti di energia, come l'energia atomica e, opportunamente trasformata, l'energia irradiata dal Sole.
Poiché sia l'ossigeno nell'atmosfera sia i combustibili fossili nelle viscere della Terra sono prodotti della fotosintesi del passato (e quindi sono stati prodotti in quantità equivalenti), si pone il problema di prevedere se la completa combustione dei combustibili fossili sulla Terra possa produrre una grave diminuzione di ossigeno nell'atmosfera. E difficile fare una stima accurata della quantità di combustibili fossili che l'uomo riuscirà a trovare nella crosta terrestre, ma le indicazioni attuali fanno prevedere che la scorta di ossigeno nell'atmosfera è di gran lunga maggiore della quantità di combustibili fossili che si prevede di scoprire ed estrarre. Ciò è dovuto in parte alla trasformazione dei combustibili fossili organici in composti inorganici ridotti del carbonio, come il carburo di ferro, nelle rocce in cui i depositi di carburante sono sepolti a grande profondità all'interno della Terra e dove essi sono sottoposti a temperature e pressioni elevate. Sembra quindi che una diminuzione di ossigeno nell'atmosfera sia un pericolo meno imminente di altri cambiamenti dell'ambiente che minacciano l'esistenza dell'uomo.
Un altro problema per il futuro è la possibilità di produrre cibo sintetico per integrare il cibo prodotto dalle piante verdi. Diversi metodi di biosintesi sono attualmente allo studio: uno di questi consiste nel far crescere Batteri a spese di combustibili fossili addizionati di sali minerali. Un altro metodo consiste nella trasformazione di fibre vegetali, particolarmente la cellulosa, da parte di Batteri, utilizzando industrialmente lo stesso principio impiegato dai Batteri presenti nello stomaco dei Ruminanti, come i Bovini. Entrambi i metodi sfruttano prodotti della fotosintesi, recenti o remoti.
In un futuro più lontano l'uomo potrà effettuare la sintesi completa di cibi a partire da materiali inorganici, come acqua e sali minerali; ciò sarà possibile solo se il costo dell'energia sarà molto diminuito, il che potrà verificarsi con qualche innovazione nella sua produzione, ad esempio sfruttando la fusione nucleare. In quel caso l'acqua potrebbe essere scissa mediante elettrolisi in idrogeno e ossigeno; quindi l'idrogeno potrebbe combinarsi chimicamente con il CO2, con i nitrati e i solfati formando molecole organiche semplici, ammoniaca e solfuro di idrogeno (acido solfidrico). Di questi composti ridotti si potrebbero nutrire Batteri e lieviti, che a loro volta potrebbero essere usati come cibo. In alternativa questi composti potrebbero servire da materiale di partenza per le biosintesi sotto l'azione di catalizzatori biologici (enzimi) stabilizzati.
Tali prospettive non allevieranno il pressante bisogno di maggiori quantità di cibo per i decenni a venire, in cui la popolazione continuerà ad aumentare rapidamente mentre molte zone del mondo mancheranno dell'infrastruttura industriale necessaria a tecnologie così avanzate. Per questo, ogni sforzo deve essere compiuto in questo periodo per incrementare la fotosintesi sulla Terra e l'efficienza con cui i suoi prodotti sono trasformati in cibo.
2. Produttività del mare e della terraferma
Benché una volta si pensasse che il mare, in virtù della sua maggiore estensione, fosse il sito di maggiore fotosintesi rispetto alla terraferma, ora si sa che non è così. Misurazioni recenti, riportate in una rassegna di J.R. Ryther (v., 1969), indicano che avviene un maggior numero di processi fotosintetici sulle terre emerse che nel mare. La ragione di ciò è che vaste aree degli oceani hanno una scarsissima fotosintesi a causa della carenza di alcuni minerali, particolarmente i fosfati, negli strati superficiali dove arriva abbastanza luce per la fotosintesi. In termini di produzione di cibo, questa mancanza di fotosintesi in vaste zone dell'oceano è ancora più grave. I Pesci, utilizzati come cibo dall'uomo, rappresentano una delle ultime tappe nella lunga catena della concentrazione del cibo. Quando i componenti del fitoplancton primario sono troppo diluiti, non possono servire da nutrimento per organismi di dimensioni tali da poter essere sfruttati dall'uomo. Perciò la maggior parte della pesca commerciale, nel mondo, ha luogo in meno del 10% dell'area totale degli oceani. Di questa superficie i tre quarti sono rappresentati dalle piattaforme continentali, l'altro quarto da aree di particolare arricchimento e risalita. Quasi metà dei pesci pescati in tutto il mondo provengono da speciali aree di intensa risalita che rappresentano solo lo 0,1% della superficie degli oceani.
Quindi sembrerebbe che aumenti realmente significativi nella produttività dei mari si possano ottenere solo arricchendo di elementi nutritivi gli strati d'acqua superficiali per aumentare la fotosintesi. Ciò avviene naturalmente nelle piattaforme continentali per efflusso di elementi nutritivi dalla terraferma portati dai fiumi e dalle correnti. In linea di principio si potrebbe trovare qualche mezzo artificiale per indurre una risalita degli strati d'acqua profondi, ricchi di sali, ma attualmente non è dato di sapere se ciò sia realizzabile da un punto di vista economico e desiderabile da un punto di vista ecologico. Una possibilità di tal genere sarebbe di scaricare calore, prodotto da potenti impianti costieri, negli strati profondi dei mari, causando di conseguenza una risalita dovuta a correnti convettive.
3. La reazione fotosintetica
La fotosintesi nelle piante verdi produce molte sostanze oltre ai carboidrati. Tuttavia gli zuccheri e altri carboidrati sono i prodotti predominanti della fotosintesi in molte piante adulte. La formazione di un carboidrato semplice, come il glucosio, può essere indicata dalla reazione chimica:
6 CO2+6 H2O+luce→C6H12O6+6 O2.
In realtà nelle foglie delle piante viene prodotto ben poco glucosio libero; invece queste unità monosaccaridiche sono unite insieme per formare l'amido o la cellulosa, o sono coniugate con un altro monosaccaride, il fruttosio, per formare il saccarosio, che è il comune zucchero.
I carboidrati, gli amminoacidi, gli acidi grassi, i lipidi, i pigmenti e numerosi altri componenti del tessuto vegetale sono sintetizzati durante la fotosintesi. Oltre agli elementi carbonio, idrogeno e ossigeno, alcune di queste sostanze contengono azoto, fosforo e zolfo; questi ultimi elementi provengono da minerali inorganici assorbiti dalle piante verdi: essenzialmente nitrati (NO-3), solfati (SO²4-) e fosfati (HPO²4-).
Una equazione generale che esprime tutto il processo della fotosintesi deve includere queste sostanze e può essere così formulata:
a CO2+b H2O+c NO-3+d SO²4-+e HPO²4-+luce→
O2+composti organici (carboidrati, grassi, proteine,
pigmenti e altri componenti dei tessuti vegetali).
La varietà e la quantità dei prodotti organici sintetizzati varia a seconda della specie vegetale e del suo stato fisiologico.
Il risultato generale della fotosintesi è la rottura del legame tra l'ossigeno ed elementi come il carbonio, l'idrogeno, l'azoto e lo zolfo. Gli atomi di ossigeno così ottenuti si uniscono fra loro a due a due, dando origine a ossigeno molecolare, mentre nuovi legami si formano tra gli atomi di carbonio e gli altri elementi per formare molecole organiche.
È richiesta più energia per rompere i legami tra l'ossigeno e gli altri elementi di quanta se ne forma quando si costituiscono nuovi legami; ulteriore energia è richiesta per unire gli atomi in catene più lunghe, per formare cioè molecole più grandi. Tutta questa energia accumulata nella costituzione di nuovi legami nelle molecole proviene dalla conversione dell'energia luminosa assorbita dai pigmenti delle piante.
4. Velocità della fotosintesi
La velocità della reazione fotosintetica è misurata spesso dalla quantità di ossigeno prodotto per unità di superficie di tessuto vegetale o per unità di peso della clorofilla totale. Alcune piante attive e vitali, come gli spinaci, producono, quando crescono in presenza di aria (CO2 presente 0,03%) a 25 °C, fino a 7,4 litri di ossigeno ogni ora per grammo di clorofilla. In queste piante vi è un grammo di clorofilla per kg di tessuto umido. Alcune alghe unicellulari, come la Chlorella pyrenoidosa, contengono circa 4 grammi di clorofilla per kg di tessuto umido e sono capaci di produrre, con sufficiente aerazione e buona illuminazione, fino a 30 litri di ossigeno per ora per kg. Questa produzione può essere aumentata di parecchie volte aumentando la concentrazione di CO2 fino all'1%. In alcune varietà termofile si sono ottenute velocità ancora maggiori elevando la temperatura a 35 °C o più.
Questa elevata produttività della Chlorella pyrenoidosa ha indotto a considerare la possibilità di un suo impiego come economica sorgente di cibo o come sistema per produrre scambi gassosi nelle navicelle spaziali. Sfortunata- mente, per quanto riguarda l'ingegneria spaziale, la Chlorella deve essere sospesa in un liquido di volume molte volte superiore al proprio o disposta in sottile pellicola perché sia efficientemente illuminata e aerata. Questa necessità ha pure limitato, finora, l'impiego di colture di alghe come sorgenti di cibo a buon mercato.
La velocità di fotosintesi è direttamente influenzata dall'intensità dell'illuminazione, dalla concentrazione di diossido di carbonio e dalla temperatura. Anche l'acqua e i sali minerali sono di importanza vitale per le piante verdi. Nelle cellule vegetali la velocità di fotosintesi dipende dalla specie e dallo stato fisiologico (salute, stato di sviluppo, fioritura, ecc.).
Il meccanismo della fotosintesi comprende un passaggio fotochimico e uno enzimatico, che possono essere distinti con studi cinetici sulla dipendenza della velocità di fotosintesi dall'intensità d'illuminazione e dalla temperatura. A intensità luminosa bassa o media la velocità di fotosintesi è determinata dalla velocità di passaggi fotochimici come l'assorbimento della luce, il trasferimento di energia tra i pigmenti e la conversione dell'energia di eccitamento in potenziale chimico. La velocità di questi passaggi dipende dall'intensità luminosa ma è quasi indipendente dalla temperatura. Ad alte intensità luminose la velocità di fotosintesi non aumenta più all'aumentare dell'intensità della luce: la fotosintesi è al punto di ‛saturazione luminosa'. Ora la velocità dipende da alcune reazioni chimiche limitanti, mediate da enzimi, ed essa, nell'ambito della stabilità termica di questi ultimi, aumenta in funzione della temperatura.
Uno dei più importanti passaggi limitanti in presenza di alte energie luminose è la reazione chimica con cui all'inizio il diossido di carbonio viene incorporato in molecole organiche. Infatti la velocità di questa reazione di carbossilazione aumenta di poco all'aumentare della concentrazione di CO2: un aumento della pressione parziale di CO2 di 100 volte, dallo 0,03% al 30%, comporta un aumento di solo 3 volte nella velocità di reazione in alcune piante molto attive come la Chlorella pyrenoidosa. Questo limitato aumento è probabilmente il riflesso di meccanismi regolatori estremamente efficaci, che mantengono il metabolismo delle piante in equilibrio malgrado il cambiare di fattori ambientali.
Ogni specie vegetale si è sviluppata in modo da adattarsi a specifiche condizioni ambientali; date queste condizioni, i complessi meccanismi di regolazione dell'apparato fotosintetico regolano automaticamente le attività enzimatiche dei passaggi limitanti allo scopo di mantenere un metabolismo equilibrato. Quando alcuni fattori ambientali, come l'intensità luminosa o la temperatura, travalicano i limiti abituali per la pianta, i meccanismi regolatori possono venir meno, producendo una diminuzione di velocità della fotosintesi e perfino la morte della pianta.
5. Efficienza della fotosintesi.
Il rapporto tra energia accumulata nelle reazioni chimiche della fotosintesi ed energia luminosa assorbita è chiamato ‛efficienza energetica'. È difficile calcolare accuratamente la quantità di energia chimica accumulata, in quanto nel corso della fotosintesi si formano molti prodotti diversi. Si può ammettere che l'equazione riportata in precedenza, esprimente la formazione del glucosio, rappresenti approssimativamente il processo reale: per ciascuna mole di ossigeno sviluppata (6•123 molecole, ovvero 32 grammi) e per 1/6 di mole di glucosio formato (30 grammi), vengono accumulate circa 117 kcal di energia libera chimica.
L'energia ε di un fotone di luce è inversamente proporzionale alla sua lunghezza d'onda:
in cui h è la costante di Planck, c è la velocità della luce nel vuoto e λ è la lunghezza d'onda della luce; le unità di misura sono erg, secondi e centimetri. Quando l'energia di un fotone è moltiplicata per 6•1023, per calcolare l'energia di una mole di fotoni (detta 1 einstein), si ottiene l'espressione E=28,4/λ, in cui E è espressa in kcal e λ è data in micrometri (1 μm=un milionesimo di metro). La luce rossa con λ eguale a 0,68 μm ha E=42 kcal.
La luce blu ha una lunghezza d'onda minore e quindi una maggiore energia (λ=0,46 μm, E=62 kcal). Tuttavia per sviluppare una mole di ossigeno è necessario lo stesso numero di einstein di luce blu o di luce rossa. Questo rapporto tra einstein di luce richiesta per mole di ossigeno sviluppato si chiama rendimento quantico ed è approssimativamente lo stesso per tutta l'energia luminosa assorbita nell'ambito di lunghezze d'onda tra 0,40 e 0,68 μm. L'energia luminosa eccedente a lunghezze d'onda minori è ceduta sotto forma di calore durante la conversione dell'energia luminosa in energia chimica. In tal modo le piante sono capaci di convertire energia per mezzo di un singolo meccanismo che può utilizzare luce rossa fino a 0,68 μm.
Si è di recente stabilito che il rendimento quantico della fotosintesi è di circa 9 einstein di luce assorbita per mole di ossigeno sviluppata. Quindi l'efficienza o resa energetica per la produzione del glucosio, quando sia adoperata solo luce rossa, può essere calcolata in 117/(9•42)=0,31. Considerando la complessità del meccanismo di fotosintesi, che comprende molte reazioni, si può considerare notevolmente alta questa efficienza, che però viene raggiunta dalle piante solo nelle condizioni ottimali realizzabili in laboratorio.
La massima efficienza dei vari passaggi della fotosintesi ottenibile con luce solare può essere calcolata dal secondo principio della termodinamica: l'energia trasferita da un corpo a temperatura T1 a un altro corpo a temperatura T2 può essere convertita in un'altra forma di energia diversa dal calore, cioè in lavoro o energia chimica, con un'efficienza non superiore a 1−T2/T1. Un corpo nero che emette abbastanza luce rossa da saturare la fotosintesi deve avere una temperatura intorno ai 1.200 °K, mentre tipicamente la fotosintesi avviene a circa 300 °K (27 °C). Quindi la massima efficienza termodinamica dei processi fotosintetici potrebbe essere 1−300/1.200=0,75=75%.
Perché le piante vivano deve esserci una rapida conversione di energia e materiali inorganici in prodotti ridotti della fotosintesi e ossigeno. Quindi tutti i passaggi delle complesse reazioni biochimiche devono operare con efficienze minori di quella massima prevista dalla termodinamica. Una certa parte delle reazioni mediate da enzimi, che avvengono al buio, comporta una perdita di energia come calore. In alcuni casi questo dispendio energetico viene usato a scopo di regolazione. I passaggi in cui vi è una dissipazione di energia sotto forma di calore limitano la velocità; l'attività degli enzimi che catalizzano questi passaggi è strettamente controllata, nelle piante, per ottenere un equilibrato flusso di sostanze lungo le varie vie metaboliche, come richiesto per la sopravvivenza e la crescita della pianta.
Le reazioni chimiche all'interno e sulla superficie delle membrane pigmentate ossidano l'acqua liberando ossigeno molecolare e trasferendo idrogeno (sotto forma di elettroni e protoni) attraverso la membrana fino ai trasportatori di elettroni. Infine i trasportatori solubili si caricano di elettroni (cioè vengono ridotti sulle superfici delle membrane) e insieme a molecole di ATP possono essere usati nella fase solubile dei cloroplasti (lo stroma) per la riduzione e la trasformazione del diossido di carbonio, dei nitrati e dei solfati in prodotti organici. L'efficienza complessiva delle reazioni che avvengono sulle membrane è di circa il 40%, mentre quella delle reazioni che avvengono nella fase solubile è di circa l'8o%.
Mentre queste sono le efficienze ottimali del processo fotosintetico in sé, l'effettiva resa energetica della pianta nel suo insieme è generalmente molto minore per una serie di ragioni. Le piante che crescono sulla terraferma perdono grosse quantità di energia per il processo di traspirazione, per cui le foglie sono raffreddate dall'evaporazione di acqua dalla loro superficie. La produzione di tessuti non fotosintetici come radici, steli, semi, frutti, e altre funzioni fisiologiche, come la respirazione, contribuiscono a diminuire la resa energetica complessiva delle piante.
Quando vengono considerati come soli prodotti terminali del processo di conversione energetica i raccolti agricoli (semi e frutti), l'efficienza è molto minore (spesso circa 1-2%). Quindi è possibile che all'aumentare della richiesta di cibo, in un mondo più popolato, si trovino metodi economici per ottenere proteine più direttamente dai tessuti verdi fotosintetici (v. Pirie, 1966). In alcuni casi il raccogliere solo tessuti particolari, come i semi e i frutti, o la trasformazione delle foglie verdi in cibo da parte degli erbivori può costituire un grosso spreco.
6. Evoluzione delle cellule fotosintetiche.
Mentre ora la maggior parte della vita dipende dalla fotosintesi, le piante verdi non sono stati i primi organismi a evolversi sulla Terra. Un'ipotesi largamente sostenuta riguardante l'atmosfera della Terra primitiva afferma che essa non solo era priva di ossigeno, ma conteneva idrogeno combinato con l'azoto (ammoniaca) e con il carbonio (metano); inoltre poteva contenere anche altri composti dell'idrogeno, del carbonio e dell'azoto. Sotto l'azione dell'irradiazione ultravioletta solare e di altre sorgenti di energia come l'attività vulcanica e le scariche dei fulmini, si sarebbero formate, nell'atmosfera e nei mari primitivi, molecole più complesse: tali composti si sarebbero accumulati nei mari primitivi e da essi si sarebbero sviluppate le prime cellule viventi (v. biofisica).
Tra le molecole organiche presenti in questi mari primordiali vi sarebbero state anche sostanze colorate o pigmenti: esperimenti di laboratorio hanno dimostrato che simili composti si possono formare irradiando molecole più semplici. Quindi quei pigmenti biologici essenziali, noti come porfirine, avrebbero potuto formarsi fotochimicamente da composti relativamente semplici come la glicina (un amminoacido) e l'acetato (un acido grasso a due atomi di carbonio). Da queste porfirine, in seguito, le cellule viventi avrebbero potuto sviluppare la clorofilla delle piante verdi, la batterioclorofilla dei batteri fotosintetici, l'emoglobina (il pigmento rosso del sangue) e i citocromi, che sono indispensabili sia per la respirazione sia per la fotosintesi e si trovano in tutti gli organismi aerobi, animali e vegetali.
L'energia è essenziale per la vita; quindi le cellule primitive devono aver sviluppato meccanismi per sfruttare l'energia luminosa captata dai propri pigmenti. Per qualche tempo l'energia potrebbe essere stata usata solo per catalizzare reazioni chimiche necessarie, senza essere accumulata; dopo l'evoluzione di una biochimica sempre più complessa, maggiori quantità di energia assorbita vennero convertite in potenziale chimico da usarsi nei processi vitali.
Si può considerare che due tipi di conversione di energia sono stati conservati fino a oggi nella fotosintesi delle piante: nella prima di queste due reazioni l'energia luminosa è usata per convertire due acidi nella corrispondente anidride con eliminazione di una molecola d'acqua. Benché la maggior parte di queste anidridi siano instabili nell'ambiente acquoso presente all'interno delle cellule viventi e quindi possano reagire con l'acqua liberando l'energia in esse contenuta, l'anidride acida di importanza biologica, nota come adenosintrifosfato (ATP), è stabile ed è essenziale come trasportatrice di energia chimica in tutte le cellule viventi (v. fosforilazione ossidativa).
Il secondo importante tipo di accumulo dell'energia fotochimica, che deve essersi sviluppato al tempo degli organismi primitivi, è il movimento di elettroni da un composto a un altro, con ossidazione di un composto, che perde elettroni, e la riduzione di un altro composto, che ne acquista. La prima di queste ossidoriduzioni fotochimiche potrebbe avere comportato l'accumulo di una piccola parte solamente dell'energia luminosa. Per esempio, elettroni potrebbero essere stati trasferiti da composti ridotti dello zolfo (solfidrilici) al ferro ossidato (Fe3+). In effetti le reazioni di ossidoriduzione che comportano il trasferimento di elettroni tra ferro e zolfo legati in strutture proteiche sono di grande importanza in tutti gli organismi viventi oggi.
Il primo organismo capace di accumulare l'energia luminosa come ATP e in reazioni ossidoriduttive potrebbe essere stato l'antenato comune dei batteri fotosintetici e delle piante verdi. Sappiamo che vi sono molte somiglianze tra questi due tipi di organismi fotosintetici, benché i batteri abbiano come pigmento una clorofilla modificata (batterioclorofilla) e siano incapaci di produrre O2. I batteri fotosintetici non formano O2, in quanto non sottraggono elettroni dall'acqua, cioè non la ossidano: invece essi ossidano diverse sostanze organiche e inorganiche (come il solfuro d'idrogeno).
L'ossidazione dell'acqua, con trasferimento degli elettroni ad altre sostanze e liberazione di O2, ossigeno molecolare, costituisce un compito arduo, che solo le cellule delle piante sono capaci di eseguire. I primi organismi che svilupparono questa capacità erano probabilmente molto simili alle attuali alghe unicellulari azzurre. Questi organismi, a somiglianza sia dei batteri fotosintetici sia di quelli non fotosintetici, si trovano in forma di cellule singole procariotiche; tali cellule non hanno nucleo o altri organelli subcellulari specializzati: il loro materiale genetico è diffuso in tutta la cellula; in questo esse differiscono dalle cellule eucariotiche, che hanno il materiale genetico nel nucleo. In pratica tutti gli organismi viventi, animali e vegetali, ad eccezione dei batteri e delle alghe azzurre, sono costituiti da cellule eucariotiche.
La comparsa sulla Terra, circa 3,5 eoni fa (1 eone=1 miliardo di anni), di queste alghe azzurre alterò profondamente l'atmosfera e la biosfera. L'accumularsi dell'ossigeno rese possibile lo svilupparsi d'organismi aerobici, che poterono utilizzare l'energia liberata dalla combustione di composti organici da parte dell'ossigeno. L'energia così liberata è di gran lunga maggiore di quella ottenuta da composti organici per mezzo della fermentazione anaerobica.
In seguito alcune cellule eucariotiche svilupparono la capacità di effettuare una completa fotosintesi, compresa la produzione di ossigeno; tali cellule di vegetali verdi contengono non solo il nucleo, ma anche organelli subcellulari, tra cui i cloroplasti, che sono responsabili dell'intero processo di fotosintesi. Una teoria sullo sviluppo di queste cellule sostiene che cellule non fotosintetiche, ameboidi, abbiano inglobato alghe azzurre; quindi per mezzo di adeguate mutazioni si sarebbe sviluppata una condizione di simbiosi, cosicché le piccole cellule inglobate sarebbero diventate doroplasti. Secondo questa teoria, la cellula ospite avrebbe prima inglobato batteri aerobi, che sarebbero poi divenuti quelli che oggi noi chiamiamo mitocondri. Al giorno d'oggi tutte le cellule vegetali della Terra, dalle alghe unicellulari alle piante superiori, sono cellule eucariotiche contenenti nucleo, mitocondri e cloroplasti. I cloroplasti di queste cellule effettuano la fotosintesi sotto l'azione della luce, sintetizzando ATP e trasferendo elettroni dall'acqua per ridurre il diossido di carbonio, i nitrati e i solfati. Al buio i mitocondri formano ATP usando l'energia liberata dalla combustione dei prodotti organici della fotosintesi da parte dell'ossigeno.
7. Lo studio della fotosintesi.
Le storiche scoperte sulla natura della fotosintesi risalgono alla fine del XVIII secolo, all'epoca dell'inizio della chimica moderna (per una rassegna, v. Rabinowitch, 1945). Nel 1772 J. Priestley comunicò di aver effettuato un esperimento mettendo un rametto di menta in un recipiente chiuso in cui era stata fatta bruciare una candela. Dopo 10 giorni in presenza della menta, l'aria all'interno del recipiente permetteva di nuovo la combustione di una candela e poteva essere respirata da un topo senza provocarne la morte. J. Ingenhousz nel 1780 scoprì che per questo fenomeno era necessaria la luce; A.-L. Lavoisier identificò il gas in questione con l'ossigeno. J. Senebier dimostrò che l'ossigeno si formava a spese di un altro gas, identificato da Lavoisier nel 1781 con il diossido di carbonio. Nel 1808 N. de Saussure scoprì che l'aumento in peso di una pianta cresciuta in un recipiente accuratamente pesato era dato dalla somma del peso del carbonio, derivante interamente dal diossido di carbonio assorbito, e di quello dell'acqua assorbita dalle radici della pianta. Quasi cinquant'anni più tardi il concetto di energia chimica era abbastanza ben sviluppato da permettere a R. Mayer, nel 1845, di scoprire che l'energia della luce solare assorbita era accumulata come potenziale chimico nei prodotti della fotosintesi.
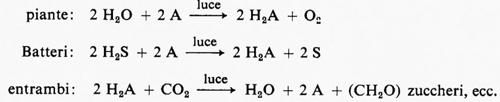
Tra i prodotti della fotosintesi l'amido e altri carboidrati sono preminenti: anche il nome, carboidrati, indica l'addizione di acqua al carbonio per dare quella proporzione degli elementi, CH2O, presente in questi composti. Quindi non costituisce sorpresa che secondo una teoria sulla fotosintesi, largamente diffusa, era il diossido di carbonio (CO2) che, decomponendosi, dava luogo al carbonio e all'ossigeno molecolare (O2), dopo di che il carbonio poteva essere ‛idratato' dall'acqua per dare i carboidrati con struttura molecolare (CH2O)n. Mentre venivano avanzate altre ipotesi, questa teoria prevalse fino a quando, nel 1931, C. B. Van Niel riconobbe che la fissazione del CO2 e la sua incorporazione in composti organici è essenzialmente la stessa nelle piante verdi e in alcuni solfobatteri fotosintetici. Le differenze tra questi organismi possono essere trovate a livello della fonte di elettroni, acqua o solfuro d'idrogeno, e nella natura dei passaggi fotochimici, che comportano differenti tipi di pigmenti. Secondo Van Niel durante la fase fotochimica vi era un trasferimento di idrogeno da H2S o H2O a un accettore A che diveniva H2A; quest'ultimo poteva reagire con il diossido di carbonio per dare il carboidrato (CH2O) e di nuovo A, con un meccanismo comune alle piante verdi e ai Batteri:
La decomposizione fotochimica dell'acqua con formazione di ossigeno fu distinta dalla riduzione del diossido di carbonio da R. Hill e R. Scarisbrick (v., 1940), i quali dimostrarono che le particelle verdi contenute nelle foglie potevano produrre ossigeno se illuminate e fornite di un opportuno accettore di elettroni (ossalato ferrico) in sostituzione dell'accettore naturale di elettroni, indicato con A da Van Niel. Lo studio di questa reazione parziale della fotosintesi, detta reazione di Hill,è stato di grande importanza nella elucidazione del meccanismo della fotosintesi.
Fin dal 1940 sono stati usati isotopi degli elementi come traccianti delle reazioni fotosintetiche. L'isotopo stabile 180 6 stato usato per ottenere maggiori informazioni sulla provenienza dell'ossigeno nella fotosintesi (v. Ruben e altri, 1940): le piante che effettuano la fotosintesi in presenza di H218O producono 18O2; le piante che la effettuano in presenza di C18O2 e H216O producono 16O2, come è da prevedere se l'ossigeno prodotto deriva dall'acqua.
Con la scoperta del carbonio radioattivo (14C) è stato possibile studiare il meccanismo dell'incorporazione del diossido di carbonio e della sua riduzione nella tappa ‛al buio' della fotosintesi.
8. Vie di fissazione del carbonio nella fotosintesi.
a) Metodi di studio
Quando le piante assorbono diossido di carbonio marcato con 14C è possibile seguire l'andamento della sua fissazione seguendo il destino chimico dell'isotopo radioattivo. Poiché la fissazione del carbonio nelle piante avviene in assenza di luce, i primi studi si accentrarono sul destino del 14CO2 assorbito dalle piante al buio, subito dopo un periodo di illuminazione. Il diossido di carbonio marcato viene incorporato, al buio, in composti stabili, che sono poi trasformati in altri composti, tra cui gli zuccheri, in seguito a una nuova esposizione alla luce.
Dal 1946 in poi M. Calvin e i suoi collaboratori (v. Calvin e Benson, 1948; v. Bassham e altri, 1954; v. Calvin e Massini, 1952; v. Bassham e Calvin, 1957) usarono CO2 marcato per scoprire l'andamento della riduzione del carbonio nella fotosintesi. In tali esperimenti si induce la fotosintesi con l'illuminazione delle piante, sia foglie come quelle di soia o di orzo, sia alghe unicellulari come la Chlorella pyrenoidosa, in presenza di 14CO2 per alcuni secondi; quindi le piante sono rapidamente uccise, in genere con alcool caldo, e i composti marcati da esse ottenuti sono separati mediante cromatografia bidimensionale su carta. In questo metodo di analisi una goccia di soluzione contenente gli estratti vegetali è deposta e fatta asciugare su di un grande foglio di carta da filtro, in vicinanza di un angolo. Si piega quindi un lembo della carta vicino al margine e lo si immerge in una vaschetta contenente una speciale miscela di solventi organici e acqua. Questi solventi migrano per capillarità attraverso la carta trascinando via dall'origine i composti solubili in essi. I composti sono trasportati in misura diversa a seconda della loro solubilità. Finita la prima cromatografia, si fa evaporare il solvente dalla carta, quindi si ruota questa di 90 gradi e si immerge l'altro lembo adiacente all'origine in una vaschetta contenente un solvente diverso dal primo. Si effettua di nuovo la cromatografia, questa volta in una direzione ad angolo retto rispetto alla prima; i soluti vengono così trasportati a varia distanza lungo la carta; indi la si asciuga di nuovo; a questo punto il cromatogramma bidimensionale è pronto per l'identificazione dei composti in esame.
Poiché i composti che interessano sono quelli radioattivi, si pone una larga pellicola, simile a quelle usate in medicina per i raggi X, a contatto con la carta cromatografica, al buio, per circa 24 h. I punti radioattivi della carta, emettendo radiazioni beta per la presenza del carbonio-14, anneriscono le aree corrispondenti della pellicola, dando un'immagine esatta (autoradiografia) della loro posizione (v. figg. 1 e 2). Quando la pellicola sviluppata è giustapposta al cromatogramma, è possibile localizzare i composti radioattivi, ritagliare i pezzi di carta che li contengono e determinare la quantità di 14C in ciascuno di essi.
I composti marcati possono essere identificati con vari metodi fisici e chimici: uno dei più importanti è la identificazione co-cromatografica, che si esegue mescolando il composto radioattivo, diluito dalla carta, con una certa quantità della sostanza che si presume costituisca il composto diluito: la miscela viene ulteriormente cromatografata con la tecnica già descritta. La carta può quindi essere spruzzata con reattivi opportuni che, reagendo con la sostanza aggiunta, danno una macchia colorata, mentre non la danno con il composto marcato originariamente presente perché contenuto in quantità troppo piccola. Se la macchia colorata coincide con la zona di annerimento dell'autoradiografia, dovuta al composto radioattivo, si può identificare in prima approssimazione il composto; se non coincide, si tenta la co-cromatografia con un'altra sostanza.
b) Primi prodotti
Quando l'alga unicellulare Chlorella pyrenoidosa fotosintetizza per soli due secondi in presenza di 14CO2, quasi tutta la radioattività viene accumulata in un solo composto, l'acido 3-fosfoglicerico (3-PGA), primo prodotto stabile della fissazione del carbonio nella maggior parte delle piante. Anche dopo un periodo così breve di fotosintesi si sono già formate piccole quantità di zuccheri monofosfati e difosfati.
Il primo prodotto, il 3-PGA, si forma anche se il CO2 radioattivo viene aggiunto al buio subito dopo la fine dell'illuminazione. Dopo 10 secondi di fotosintesi in presenza di 14CO2, si trovano grosse quantità di carbonio radioattivo nei glucidi fosfati, negli amminoacidi e in altri composti
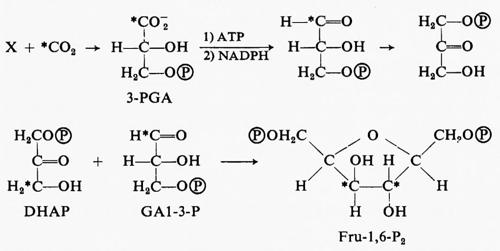
Al tempo di queste scoperte era già ben nota la via metabolica della gluconeogenesi, per mezzo della quale le cellule non fotosintetiche formano il glucosio a partire dal 3-PGA. Poiché la riduzione fotosintetica del carbonio produce glucidi fosfati e il primo composto che si forma è il 3-PGA, si suppose che il 3-PGA venisse ridotto a glucidi fosfati in modo essenzialmente simile a quanto avviene nella gluconeogenesi. Nella prima reazione, catalizzata dall'enzima fosfogliceratochinasi, il fosfato terminale di un ATP (adenosintrifosfato) viene legato al gruppo carbossilico del 3-PGA, formando l'acido 1,3-difosfoglicerico (1,3-P2-GA).
Nel secondo passaggio l'enzima triosofosfatodeidrogenasi trasferisce due elettroni dal trasportatore di essi, il nicotinammide-adenin-dinucleotide-fosfato (NADPH), al legame anidridico interposto tra fosfato e PGA, liberando acido fosforico e riducendo il gruppo carbossilico ad aldeide, trasformando perciò il composto a tre atomi di carbonio in un glucide fosfato anch'esso a tre atomi di carbonio (GAl-3-P, gliceraldeide-3-fosfato).
Alcune molecole di GAl-3-P sono isomerizzate a diidrossiaceton-fosfato (DHAP) per mezzo della triosofosfatoisomerasi, e i due triosofosfati sono condensati, per mezzo dell'enzima aldolasi, per costituire il fruttosio-1,6-difosfato. ???30??? indica un radicale fosforico, −OPO3H−;
gli asterischi indicano gli atomi di 14C:
Il radicale fosforico nella posizione 1 dell'esosio Fru-1,6-P2 viene rimosso per idrolisi e si produce così il fruttosio-6-P (Fru-6-P). Nella sintesi del glucosio per la produzione di amido, il Fru-6-P è ulteriormente convertito in glucosio-6- fosfato (Glc-6-P) per mezzo dell'esosofosfatoisomerasi (v. fig. 5).
Partendo dal fatto che il primo composto stabile è un derivato carbossilico a 3 atomi di carbonio, e dalla conoscenza generalizzata che si aveva a quel tempo delle reazioni di carbossilazione in biochimica, si formulò l'ipotesi che il 3-PGA si formasse per addizione di CO2 a un composto bicarbonioso di natura sconosciuta. Se così fosse, a brevi tempi si dovrebbe trovare marcato il carbonio del carbossile e non gli altri due. In effetti la degradazione chimica della molecola, con rottura dei legami tra gli atomi di carbonio, e l'isolamento di questi in forma stabile hanno dimostrato che la maggior parte del 14C è accumulato nel carbossile del 3-PGA formatosi durante i primi secondi di fotosintesi in presenza di 14CO2. Durante il processo riduttivo che porta alla formazione dei glucidi fosfati, questo gruppo carbossilico viene ridotto ad aldeide e la susseguente condensazione di due triosofosfati dovrebbe produrre esosi marcati negli atomi di carbonio in posizione 3 e 4; la demolizione chimica di tali esosi ha confermato questa ipotesi.
c) La reazione di carbossilazione
Tra i glucidi fosfati e difosfati che risultano marcati dopo pochi secondi di fotosintesi si trovarono non solo composti a 3 e a 6, ma anche a 5 e a 7 atomi di carbonio. Si pensò che questi ultimi potevano in qualche modo fornire il composto a due atomi di carbonio necessario per la reazione di carbossilazione. Tuttavia fu necessario un esperimento diverso per chiarire il meccanismo di questa reazione. Alghe unicellulari furono lasciate fotosintetizzare per 5-10 minuti in presenza di 14CO2: la concentrazione di diossido di carbonio e il rapporto tra atomi di carbonio marcati e non marcati erano mantenuti costanti. Alla fine di questo periodo i primi composti intermedi della fissazione del carbonio risultarono marcati con 14C derivante dal diossido di carbonio. La quantità di 14C trovato in ciascun composto divisa per il rapporto tra 14C e 12C (carbonio non marcato) indicava il numero di atomi di carbonio in quel composto, mentre l'ulteriore divisione per il numero di atomi di carbonio per molecola dava la concentrazione del composto nel tessuto. Campioni di alghe venivano prelevati a tempi determinati durante questo periodo e quindi analizzati con cr0matografia su carta e autoradiografia per determinare la concentrazione dei composti intermedi con questa tecnica di marcatura a saturazione.
Come proseguimento dello stesso esperimento, le alghe venivano bruscamente sottoposte a cambiamenti delle condizioni ambientali: più campioni di alghe erano prelevati a intervalli di pochi secondi e quindi analizzati per vedere l'effetto prodotto sulle concentrazioni dei composti intermedi.
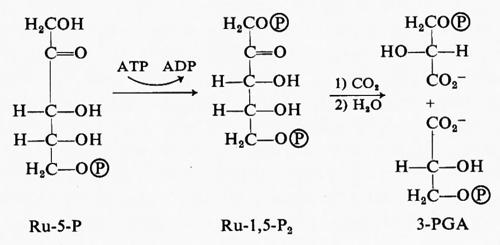
In un esperimento la luce fu spenta in modo che fosse interrotto il flusso di cofattori (elettroni e ATP) dalle reazioni fotochimiche alle reazioni metaboliche a carico del carbonio: si ottenne il blocco di quei passaggi metabolici che richiedevano tali cofattori; si accumularono i composti intermedi a monte delle reazioni bloccate, mentre diminuirono fortemente le sostanze a valle di queste reazioni. Ne risultò che in queste condizioni la concentrazione del PGA aumentava rapidamente, mentre quella di un glucide difosfato a 5 atomi di carbonio, il ribulosio-1,5-difosfato (Ru-1,5-P2), diminuiva (v. Calvin e Massini, 1952). Se ne concluse che i cofattori originati dalla luce sono necessari per la formazione del ribulosiodifosfato e per l'utilizzazione dei 3-PGA, mentre una reazione in assenza di luce forma 3-PGA a spese del ribulosiodifosfato: ciò indica che la reazione in assenza di luce consisterebbe nella carbossilazione in cui il Ru-1,5-P2 sarebbe il substrato che dà poi luogo a due molecole di PGA.
Per verificare questa ipotesi fu compiuto un altro esperimento, in cui si facevano fotosintetizzare le alghe per diversi minuti allo scopo di marcare completamente con carbonio radioattivo i primi composti intermedi: la luce era mantenuta accesa e la concentrazione di CO2 veniva notevolmente diminuita facendo fluire aria a basso contenuto di CO2 (v. Calvin e Wilson, 1955). Come previsto, il livello di Ru-1,5- P2 ne era aumentato, mentre quello di 3-PGA diminuiva (v. fig. 3). In base a questi esperimenti è stata proposta non solo la carbossilazione del Ru-1,5-P2, ma anche la sua formazione in una reazione cui partecipano ribulosio-5-fosfato e ATP:
9. Il ciclo riduttivo dei pentosofosfati.
Per stabilire le vie seguite per la sintesi di Ru-5-P a partire da triosofosfati e completare così il ciclo della riduzione del carbonio, Calvin e i suoi collaboratori studiarono la posizione del 14C nei glucidi fosfati marcati che si formavano dopo solo pochi secondi di fotosintesi in presenza di 14CO2 (v. Bassham e altri, 1954). I risultati di questi esperimenti indicarono il modo in cui molecole di triosi e di esosi venivano modificate per dar luogo a pentosi. Alcuni enzimologi interessati allo studio di un ciclo ossidativo dei pentosi, avente luogo in molti organismi fotosintetici e non fotosintetici, isolarono gli enzimi che catalizzano la maggior parte delle reazioni implicate (per una rassegna sull'argomento v. Bassham e Calvin, 1957).
Si poté quindi stabilire l'intero ciclo riduttivo del carbonio nella fotosintesi: in questo ciclo sono necessarie 5 molecole di triosofosfati per formare 3 molecole di Ru-5-P, che sono fosforilate con ATP per formare Ru-1,5-P2. La carbossilazione di queste 3 molecole di Ru-1,5-P2 dà luogo a 6 molecole di 3-PGA e la riduzione di questo richiede 6 molecole di ATP e 6 molecole di NADPH. Delle risultanti 6 molecole di triosofosfati (GAI-3-P e DHAP), 5 sono necessarie per la prosecuzione del ciclo, mentre la sesta può essere utilizzata per la sintesi di carboidrati o altri prodotti collaterali della fotosintesi.
In definitiva, per la sintesi ex novo di una molecola di triosofosfato sono necessarie 3 molecole di CO2, 9 di ATP e 6 di NADPH, ossia 3 molecole di ATP e 2 di NADPH per ogni molecola di CO2 ridotta. Considerando il meccanismo di trasporto dei fotoelettroni, che verrà esposto in seguito, è praticamente sicuro che due molecole di NADPH (4 elettroni in totale) e almeno due molecole di ATP si generano a spese di 8 fotoni di luce assorbiti dall'apparato fotochimico. Ulteriore ATP può essere generato dall'energia luminosa assorbita con il processo della fotofosforilazione ciclica, di cui si parlerà più avanti, ma la resa quantica di questo processo non è del tutto nota. Altre molecole di ATP e di NADPH sono necessarie per l'ulteriore trasformazione dei triosofosfati, formati nel principale ciclo riduttivo del carbonio, in prodotti secondari come carboidrati, grassi, proteine e pigmenti. E ancora ulteriori agenti riducenti che provengono dal sistema di trasporto dei fotoelettroni servono a ridurre i nitrati e i solfati necessari, sotto forma di azoto e zolfo ridotti, per la sintesi di amminoacidi e altre sostanze. Quindi non desta meraviglia il fatto che la Chlorella pyrenoidosa, crescendo in condizioni ottimali, assorba 9-10 fotoni per ogni molecola di CO2 ridotta (v. Ng e Bassham, 1968).
10. Biosintesi e regolazione metabolica
Una volta si pensava che la fotosintesi producesse direttamente solo carboidrati; ora si sa che i composti intermedi del principale ciclo riduttivo del carbonio possono direttamente essere utilizzati per la sintesi di altri composti terminali, come amminoacidi, acidi grassi, lipidi e proteine. Quindi, mentre alcune molecole di Fru-6-P del ciclo sono utilizzate per la sintesi di carboidrati, altre molecole di triosofosfati e di 3-PGA vanno a sintetizzare altri composti. Un continuo ed efficiente funzionamento dei sistemi fondamentali fotosintetici e di quelli biosintetici richiede che l'insieme sia soggetto a rigoroso controllo metabolico. Questo controllo è raggiunto nelle cellule vegetali con la regolazione metabolica dell'attività di certi enzimi che catalizzano le reazioni-chiave del ciclo e dei processi metabolici originati dal ciclo stesso (v. Bassham, 1971). L'attività di questi enzimi è a sua volta regolata dalle condizioni cellulari (fotosintesi, respirazione, maturità, stato di salute, ecc.) ed è regolata in modo da rispondere ai cambiamenti delle condizioni ambientali (temperatura, pressione di CO2, ecc.). I siti regolatori importanti, nell'ambito del ciclo riduttivo del carbonio, sono la reazione di carbossilazione (il passaggio iniziale in cui viene incorporato il diossido di carbonio) e le reazioni in cui il Fru-1,6-P2 è convertito a Fru-6-P, il sedoeptulosio-1,7-difosfato (Sed-1,7-P2) a sedoeptulosio-7-fosfato (Sed-7-P) e il Ru-5-P a Ru-1,5-P2. Gli enzimi che catalizzano ciascuna di queste reazioni diventano inattivi in assenza di luce, quando la fotosintesi si arresta e le reazioni catalizzate da detti enzimi non procedono affatto o procedono molto lentamente.
In presenza di luce questi stessi enzimi regolano il bilancio del carbonio all'interno del ciclo facendo fluire il carbonio dal ciclo stesso verso reazioni collaterali. Pertanto, quando una maggiore quantità di carbonio è necessaria per sintetizzare grassi e proteine, la velocità di conversione del Fru-1,6-P2 in Fru-6-P può essere leggermente diminuita, cosicché si accumula carbonio sotto forma di 3-PGA e triosofosfati che vengono prelevati dal ciclo e usati per la biosintesi di grassi e proteine. Quando il fabbisogno fisiologico delle piante è maggiore nei riguardi dei carboidrati, l'attività dell'enzima Fru-1,6-difosfatasi aumenta rispetto a quella della carbossilasi, quindi il carbonio viene accumulato come Fru-6-P e utilizzato per la sintesi dei carboidrati. Ulteriori controlli metabolici sono effettuati dagli enzimi catalizzanti reazioni che partono da composti del ciclo, con formazione di prodotti collaterali.
L'inattivazione al buio degli enzimi regolatori del ciclo fa sì che l'apparato metabolico del cloroplasto passi da un metabolismo fotosintetico a uno ossidativo quando il sole tramonta. Piccoli cambiamenti di attività di questi enzimi in presenza di luce mantengono bilanciato il flusso di carbonio dal ciclo fondamentale alle vie biosintetiche.
11. Fotorespirazione
La fotorespirazione è quel processo in cui parte del carbonio incorporato ex novo per fotosintesi viene nuovamente ossidato ed eliminato come diossido di carbonio. Sembra che questo processo, in molte piante, limiti la velocità massima di fotosintesi netta raggiungibile. La fotorespirazione aumenta all'aumentare della concentrazione di ossigeno, della temperatura e dell'intensità di illuminazione e al diminuire della concentrazione di diossido di carbonio. La fotorespirazione è la causa principale dell'inibizione della fotosintesi da parte dell'ossigeno. Il composto principale di questo processo è l'acido glicolico (per una rassegna su questo argomento, v. Tolbert, 1971). Questo acido a due atomi di carbonio si forma per ossidazione degli atomi di carbonio 1 e 2 sia dei glucidi monofosfati che dei difosfati presenti nel ciclo riduttivo dei pentosofosfati. Una piccola parte di questo acido viene utilizzata a scopo biosintetico, ivi compresa la sintesi di un importante amminoacido, la glicina. Il restante acido glicolico, prodotto per ossidazione dei glucidi fosfati, in alcune alghe unicellulari, come la Chlorella pyrenoidosa, viene escreto. Nelle foglie delle piante superiori l'acido glicolico viene metabolizzato al di fuori dei cloroplasti con formazione di CO2 e di alcuni composti carboniosi ridotti, che sono riutilizzati.
12. Via degli acidi piruvico e malico
Per piante che crescano in condizioni di semi-aridità, con temperature e intensità luminose elevate, la fotorespirazione può rappresentare un problema serio, essendo, a causa di questa, ridotta la crescita e la riproduzione; ciò avviene in quanto le piante che crescono in tali condizioni spesso devono chiudere gli stomi, attraverso cui il diossido di carbonio penetra nella foglia, per evitare perdite di acqua. Ne risulta una diminuzione della pressione di CO2, mentre sotto intense illuminazioni si ha una fotorespirazione molto intensa. Alcune specie ditali piante hanno sviluppato un meccanismo protettivo in cui viene consumata dell'energia per difesa contro la fotorespirazione: tale meccanismo si riscontra, ad esempio, nella canna da zucchero, nel mais e in altre specie e consiste in una fissazione preliminare del carbonio, che utilizza composti intermedi non facilmente ossidabili.
Questo processo (v. fig. 6) inizia con la carbossilazione dell'acido fosfoenolpiruvico (PEPA) per dare acido ossalacetico (OAA), che viene quindi ridotto con il NADPH ad acido malico (v. Kortschak e altri, 1965; v. Hatch e Slack, 1966). Questa parte del ciclo avviene nelle cellule del mesofillo, che sono più vicine alla superficie della foglia; si pensa che in seguito l'acido malico migri da queste cellule a quelle vascolari, che si trovano più in profondità. Qui l'acido malico viene decarbossilato producendo acido piruvico, NADPH e CO2: quest'ultimo viene poi incorporato per mezzo del ciclo riduttivo dei pentosofosfati (v. fig. 4). Il piruvato presumibilmente torna nelle cellule del mesofillo, dove reagisce con ATP e fosfato inorganico producendo PEPA, difosfato inorganico (PPi) e adenosinmonofosfato (AMP). Una rassegna su questo argomento è quella di Hatch e Slack (v., 1970).
Per formare di nuovo ATP dall'AMP sono necessarie due fosforilazioni (v. fosforilazione ossidativa): quindi il fabbisogno energetico di questo ciclo aggiuntivo è di due molecole di ATP per ogni molecola di diossido di carbonio. Poiché le piante che adoperano questo ciclo crescono in condizioni d'intensa illuminazione, l'energia non costituisce di certo un fattore limitante. Il vantaggio per tali piante è che in questo ciclo, essendo il diossido di carbonio prodotto per fotorespirazione nello strato più interno dei tessuti, esso può essere reincorporato dalle cellule del mesofillo prima che arrivi a sfuggire dalla foglia. Di conseguenza, le cellule che presentano questo ciclo con composti a quattro atomi di carbonio si sono adattate con evoluzioni biochimiche e morfologiche a utilizzare più efficientemente il diossido di carbonio, che per esse è limitante, e meno efficientemente l'energia, che non lo è.
13. Struttura dei cloroplasti
Prima di rivolgere la nostra attenzione ai vari passaggi della fotosintesi è necessario considerare in maggior dettaglio la struttura estremamente complessa e organizzata del cloroplasto, che racchiude l'intero apparato fotosintetico. I cloroplasti hanno approssimativamente la forma di sferoidi schiacciati ai poli, con dimensioni di circa 2,5×5,5 μm; ogni cloroplasto è racchiuso in una doppia membrana. In alcune alghe vi è un solo cloroplasto che può occupare più di metà del volume della cellula; le cellule di piante superiori, come gli spinaci, essendo molto grandi, contengono più cloroplasti.
Quando si esamina col microscopio elettronico la sezione trasversale di un cloroplasto, si distinguono parti di aspetto diverso. La parte dello stroma contiene poche membrane ed è per lo più non strutturata; è occupata da enzimi solubili, tra cui quelli del ciclo riduttivo del carbonio. Altre piccole aree non strutturate sono costituite da sezioni di granuli di amido. Nelle zone strutturate vi sono le lamelle, che sono membrane contenenti tutti i pigmenti fotosintetici e le proteine legate, i lipidi e i coenzimi dell'apparato di trasporto dei fotoelettroni. Alcune lamelle si estendono attraverso tutto il cloroplasto.
Lo studio delle sezioni trasversali dimostra che le lamelle sono unite per gli spigoli e formano dei dischi cavi chiusi, detti tilacoidi (cioè sacciformi). Vi sono almeno due tipi di spazi nel cloroplasto: quello all'interno dei tilacoidi e quello all'esterno, che si confonde con lo spazio stromale.
In molte piante superiori i cloroplasti hanno un'ulteriore importante caratteristica: in alcune regioni di essi i tilacoidi sono strettamente uniti in pile dette grani; poiché le lamelle contengono la clorofilla e altri pigmenti, i grani sono molto colorati e si possono vedere al microscopio ottico come corpicciuoli verdi all'interno dei cloroplasti.
Alcuni tilacoidi sembrano estendersi attraverso la regione stromale e sono connessi in vari punti con i tilacoidi che sono all'interno dei grani; in alcuni cloroplasti sembra che un singolo grande tilacoide stromale possa connettersi con molti differenti tilacoidi dei grani; quindi sarebbe possibile la diffusione di piccoli ioni, come i protoni, nello spazio interno dei tilacoidi.
Le lamelle hanno una struttura e una composizione chimica complesse; contengono approssimativamente eguali quantità di lipidi e proteine: queste ultime comprendono proteine strutturali, enzimi e proteine munite di coenzima. Le proteine strutturali, che possono avere, o meno, una specifica funzione catalitica, tengono insieme gli altri componenti formando una matrice in cui questi possono essere immersi. Gli enzimi, nelle lamelle, sono i catalizzatori che favoriscono reazioni specifiche, come l'ossidazione dell'acqua o il trasferimento di elettroni dalle membrane ai trasportatori solubili.
Le proteine munite di coenzima, nelle lamelle, sono importanti come trasportatori di elettroni e comprendono i citocromi, le proteine contenenti ferro non eminico e quelle contenenti rame. I citocromi contengono una parte proteica e un anello porfirinico (eme) con un atomo di ferro al centro, capace di ossidarsi e ridursi per rimozione o aggiunta di un elettrone. Quando un citocromo viene ossidato o ridotto, il suo spettro di assorbimento (cioè il suo colore) cambia: quindi si può usare uno spettrofotometro per seguire cambiamenti di ossidazione a carico di questi pigmenti, che si verificano quando gli elettroni sono trasportati attraverso di essi nei tessuti vegetali. Hanno importanza, per il trasporto di elettroni nella fotosintesi, il citocromo f, con massimo di assorbimento a 553 nm, e due citocromi di tipo b uno con massimo di assorbimento a 559 nm e un altro, il citocromo b6, con massimo a 564 nm.
Oltre agli atomi di metallo contenuti nei citocromi, ve ne sono molti altri nelle proteine delle lamelle: per un peso molecolare proteico totale di 900.000 vi sono due atomi di manganese, 10 di ferro e 6 di rame. Gli atomi di manganese sono importanti per i passaggi che riguardano l'ossidazione dell'acqua e la produzione di O2. Il ferro e il rame proteici sono implicati in altri stadi del trasporto elettronico; la proteina contenente rame è detta plastocianina (PC). L'accettore terminale di elettroni nella via di trasporto di essi all'interno delle lamelle è la ferredoxina, una proteina contenente ferro non eminico che in parte è legata alle lamelle, in parte è tra i componenti solubili del cloroplasto: può darsi che la ferredoxina solubile prelevi elettroni da quella legata, trasportandoli così ai componenti solubili della regione stromale.
La parte lipidica delle lamelle è formata per un quarto da pigmenti e coenzimi e per tre quarti da lipidi e fosfolipidi. Questi sono essenziali per la struttura delle lamelle, che sono membrane, e probabilmente conferiscono alle membrane la proprietà di comportarsi come isolanti elettrici, in modo che si possa instaurare una differenza di potenziale tra le due superfici di esse. È possibile che questa differenza di potenziale si stabilisca per conduzione di elettroni o di ioni carichi attraverso specifici punti di passaggio nella membrana. Il potenziale diviene una fonte di energia elettrica o chimica, analogamente a quanto avviene in un condensatore che può liberare energia in un circuito elettrico.
Un'altra funzione dei lipidi nelle membrane lamellari è di servire come solvente per le molecole idrofobiche, necessarie per alcune reazioni fotochimiche o per il trasporto di elettroni, ma non solubili in mezzo acquoso. Si pensa che i fosfolipidi abbiano la funzione di agenti tensioattivi, orientando la parte lipidica della molecola verso la fase idrofobica e i gruppi fosforici verso la fase acquosa; così orientati, i fosfolipidi conferirebbero stabilità alle strutture lamellari, contribuendo all'orientazione di altri componenti.
Circa un quinto della parte lipidica delle lamelle è costituito da un pigmento verde, la clorofilla, che per due terzi è clorofilla a e per il resto clorofilla b. Nelle lamelle si trovano grandi quantità di pigmenti giallo-arancione, i caroteni e i carotenoidi, e parecchi composti del tipo del plastochinone. I chinoni sono importanti per il trasporto di elettroni, in quanto possono assumere uno o due elettroni e funzionare sia in ambiente acquoso che non acquoso. La funzione dei caroteni non è nota, ma essi possono essere importanti per la stabilizzazione delle proprietà strutturali e fisiche dei complessi pigmenti-proteine.
La struttura delle lamelle non è ben conosciuta, ma è evidente che essa è altamente organizzata e che questa organizzazione è necessaria per un corretto svolgimento dei processi fotosintetici in presenza di luce. Il più alto grado di organizzazione sembra essere necessario per la formazione dell'ATP, in quanto il frazionamento delle lamelle in frammenti minori distrugge la loro capacità di sintetizzare questo composto in concomitanza all'utilizzazione della luce e al trasporto di elettroni. Le lamelle possono essere frammentate con mezzi meccanici in unità più piccole capaci di assorbire energia luminosa e di ossidare l'acqua con formazione di ossigeno, trasportando contemporaneamente elettroni verso opportuni accettori. Con particolari trattamenti delle lamelle basati sull'uso di ultrasuoni o di detergenti, si possono ottenere due tipi di subunità: un tipo è capace di assorbire luce, di ossidare acqua e di svolgere ossigeno, cedendo nel contempo elettroni a un colorante opportunamente aggiunto, che ne viene ridotto. L'altro tipo di subunità può assorbire luce e trasferire elettroni da un donatore di elettroni artificiale all'accettore naturale di essi, la ferredoxina. Si pensa che questi due tipi di attività fotochimiche rappresentino i due stadi del trasporto di fotoelettroni per azione della luce, come sarà descritto in seguito.
14. Conversione primaria dell'energia fotochimica
Dall'analisi degli esperimenti cinetici e dalla conoscenza della composizione in pigmenti e coenzimi delle lamelle si può ricavare la struttura dell'apparato per la conversione dell'energia. Si pensa che l'unità primaria di conversione fotochimica sia formata da un grande numero di molecole di clorofilla, forse 300 circa, disposte intorno a un centro di reazione in cui avviene la conversione energetica per una rassegna sull'argomento, v. Clayton, 1965). In questo centro di reazione vi sarebbero alcune speciali molecole di clorofilla che possono essere ossidate o ridotte (perdere o acquistare elettroni). In intima unione con questa speciale clorofilla vi sarebbero i trasportatori di elettroni, come i citocromi e le proteine contenenti ferro, rame e manganese. Allorché l'energia luminosa viene assorbita da altre molecole di clorofilla (non presenti nel centro di reazione), lo stato di eccitazione viene trasferito da una molecola di clorofilla all'altra fino a giungere al centro di reazione. Quando la clorofilla del centro di reazione viene eccitata, cede un elettrone a un accettore che lo trasferisce, a sua volta, ad altre molecole (v. Calvin, 1958). La molecola di clorofilla ossidata, poi, strappa un elettrone da un donatore di elettroni e ritorna allo stato non eccitato
Impulsi luminosi di brevissima durata (20 nanosecondi) sembrano poter suscitare un potenziale elettrico attraverso le membrane (v. Wolff e altri, 1969). È possibile che i donatori e gli accettori di elettroni nel centro di reazione siano disposti in modo tale che la risultante del trasporto fotoelettronico sia un movimento di elettroni attraverso la membrana, dall'interno all'esterno del tilacoide (la parte stromale) (v. Grünhagen e Witt, 1970).
Vi sono due tipi di centri fotoreattivi nelle lamelle delle piante verdi; insieme questi centri generano potenziale chimico sufficiente per compiere tutte le reazioni della fotosintesi. Il potenziale chimico complessivo richiesto per trasferire elettroni dall'ossigeno dell'acqua ai cofattori necessari per ridurre il diossido di carbonio è troppo alto per poter essere generato in una singola reazione fotochimica: ciò a causa delle limitazioni termodinamiche dell'efficienza di conversione luminosa, discussa in precedenza, e del fatto che parte dell'energia luminosa deve essere utilizzata per formare ATP.
In un tipo di centro di fotoreazione si forma un cofattore ossidato abbastanza reattivo da strappare elettroni all'acqua producendo ossigeno molecolare; il cofattore ridotto prodotto nella stessa fotoreazione cede i suoi elettroni ad altri trasportatori intermedi.
In un altro tipo di apparato fotochimico, il cofattore ossidato formatosi per azione della luce è nuovamente ridotto per mezzo di elettroni ceduti dai trasportatori testé citati. Il cofattore ridotto fotochimicamente trasferisce i suoi elettroni alla ferredoxina; nella zona dello stroma la ferredoxina ridotta cede elettroni al NADP, che viene utilizzato nelle reazioni di riduzione del carbonio.
15. Via di trasporto dei fotoelettroni
Al giorno d'oggi è universalmente riconosciuto che ogni elettrone trasportato dall'acqua ai cofattori usati nella riduzione del carbonio deve passare attraverso due stadi fotochimici, come proposto da R. Hill e F. Bendall nel 1960. Una versione corrente di questo schema comprende due stadi fotochimici e diversi trasportatori intermedi di elettroni, che trasportano questi da uno stadio fotochimico all'altro; inoltre include altri fattori necessari per l'ossidazione dell'acqua e la riduzione della ferredoxina.
Nel fotosistema II, l'energia di un fotone assorbito è usata per effettuare il trasferimento di un elettrone dal pigmento (PII) del centro di reazione a qualche trasportatore (Q) di potenziale ossidoriduttivo intermedio. Gli elettroni sono in seguito trasferiti da Q al plastochinone (PQ). Le molecole di plastochinone sono probabilmente molto più numerose dei centri di reazione. Sembra probabile che il plastochinone abbia un importante ruolo nell'accumulo e nel trasferimento di elettroni tra i due sistemi fotochimici (v. Schmidt-Mende e Witt, 1968).
Il pigmento ossidato (P+II) deve essere un potente ossidante in quanto è capace di strappare elettroni all'ossigeno dell'acqua, il che richiede un potenziale maggiore di +0,8 volt. I dettagli di questa reazione non sono ancora noti: lo sviluppo di una molecola di O2 richiede la rimozione di 4 elettroni, due da ogni molecola d'acqua. Studi cinetici della quantità di ossigeno sviluppata in funzione di successivi impulsi di luce molto intensa separati da brevi periodi di oscurità suggeriscono la presenza di diversi passaggi sequenziali in questo processo ossidativo. Il ruolo del manganese in tale contesto potrebbe dipendere dal fatto che questo metallo ha diversi livelli stabili di ossidazione.
Nel fotosistema I un elettrone viene ceduto dalla molecola di pigmento PI a un accettore sconosciuto Z. La natura di Z è appunto sconosciuta; il suo potenziale come agente riducente dovrebbe essere tra −0,55 e −0,7 volt (v. Kok e altri, 1965); secondo esperimenti di altri autori (Hyama e Ke, 1971), esso avrebbe una banda di assorbimento a 430 nm. In seguito l'elettrone verrebbe trasferito da Z- alla ferredoxina.
Parte della ferredoxina è legata alla matrice lamellare e viene ridotta anche a −196 °C per illuminazione dei cloroplasti di spinaci (v. Malkin e Bearden, 1971). Ossidoriduzioni che avvengono anche a temperature così basse sono spesso considerate come eventi primari della fotosintesi, cioè non mediati da enzimi: è possibile che gli elettroni passino da PI a Z e quindi alla ferredoxina legata senza l'intervento di enzimi.
La ferredoxina legata, ridotta, che si trova all'interfacie della membrana può presumibilmente cedere elettroni alla ferredoxina solubile nella regione dello stroma, la quale a sua volta può cederli al NADP+ o ridurre direttamente il nitrato a ione ammonio o il solfato a solfito.
Si pensa che la molecola di pigmento ossidato P+I (detta anche P700) sia una clorofilla a ossidata; ha un potenziale di +0,43 volt (v. Kok, 1961); può riossidare il citocromo f e la plastocianina (PC), che a loro volta ricevono elettroni dal fotosistema II tramite trasportatori intermedi come il plastochinone o il citocromo b559.
Oltre al flusso di elettroni dall'acqua al NADP secondo questo schema di duplice azione luminosa, vi può essere anche un riflusso di elettroni da Z- a PI, mediato dai citocromi.
16. Prove dell'esistenza di due distinte reazioni fotochimiche
1. Si conoscono varie prove dell'esistenza di due distinte reazioni fotochimiche, che richiedono luce di due diverse lunghezze d'onda. Benché la luce rossa, con lunghezza d'onda superiore a 680 nm, venga assorbita dalla Chlorella pyrenoidosa, la sua resa quantica, in assenza di luce di altro tipo, rispetto alla produzione di ossigeno è molto bassa. Se si illumina con luce di lunghezza d'onda minore, non solo si registra l'aumento nella produzione di O2 dovuto a quest'ultima, ma aumenta di molto anche la resa della luce a lunghezza d'onda maggiore (v. Emerson e altri, 1957). Ciò fa pensare a una cooperazione dei due tipi di luce nel trasporto di elettroni con produzione di ossigeno e riduzione del CO2. Rimane da stabilire se questa cooperazione (aumento) si verifica solo a livello della cellula in toto e dei cloroplasti nel loro insieme o è un fenomeno inerente al trasporto di elettroni dall'acqua al NADP+ nei tilacoidi.
2. Il trasporto di elettroni dall'acqua al NADP+ in tilacoidi isolati, sotto illuminazione, può essere evidenziato se si aggiungono alla sospensione di tilacoidi NADP+, ferredoxina e un enzima che facilita il trasporto di elettroni ai componenti solubili; si sviluppa ossigeno, mentre viene ridotto il NADP+. Si dimostra così l'effetto cooperativo delle due luci, a maggiore e minore lunghezza d'onda, nei riguardi del trasporto di elettroni dall'acqua al NADP+ (v. Govindjee e Hoch, 1964). Quindi il trasporto dei fotoelettroni nei tilacoidi richiede due reazioni fotochimiche cooperative, una delle quali può essere attivata da luce di 700 nm. Diversi ricercatori per qualche tempo non hanno potuto dimostrare questo effetto nei tilacoidi isolati, finché non si è scoperto che bisognava aggiungere, ai tilacoidi isolati, ioni magnesio in concentrazioni comparabili a quelle presenti nei cloroplasti (v. Sun e Sauer, 1971).
3. Nel sistema di tilacoidi isolati e illuminati, come descritto sopra, il trasporto di elettroni dall'acqua al NADP+ può essere bloccato per aggiunta dell'erbicida diclorofenilmetilurea (DCMU). Quando i tilacoidi sono osservati con uno spettrometro che misura i cambiamenti di assorbimento della luce dovuti all'ossidazione di composti colorati, si nota l'ossidazione del citocromo f; ciò fa supporre che gli elettroni siano trasportati dal fotosistema I a partire da trasportatori intermedi come il citocromo f fino alla ferredoxina e al NADP, ma che gli elettroni sottratti al citocromo f non vengano rimpiazzati da quelli provenienti dall'acqua attraverso il fotosistema II. Studi di questo genere hanno dimostrato altresì che l'azione inibente della DCMU si esercita sul trasporto di elettroni da Q al plastochinone (PQ). Quando si aggiungono donatori di elettroni artificiali capaci di cedere elettroni a trasportatori intermedi di elettroni, a valle del blocco, si verifica un flusso di elettroni da questi donatori, attraverso il fotosistema I, alla ferredoxina e al NADP e si può osservare la riduzione del citocromo f e del NADP+.
4. È possibile osservare interruzioni nel trasporto intermedio di fotoelettroni tra le due reazioni fotochimiche in alcuni mutanti dell'alga Chlamydomonas reinhardi (Levine e Smiley, 1962). Per esempio, uno di tali mutanti, che è incapace di effettuare l'ossidazione dell'acqua, è in grado di fotoridurre il NADP+ senza produzione di ossigeno, purché siano presenti donatori artificiali di elettroni.
5. Anche in assenza di interruzioni tra i due fotosistemi, la luce a lunghezza d'onda maggiore (700 nm) produce l'ossidazione di trasportatori intermedi di elettroni, come il citocromofe il plastochinone. Illuminando poi con luce a lunghezza d'onda minore, si nota una parziale riduzione di questi composti.
6. È stata calcolata la resa quantica di ciascuno dei due fotosistemi: viene assorbito un fotone per ogni elettrone trasferito in ognuno dei due sistemi, cioè due fotoni per ogni elettrone trasferito dall'acqua al NADP+; quindi in totale per staccare 4 elettroni da due molecole d'acqua, produrre una molecola di O2 e ridurre una molecola di CO2 sono necessari 8 fotoni.
17. Fotofosforilazione
Parte dell'energia luminosa assorbita viene usata nei tilacoidi per trasformare ADP e fosfato in ATP (v. Arnon e altri, 1954). Questo processo, detto fotofosforilazione, è stato distinto in due tipi: ciclico e non ciclico (v. Whatley e altri, 1960). Nella fotofosforilazione ciclica gli elettroni trasferiti dal fotosistema I all'agente riducente (Z-) ritornano al pigmento ossidato (P+I) tramite vari trasportatori intermedi. L'energia liberata da questo flusso ‛discendente' di elettroni sarebbe usata, secondo una teoria, per la formazione di ATP. Nella fotofosforilazione non ciclica la formazione di ATP accompagna il flusso di elettroni dall'acqua alla ferredoxina. In questo caso si potrebbe ottenere energia dal flusso di elettroni da Q al PI. Una possibilità alternativa per entrambi i tipi di fosforilazione è che l'energia utilizzata sia una parte dell'energia convertita nelle reazioni fotochimiche primarie. Secondo questa teoria, la reazione primaria non solo sposterebbe gli elettroni dalla molecola di pigmento all'accettore primario, ma fornirebbe nel contempo l'energia potenziale, probabilmente sotto forma di un potenziale di membrana, che in seguito potrebbe effettuare la trasformazione dell'ADP e del fosfato in ATP.
Dalla superficie della membrana tilacoidea può essere isolata una proteina con funzione di fattore accoppiante; questo fattore, in presenza della membrana energizzata, è capace di catalizzare la formazione di ATP da ADP e fosfato utilizzando l'energia fornita dalla membrana stessa.
Le principali teorie sul meccanismo di accoppiamento possono essere divise in chimiche, chemiosmotiche e conformazionali (v. fosforilazione ossidativa). Secondo la teoria chimica, il flusso discendente di elettroni da un trasportatore a un altro è utilizzato per produrre un composto ossidato o ridotto (X~I), che è tanto reattivo da poter legare il fosfato inorganico producendo un composto fosforilato (X~P) utilizzabile a sua volta dal fattore accoppiante per fosforilare l'ADP ad ATP.
La teoria chemiosmotica propone che si instauri un gradiente di ioni H+ in modo che il pH all'interno del tilacoide sia molto minore del pH nella regione dello stroma: tale gradiente è una forma di energia potenziale. Il passaggio di tre protoni dall'interno all'esterno del tilacoide attraverso un gradiente di 4 unità di pH (il che equivale a un rapporto di 104 tra le concentrazioni di idrogenioni) può fornire abbastanza energia da formare una molecola di ATP da ADP e fosfato inorganico.
Il gradiente di H+ può derivare dal movimento unidirezionale di elettroni attraverso la membrana e di atomi di idrogeno legati a trasportatori nel senso opposto, con liberazione di protoni nel mezzo e successivo ritorno degli elettroni. Per esempio, se la reazione primaria II in presenza di luce estrae elettroni dall'acqua all'interno dei tilacoidi, sarà liberato un protone per ogni elettrone trasportato. Nella superficie stromale della membrana tilacoidea i due elettroni potrebbero reagire con un chinone e due protoni producendo PQH2. A causa della sua liposolubilità, il PQH2 potrebbe attraversare la membrana verso l'interno e qui essere riossidato dal citocromo f, formando due protoni all'interno del tilacoide. Il trasporto di questi due elettroni attraversò la membrana tramite la reazione fotochimica 1 e la susseguente riduzione del CO2 nella regione dello stroma dovrebbe consumare un protone per elettrone. Il risultato netto di queste reazioni sarebbe il trasferimento di due protoni dalla regione stromale all'interno del tilacoide per ogni elettrone trasferito nelle due reazioni in presenza di luce.
La teoria conformazionale partecipa di ambedue le altre teorie. Lo stabilirsi di un gradiente elettrico o ionico attraverso la membrana produrrebbe un forte campo localizzato, in quanto la membrana tilacoidea ha uno spessore di soli 150 Å. Questo campo causerebbe alterazioni nella struttura fisica delle macromolecole della membrana, ad esempio nelle proteine. Tale distorsione fisica della molecola a sua volta produrrebbe la destabilizzazione di alcuni legami normalmente stabili, rendendoli suscettibili di rottura e di conseguenti reazioni chimiche. In tal modo potrebbe essere resa disponibile per la proteina accoppiante l'energia sufficiente a permettere la formazione di una specie reattiva di fosfato, che in seguito potrebbe reagire con l'ADP per formare ATP.
Le presenti informazioni sulla fosforilazione richiedono che in ognuna di queste teorie ogni passaggio sia reversibile.
18. Future ricerche sulla fotosintesi
Benché si sia imparato molto dell'intricato meccanismo con cui le piante verdi utilizzano l'energia luminosa per trasformare i composti inorganici in sostanze organiche complesse, vi sono diversi punti insoluti, tra cui i seguenti: a) il meccanismo preciso con cui viene usata l'energia luminosa per trasportare elettroni da una molecola all'altra, presumibilmente attraverso la membrana tilacoidea; b) il meccanismo enzimatico interessato nell'ossidazione dell'acqua a ossigeno; c) il meccanismo della fotofosforilazione; d) l'esatta natura chimica degli accettori di elettroni generati in ciascuno dei due eventi fotochimici e la loro sequenza; e) la natura del meccanismo regolatore che mantiene bilanciato il rifornimento di ATP e di elettroni per le reazioni fotosintetiche; f) il meccanismo che controlla il flusso di metaboliti e di ioni attraverso la doppia membrana esterna dei cloroplasti; g) i meccanismi biochimici responsabili della regolazione osservata a carico del flusso di carbonio nel ciclo riduttivo dei pentosofosfati e nelle vie metaboliche secondarie; h) l'esatta natura dell'interazione tra i due tipi di cellule fotosintetiche delle piante che sfruttano la speciale via metabolica degli acidi piruvico e malico per fissare il carbonio; i) il meccanismo dettagliato con cui durante la fotorespirazione si produce l'acido glicolico, per ossidazione dei glucidi fosforilati.
La ricerca nel campo della fotosintesi darà senza dubbio risposta ad alcuni di questi quesiti in un futuro prossimo, ma è probabile che sorgeranno nuovi interrogativi.
Bibliografia
Arnon, D. E., Whatley, F. R., Allen, M. B., Photosynthesis by isolated chloroplasts. II. Photosynthetic phosphorylation, the conversion of light into phosphate bond energy, in ‟Journal of the American Chemical Society", 1954, LXXVI, pp. 6324-6329.
Bassham, J. A., Control of photosynthetic carbon metabolism, in ‟Science", 1971, CLXXII, pp. 526-534.
Bassham, J. A., Benson, A. A., Kay, L. D., Harris, A. Z., Wilson, A. T., Calvin, M., The path of carbon in photosynthesis. XXI. The cyclic regeneration of carbon dioxide acceptor, in ‟Journal of the American Chemical Society", 1954, LXXVI, pp. 1760-1770.
Bassham, J. A., Calvin, M., The path of carbon in photosynthesis, Englewood Cliffs, N. J., 1957.
Calvin, M., From microstructure to macrostructure and function in the photochemical apparatus, in Energy conversion by the photosynthetic apparatus (a cura di R. C. Fuller), Upton, N. Y., 1958, pp. 160-180.
Calvin, M., Benson, A. A., The path of carbon in photosynthesis, in ‟Science", 1948, CVII, pp. 476-480.
Calvin, M., Massini, P., The path of carbon in photosynthesis. XX. The steady state, in ‟Experientia", 1952, VIII, pp. 445-457.
Calvin, M., Wilson, A. T., The photosynthetic cycle. CO2-dependent transients, in ‟Journal of the American Chemical Society", 1955, LXXVII, pp. 5948-5957.
Clayton, R. K., Molecular physics in photosynthesis, New York 1965.
Emerson, R., Chalmers, R., Cederstrand, C., Some factors influencing the long-wave limit of photosynthesis, in ‟Proceedings of the National Academy of Sciences", 1957, XLIII, pp. 133-143.
Govindjee, R., Hoch, G., Emerson enhancement effect in chloroplast reactions, in ‟Plant physiology", 1964, XXXIX, pp. 10-14.
Grünhagen, H., Witt, H. T., Primary ionic events in the functional membrane of photosynthesis, in ‟Zeitschrift für Naturforschung", 1970, XXV, b, pp. 373-386.
Hatch, M. D., Slack, C. R., Photosynthesis by sugar-cane leaves, a new carboxylation reaction, and the pathway of sugar formation, in ‟Biochemical journal", 1966, CI, pp. 103-111.
Hatch, M. D., Slack, C. R., Photosynthetic CO2-fixation pathways, in ‟Annual review of plant physiology", 1970, XXI, pp. 141-162.
Hill, R., Bendall, F., Function of the two cytochrome components in chloroplasts. A working hypothesis, in ‟Nature", 1960, CLXXXVI, pp. 136-137.
Hill, R., Scarisbrick, R., Production of oxygen by illuminated chloroplasts, in ‟Nature", 1940, CXLVI, pp. 61-62.
Kok, B., Partial purification and determination of oxidation reduction potential of the photosynthetic chlorophyll complex absorbing at 700 mμ, in ‟Biochimica et biophysica acta", 1961, XLVIII, pp. 527-533.
Kok, B., Rubainski, H. J., Owens, I. V. H., The reducing power generated in photoact I of photosynthesis, in ‟Biochimica et biophysica acta", 1965, CIX, pp. 347-356.
Kortschak, H. P., Hartt, C. E., Burr, G. O., Carbon dioxide fixation in sugar-cane leaves, in ‟Plant physiology", 1965, XL, pp. 209-213.
Malkin, R., Bearden, A., Primary reactions of photosynthesis. Photoreduction of a bound chloroplast ferredoxin at low temperature as detected by EPR spectroscopy, in ‟Proceedings of the National Academy of Sciences", 1971, LXVIII, pp. 16-19.
Ng, K. S., Bassham, J. A., The quantum requirement of photosynthesis in Chlorella, in ‟Biochimica et biophysica acta", 1968, CLXII, pp. 254-264.
Park, R. B., Sane, P. V., Distribution of function and structure in chloroplast lamellae, in ‟Annual review of plant physiology", 1971, XXII, pp. 395-430.
Pirie, N. W., Leaf protein as a human food, in ‟Science", 1966, CLII, pp. 1701-1705.
Rabinowitch, E. I., Photosynthesis and related processes, New York 1945.
Ruben, S., Hassid, W. Z., Kamen, M. D., Photosynthesis with radioactive carbon. II. Chemical properties of the intermediates, in ‟Journal of the American Chemical Society", 1940, LXII, pp. 3443-3450.
Ryther, J. H., Photosynthesis and fish production in the sea, in ‟Science", 1969, CLVI, pp. 72-76.
Schmidt-Mende, P., Witt, H. T., Oxidation of plastoquinone during photosynthesis, in ‟Zeitschrift für Naturforschung", 1968, XXIII b, pp. 228-235.
Sun, A. S., Sauer, K., Pigment systems and electron transport in chloroplasts. I. Quantum requirements for the two light reactions in spinach chloroplasts, in ‟Biochimica et biophysica acta", 1971, CCXXXIV, pp. 399-414.
Tolbert, N. E., Microbodies. Peroxisomes and glyoxysomes, in ‟Annual review of plant physiology", 1971, XXII, pp. 45-74.
Van Niel, C. B., On the morphology and physiology of the purple and green sulphur bacteria, in ‟Archiv für Mikrobiologie", 1931, III, pp. 1-112.
Whatley, F. R., Allen, M. B., Trebst, A. V., Arnon, D. I., Photosynthesis by isolated chloroplasts. IV. Photosynthetic phosphorylation and CO2 assimilation in different species, in ‟Plant physiology", 1960, XXXV, pp. 188-193.
Wolff, C. H., Buchwald, H. E., Rüppel, H., Witt, K., Witt, H. T., Rise time of the light induced electrical field across the function membrane of photosynthesis, in ‟Zeitschrift für Naturforschung", 1969, XXIV, b, pp. 1038-1041.