Alzheimer, malattia di
Alzheimer, malattia di
Malattia degenerativa a esordio tipicamente senile (oltre i 60 anni di età, anche se può manifestarsi più precocemente), con decorso cronico progressivo e prognosi sfavorevole. Deve il suo nome a uno psichiatra tedesco, Alois Alzheimer, che per primo, nel 1907, ne descrisse un caso clinico. Nel mondo occidentale, la malattia di A. (MA) costituisce la più comune forma di demenza, responsabile del 60÷75% di tutti i decadimenti cognitivi.
Clinica e diagnosi
L’esordio tipico si caratterizza per la comparsa di deficit di memoria ingravescenti. Essi sono inizialmente confinati alla memoria episodica anterograda (per es., ricordarsi cosa si è fatto durante la giornata). Successivamente, si estendono ad altri tipi di memoria, come quella prospettica, che riguarda l’organizzazione del futuro prossimo (per es., ricordarsi di un appuntamento), la memoria episodica retrograda, che riguarda eventi passati (autobiografici o pubblici), e la memoria semantica, che costituisce il bagaglio di conoscenze acquisite. Al contrario, la memoria procedurale, implicata nell’esecuzione automatica di azioni, rimane relativamente risparmiata. La fase iniziale della MA è stata recentemente ben caratterizzata con l’introduzione del concetto di mild cognitive impairment («disturbo cognitivo lieve»). Il suo riconoscimento consente di individuare precocemente soggetti a elevato rischio di conversione a MA. Nelle fasi più avanzate di malattia, si assiste a un progressivo aggravamento della sintomatologia, con coinvolgimento di altri domini cognitivi, quali l’attenzione, le funzioni esecutive, le abilità visuo-spaziali, le prassie e il linguaggio. Tipicamente, raggiunto un certo livello di disabilità cognitiva, i soggetti divengono incapaci di assolvere gran parte delle attività quotidiane. Il superamento di questa soglia viene definito conversione a demenza conclamata e risponde ai criteri diagnostici di MA probabile. Tale diagnosi viene correntemente eseguita mediante strumenti clinici e neuropsicologici e con il supporto di marcatori neuroradiologici (misure di atrofia cerebrale regionale) e neurobiologici (dosaggio di isoforme delle proteine β-amiloide e tau nel fluido cerebrospinale). La diagnosi di MA certa può essere definita unicamente mediante criteri anatomopatologici.
Patologia
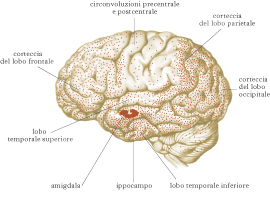
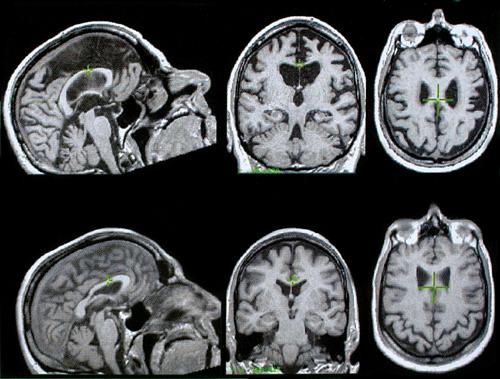
I processi degenerativi della MA coinvolgono specifiche popolazioni neuronali situate nella corteccia cerebrale associativa, responsabile delle funzioni cerebrali superiori. Macroscopicamente, il cervello dei pazienti con MA va incontro a progressiva perdita di volume (atrofia) che, parallelamente all’aggravamento dei deficit cognitivi, coinvolge dapprima le strutture temporali mediali (implicate nelle funzioni di memoria), per poi estendersi all’intera corteccia associativa. Restano relativamente preservate, fino agli stadi più avanzati di malattia, aree cerebrali deputate a funzioni sensoriali e motorie. Microscopicamente, il tessuto cerebrale dei pazienti con MA presenta alterazioni che, riscontrabili anche in soggetti normali, mostrano caratteristiche peculiari di quantità e distribuzione anatomica. Tali alterazioni, descritte per la prima volta da Alois Alzheimer, sono note come degenerazioni neurofibrillari e placche senili. Le prime sono costituite da depositi extracellulari di proteina β-amiloide (➔ amiloide, sostanza), le seconde sono accumuli intracellulari di specifiche isoforme della proteina tau. Indipendentemente dal loro preciso ruolo fisiopatologico (ancora oggetto di intenso dibattito scientifico), queste lesioni si accompagnano a danno neuronale e apoptosi (➔).
Neurochimica
I deficit neurochimici più rilevanti nella MA riguardano la trasmissione colinergica. Essi sono primariamente dovuti a degenerazione del nucleo basale di Meynert, un grosso agglomerato di neuroni che utilizzano acetilcolina come neurotrasmettitore. Questi neuroni proiettano diffusamente all’intera corteccia cerebrale, modulandone l’attività e contribuendo ai meccanismi di plasticità neuronale.
Terapia
Sulla base delle conoscenze neurochimiche, sono stati sviluppati farmaci, attualmente in uso nella cura della MA, denominati anticolinesterasici. Essi, bloccando l’enzima che degrada l’acetilcolina a livello delle sinapsi nervose, ne aumentano la biodisponibilità, e suppliscono alla perdita di neuroni colinergici. Tra gli anticolinesterasici più utilizzati vi sono il donezepil, la rivastigmina e la galantamina. Essi sono efficaci nel migliorare, sebbene per periodi limitati di tempo, i deficit cognitivi della MA. Inoltre, secondo alcuni autori, essi svolgerebbero anche un’azione neuroprotettiva. Un approccio alternativo si basa su molecole, come la memantina, in grado di ridurre l’effetto citotossico dell’acido glutammico. Vi sono inoltre altre terapie in fase di sperimentazione, mirate a modificare i processi fisiopatologici della MA. Notevole interesse si è creato attorno allo sviluppo di vaccini per l’induzione di una risposta immunitaria contro la deposizione di proteina β-amiloide. Nonostante i risultati contrastanti, la strategia immunologica rappresenta tutt’oggi (2010) un’interessante prospettiva. A complemento della terapia farmacologica, esistono strategie comportamentali; in partic., le tecniche di attivazione cognitiva aspecifica vengono utilizzate per stimolare capacità residue e migliorare l’esecuzione di compiti quotidiani. È infine rilevante il supporto (informativo e psicologico) rivolto ai caregivers, ossia coloro che accudiscono i pazienti con MA.