Midollo spinale
Midollo spinale
Il midollo spinale forma insieme all’encefalo il sistema nervoso centrale. Deriva dalla porzione caudale, non vescicolata, del tubo neurale e ne mantiene la struttura cilindrica. È ubicato nel canale vertebrale e nei primi tre mesi della vita intrauterina lo occupa per l’intera lunghezza. Successivamente, la colonna vertebrale si accresce più del suo contenuto, cosicché nell’adulto il midollo, che raggiunge una lunghezza di circa 50 cm, occupa solo i due terzi superiori del canale vertebrale, terminando con un’estremità inferiore a forma conica, il cono midollare, in corrispondenza della parte superiore della seconda vertebra lombare. L’estremo opposto del midollo si continua con il tronco dell’encefalo, precisamente con il bulbo, a livello del forame occipitale.
1. Struttura generale
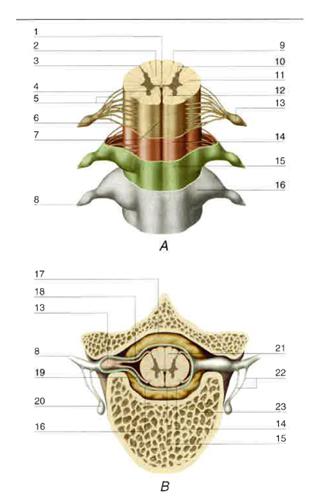
Il midollo spinale è la parte del sistema nervoso centrale che occupa il canale vertebrale e che presiede alla trasmissione afferente ed efferente delle informazioni, rispettivamente sensitiva e motrice, e al meccanismo delle funzioni riflesse. La fig. 1 illustra gli aspetti più importanti della sua morfologia e dei suoi rapporti con la colonna vertebrale.
Nel canale vertebrale, tra la pia madre, che ricopre il tessuto midollare, e il periostio dei corpi e degli archi delle vertebre si interpongono, dall’esterno all’interno, varie strutture, aventi funzione protettiva nei confronti del midollo spinale: lo spazio epidurale, riempito di grasso e di vasi, soprattutto plessi venosi; la dura madre e l’aracnoide che aderisce a essa; lo spazio subaracnoideo, contenente il liquor cerebrospinale.
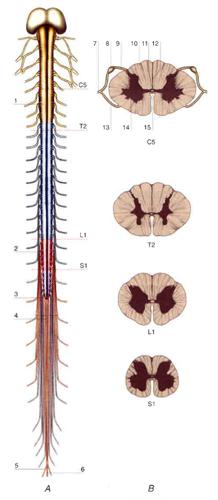
Dalle facce laterali del midollo emergono due serie continue, anteriori e posteriori, di filamenti che convergono da ciascun lato in 31 paia di fasci più spessi, chiamati radici e distinti in anteriori e posteriori, che a loro volta si uniscono a formare altrettanti nervi spinali. All’origine di ciascun nervo spinale, alla radice posteriore è accollato un ganglio radicolare o spinale, contenente neuroni pseudounipolari con neurite a T, le cui branche distali si portano nei nervi periferici e le cui branche prossimali o centrali vanno a costituire la radice posteriore stessa. Le radici anteriori rappresentano i canali efferenti (motori) e le radici posteriori quelli afferenti (sensitivi) del midollo spinale; i 31 nervi spinali di destra e di sinistra (v. nervoso, sistema), dopo aver attraversato i forami intervertebrali a essi corrispondenti, si dividono in vari nervi periferici che distribuiscono fibre di moto e di senso alle rispettive metà del corpo. Si definisce segmento spinale, o mielomero, la porzione di midollo che riceve le fibre delle radici posteriori e dà origine alle fibre delle radici anteriori di un paio di nervi spinali, uno a destra e l’altro a sinistra. Il midollo è pertanto formato da 31 segmenti, e cioè 8 segmenti cervicali, convenzionalmente indicati con le sigle da C1 a C8, 12 segmenti toracici (da T1 a T12), 5 segmenti lombari (da L1 a L5), 5 segmenti sacrali (da S1 a S5), e 1 segmento coccigeo. A causa della minore lunghezza del midollo rispetto alla colonna vertebrale, i segmenti spinali lombari sono dislocati a livello dei corpi delle due ultime vertebre toraciche e della prima lombare, e i segmenti sacrali e coccigei sono situati a livello dei corpi delle prime due vertebre lombari. Di conseguenza, affinché ciascun nervo spinale possa raggiungere il rispettivo forame intervertebrale, la lunghezza delle radici spinali aumenta dall’alto in basso, tanto che, al di sotto del cono midollare, il canale vertebrale è occupato dalle lunghe radici dei segmenti lombari e sacrococcigei, che insieme formano la cosiddetta cauda equina (fig. 2).
2. Organizzazione segmentale dei rapporti tra corpo e midollo
La distribuzione periferica dei nervi spinali obbedisce a una organizzazione metamerica, grazie alla quale le strutture cutanee, muscolari e connettive derivanti da un determinato somite (unità embriologica fondamentale dello sviluppo segmentale di ciascuna metà del corpo) sono innervate pressoché esclusivamente dalle fibre afferenti ed efferenti di un determinato nervo spinale dello stesso lato.
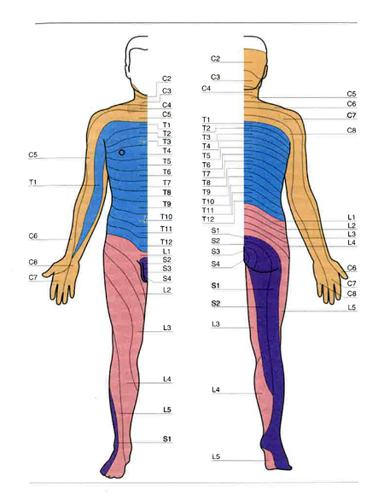
L’organizzazione segmentale è particolarmente manifesta nell’innervazione della cute per la sensibilità tattile, pressoria, termica e dolorifica. La striscia di cute innervata da fibre afferenti a un singolo mielomero si chiama dermatomero. In fig. 3 viene illustrata la corrispondenza tra i dermatomeri del corpo umano e i rispettivi mielomeri; va tenuto presente che i confini tra dermatomeri contigui non sono così netti come suggerisce la figura, in quanto scambi tra i filamenti di radici adiacenti fanno sì che al confine tra dermatomeri contigui esistano zone innervate da due mielomeri anziché da uno. Queste zone di sovrapposizione segmentale sono più sottili per la sensibilità dolorifica che per quella tattile.
L’organizzazione segmentale dell’innervazione dei muscoli, assai meno evidente di quella della cute, è tuttavia indicata dal fatto che i muscoli sottostanti a una data zona cutanea sono di regola innervati dagli stessi mielomeri che innervano i dermatomeri di quella zona. Per es., i mielomeri C1-C4 innervano i muscoli del collo, i mielomeri C5-C6 innervano il bicipite brachiale, i mielomeri C8-T1 innervano i muscoli intrinseci della mano, i mielomeri T2-T12 innervano i muscoli addominali e i muscoli della cassa toracica (escluso il diaframma che è innervato da C3-C5), i mielomeri L1-L2 innervano i flessori della coscia, i mielomeri S1-S2 innervano i flessori plantari della caviglia, e i mielomeri S3-S5 innervano i muscoli perineali e gli sfinteri striati vescicale e rettale. I mielomeri che devono provvedere all’innervazione degli arti, oltre che di una parte del tronco, hanno dimensioni maggiori dei mielomeri che innervano unicamente parti del tronco. Infatti il diametro trasverso del midollo, che in media è di circa 1 cm, aumenta di oltre un terzo nei cosiddetti rigonfiamenti cervicale (da C5 a T1) e lombare (da L1 a S2), in rapporto rispettivamente con gli arti superiori e inferiori.
3. Organizzazione della sostanza grigia e della sostanza bianca midollare
Come nell’encefalo, nel midollo si riconoscono una sostanza grigia e una sostanza bianca. La sostanza grigia midollare è un complesso intreccio (neuropilo) di corpi neuronali, di dendriti, di assoni e delle loro arborizzazioni terminali, di sinapsi, di cellule gliali e di vasi sanguigni. In sezioni trasverse, a qualsiasi livello del midollo, la sostanza grigia spinale si presenta a forma di H distorta e ispessita, posta a cavallo del canale longitudinale obliterato, che rappresenta il punto centrale del midollo (fig. 1). Le due metà dorsali e le due metà ventrali delle gambe della H sono denominate rispettivamente corna posteriori e corna anteriori. La sostanza grigia è circondata da sostanza bianca formata da fibre in maggioranza mieliniche, con decorso ascendente, discendente o commissurale, che hanno origini e terminazioni midollari o extramidollari. Da ciascun lato, la sostanza bianca risulta divisa in tre cordoni o funicoli, separati dalle zone di emergenza dei filamenti delle radici anteriori e posteriori: un funicolo ventrale, un funicolo laterale, a sua volta distinto in ventrolaterale e dorsolaterale, e un funicolo posteriore, che tra C1 e T6 si articola a sua volta in un fascicolo gracile, mediale, e un fascicolo cuneato, laterale.
a) Sostanza grigia. Da un punto di vista funzionale si possono distinguere tre categorie di neuroni midollari. Una prima categoria è costituita dai motoneuroni e dai neuroni pregangliari dei sistemi orto- e parasimpatico, accomunati sia dal fatto che i loro assoni formano le radici anteriori, sia dall’utilizzo dello stesso trasmettitore sinaptico, l’acetilcolina. La seconda categoria è rappresentata dai neuroni di proiezione, che risiedono con il loro corpo nella sostanza grigia midollare, mentre i loro lunghi assoni lasciano il midollo per raggiungere altre regioni del sistema nervoso centrale. La terza categoria è formata dai neuroni propriospinali e dagli interneuroni spinali, il cui assone termina nel midollo spinale stesso.
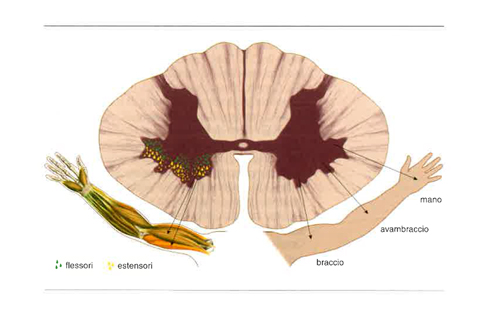
I motoneuroni, il cui numero nella specie umana varia da 2 a 3 milioni, hanno il loro corpo cellulare nelle corna anteriori del midollo e i loro assoni arrivano alle fibre dei muscoli scheletrici, innervando gruppi composti da un numero variabile di fibre muscolari: da 3-4 a varie centinaia. L’insieme di un motoneurone e delle fibre da esso innervate costituisce l’unità motoria. La contrazione muscolare fisiologica può essere causata unicamente dall’attività dei motoneuroni, che rappresentano il tramite unico, o ‘via finale comune’, tra il sistema nervoso centrale e i muscoli. I motoneuroni che innervano un singolo muscolo si aggregano in una colonna compatta che si estende longitudinalmente nel midollo per 1-3 segmenti spinali. Questi aggregati includono tanto i grandi motoneuroni α (con diametro del soma maggiore di 25 μm), che innervano le fibre ordinarie (extrafusali) del muscolo, quanto i meno voluminosi motoneuroni γ (con diametro di circa 15 μm) che innervano i fusi neuromuscolari e modulano la sensibilità allo stiramento del muscolo. Le colonne di motoneuroni che innervano i muscoli assiali, cioè quelli del collo e del tronco, si dispongono in un gruppo motorio mediale, presente in tutti i segmenti midollari; quelle dei motoneuroni per i muscoli degli arti si dispongono in un gruppo laterale, presente solamente nei rigonfiamenti cervicale (arto superiore) e lombare (arto inferiore). Il gruppo laterale è suddiviso in una porzione ventromediale, contenente i motoneuroni per i muscoli dei cingoli scapolare (a livello cervicale) e pelvico (a livello lombare), e una porzione dorsolaterale contenente i motoneuroni per i muscoli intrinseci degli arti e delle loro estremità distali. Sia nel gruppo mediale sia in quello laterale le colonne motoneuronali dei muscoli flessori sono collocate posteriormente rispetto a quelle dei muscoli estensori (fig. 4).
I neuroni pregangliari dell’ortosimpatico e del parasimpatico occupano una porzione della zona intermedia della sostanza grigia tra corno anteriore e corno posteriore. Le colonne di neuroni pregangliari dell’ortosimpatico, dette intermediolaterale e intermediomediale, si estendono da T1 a L2-3 e proiettano, tramite le radici anteriori, i nervi spinali e i rami comunicanti bianchi ai gangli simpatici para- e prevertebrali. Mediante i neuroni postgangliari e le loro proiezioni, il sistema ortosimpatico toracolombare influenza l’attività del miocardio, la motilità dei muscoli lisci intraoculari, la motilità di tutte le resistenze variabili dell’albero vascolare, la motilità dei visceri toracici, addominali e pelvici, le secrezioni lacrimale, sudoripara e di tutte le ghiandole esocrine annesse al canale alimentare. Esso controlla inoltre direttamente, senza l’interposizione di neuroni postgangliari, la secrezione endocrina della midollare del surrene. La colonna dei neuroni pregangliari del parasimpatico sacrale occupa una posizione laterale nella sostanza grigia intermedia dei segmenti da S2 a S4 e proietta ai neuroni postgangliari situati entro o in vicinanza degli organi innervati. Il parasimpatico sacrale influenza, in genere con azione antagonista rispetto all’ortosimpatico, la motilità e la secrezione di parte del grosso intestino, dal colon trasverso al retto, la motilità della vescica, dell’utero e annessi e delle vescichette seminali, e la vasomotilità nei genitali esterni. Così come i motoneuroni costituiscono la via finale comune del sistema nervoso di relazione, i neuroni pregangliari orto- e parasimpatici del midollo spinale costituiscono, insieme ai neuroni pregangliari del parasimpatico craniale, la via finale comune del sistema nervoso vegetativo.
I neuroni di proiezione, che compongono la seconda categoria di neuroni midollari, si possono dividere, funzionalmente, in un gruppo che proietta al talamo (neuroni spinotalamici) e al tronco dell’encefalo (formazione reticolare bulbare e pontina, corpo quadrigemino anteriore e sostanza grigia periventricolare mesencefalica: neuroni spinoreticolari e spinomesencefalici) formando il cosiddetto sistema anterolaterale, e un altro gruppo che proietta al cervelletto tramite i tratti spinocerebellari. I corpi dei neuroni del sistema anterolaterale sono ubicati in tutti i segmenti midollari nella lamina grigia più dorsale (zona marginale) e in altre lamine localizzate alla base del corno posteriore (nucleo proprio), e in parte nella zona intermedia. Essi ricevono direttamente o indirettamente dalle radici posteriori informazioni termocettive, nocicettive e, in esigua parte, tattili che vengono elaborate nel corno posteriore.
La maggioranza degli assoni di questi neuroni si incrocia nel segmento di origine o in quello appena superiore, e sale nei funicoli ventrale e ventrolaterale del lato opposto per raggiungere i centri encefalici per la sensibilità termodolorifica e il tatto protopatico. Altri assoni, meno numerosi, arrivano agli stessi centri decorrendo nel funicolo ventrale ipsilaterale, oppure nei funicoli dorsali di entrambi i lati. I neuroni che danno origine ai tratti spinocerebellari dorsale e ventrale sono situati, rispettivamente, nella colonna mediale di Clarke, alla base del nucleo posteriore nei segmenti da C8 a L3, e nella zona intermedia da L1 a tutti i segmenti sacrali. I tratti spinocerebellari decorrono nel funicolo dorsolaterale dello stesso lato per il tratto dorsale e del lato opposto per il tratto ventrale, che tuttavia si reincrocia nel cervelletto. I tratti spinocerebellare dorsale e ventrale trasmettono al cervelletto, rispettivamente, informazioni propriocettive ed esterocettive dagli arti inferiori, e informazioni dai circuiti riflessi spinali relativi alla parte inferiore del corpo. L’equivalente anatomofunzionale del tratto spinocerebellare ventrale per gli arti superiori, che peraltro ha un decorso senza incrociamenti, è il tratto spinocerebellare rostrale che nasce da neuroni della zona intermedia del rigonfiamento cervicale. L’equivalente anatomofunzionale del tratto spinocerebellare dorsale per gli arti superiori, il tratto cuneocerebellare, non nasce nel midollo spinale ma nel nucleo cuneato del bulbo. Esiste, tuttavia, un tratto cervicocerebellare che prende origine da neuroni della sostanza intermedia dei segmenti cervicali superiori e trasmette al cervelletto informazioni propriocettive dal collo. Il cervelletto utilizza tutte le informazioni che vengono trasmesse dal midollo spinale per adempiere alle sue funzioni di programmazione e di esecuzione dei movimenti.
Per quanto concerne la differenza tra neuroni propriospinali e interneuroni spinali, i quali formano la terza categoria di neuroni midollari, occorre specificare che la denominazione di propriospinali dovrebbe essere riservata ai neuroni che proiettano a segmenti diversi da quello in cui risiede il loro corpo, e quella di interneuroni ai neuroni ubicati interamente in un singolo segmento; generalmente, però, il termine interneuroni si usa per entrambe le categorie. Gli interneuroni spinali svolgono svariati ruoli funzionali, che vanno dalla trasmissione di comandi encefalici ai motoneuroni e ai neuroni pregangliari orto- e parasimpatici alla mediazione di attività riflesse polisinaptiche, dalla generazione autogena di movimenti stereotipati alla modulazione ed elaborazione di informazioni di senso destinate all’encefalo. Dal punto di vista dell’azione sinaptica, gli interneuroni spinali si dividono in eccitatori e inibitori, e su ciascun motoneurone convergono interneuroni di entrambi i tipi. L’attivazione simultanea o consecutiva di interneuroni eccitatori e inibitori da parte di un comando centrale o di un segnale afferente dalla periferia consente la coordinazione delle attività di muscoli diversi secondo il principio dell’innervazione reciproca. Grazie a un complesso schema di connessioni selettive tra interneuroni e motoneuroni spinali, il midollo spinale possiede la capacità di coordinare contrazioni e rilasciamenti muscolari nel tempo e nello spazio, in modo da produrre attività motorie finalizzate. L’innervazione reciproca fa sì che, di regola, l’attivazione dei motoneuroni di un muscolo e dei muscoli sinergici si associ all’inibizione dei motoneuroni dei muscoli antagonisti, facilitando in tal modo il movimento desiderato. Inoltre, sempre in base all’organizzazione specifica delle connessioni intrinseche del midollo, essa consente vari tipi di coordinazione tra movimenti di tutti gli arti, come per es. nella locomozione. Nelle corna anteriori sono presenti gruppi di interneuroni che proiettano direttamente ai motoneuroni e si distinguono per la diversa posizione nella sostanza grigia e la diversa lunghezza dei loro assoni. Gli interneuroni laterali hanno assoni corti con decorso ipsilaterale limitato a pochi segmenti, si connettono con i motoneuroni dei muscoli distali dell’arto superiore o inferiore e servono alle coordinazioni muscolari di un singolo arto; gli interneuroni intermedi hanno assoni che si estendono ipsilateralmente per più segmenti, si connettono con i motoneuroni dei muscoli dei cingoli scapolare o pelvico, e servono alla coordinazione muscolare tra gli arti e il tronco; gli interneuroni mediali hanno assoni che possono percorrere tutta la lunghezza del midollo, si connettono con i motoneuroni dei muscoli assiali dello stesso lato e del lato opposto, e servono alla coordinazione bilaterale dei muscoli del tronco. Una classe speciale di interneuroni spinali inibitori è costituita dai neuroni di Renshaw, che sono attivati da collaterali ricorrenti degli assoni dei motoneuroni e che inibiscono, in un circuito a retroazione negativa, gli stessi motoneuroni o i motoneuroni dello stesso muscolo oppure di muscoli sinergici, utilizzando come trasmettitore sinaptico la glicina. Nonostante la sistematica convergenza di più vie centrali e periferiche su uno stesso interneurone eccitatorio o inibitorio, che consente all’interneurone stesso di essere utilizzato in molteplici attività spinali, vi è una selettività di connessioni per la quale, per es., gli interneuroni inibitori utilizzati dai riflessi a partenza dai recettori muscolotendinei sono diversi dagli interneuroni inibitori utilizzati dai riflessi a partenza dai fusi neuromuscolari. Per quanto riguarda l’elaborazione spinale di segnali sensitivi diretti all’encefalo, si ritiene che i piccoli interneuroni della sostanza gelatinosa del corno posteriore siano in grado di modulare la trasmissione di informazioni nocicettive da parte del sistema anterolaterale, sia influenzando i neuroni che danno origine a questo sistema, sia esercitando un’inibizione presinaptica sulle terminazioni primarie di senso.
b) Sostanza bianca. Si è già detto della divisione della sostanza bianca in funicoli. Oltre ai già ricordati tratti spinocerebellari e al sistema anterolaterale, che originano nel midollo spinale stesso, e ai fasci propriospinali formati dagli interneuroni con assone lungo, la sostanza bianca del midollo spinale contiene fasci di fibre che nascono dai gangli radicolari e ascendono all’encefalo nei funicoli dorsali, nonché fasci di fibre che discendono dall’encefalo lungo i funicoli ventrale e laterale per terminare nel midollo.
Il sistema ascendente dei funicoli dorsali è al servizio della sensibilità tattile discriminativa e della propriocezione muscolare, tendinea e articolare. È formato da fibre di calibro diverso (da grosso a medio), fornite dalle branche centrali dei neuriti appartenenti ai neuroni dei gangli radicolari, che entrano nel midollo medialmente rispetto alle più sottili afferenze primarie termiche e nocicettive e si dividono in due rami che decorrono nel funicolo dorsale dello stesso lato, uno breve discendente e uno lungo ascendente. Al contrario delle afferenze termiche e nocicettive, che sono destinate a terminare nelle corna posteriori, i rami ascendenti delle fibre afferenti primarie dei funicoli dorsali - che al pari dei rami discendenti prendono contatti tramite diramazioni collaterali con neuroni di gran parte della sostanza grigia spinale, motoneuroni inclusi - non terminano nel midollo bensì nel bulbo. Nei funicoli dorsali le fibre che provengono dalle parti inferiori del corpo (arto inferiore e tronco) si dispongono medialmente, formando il funicolo gracile, mentre quelle provenienti dalle parti superiori del corpo (arto superiore, collo e nuca) si dispongono lateralmente, formando il funicolo cuneato. La stazione finale delle fibre dei funicoli gracile e cuneato è rappresentata dai nuclei omonimi del bulbo, da cui parte il lemnisco mediale che è diretto ai nuclei somatosensitivi del talamo.
Le vie discendenti svolgono funzioni diverse: il controllo della postura e dei movimenti, inclusi i movimenti respiratori, esercitato tramite i motoneuroni alfa e gamma spinali e i muscoli da essi innervati; il controllo di funzioni vegetative, mediante l’attività dei neuroni spinali pregangliari dell’ortosimpatico e del parasimpatico; il controllo della trasmissione spinale di informazioni di senso all’encefalo, determinato dalle proiezioni a neuroni delle corna posteriori. I sistemi di proiezione dall’encefalo ai motoneuroni spinali alfa e gamma sono costituiti dalla componente corticospinale della via piramidale e da vie non piramidali con nuclei di origine nel tronco dell’encefalo: la via rubrospinale, la via reticolospinale e, infine, la via vestibolospinale. Tutte queste vie includono fibre che prendono contatto con i motoneuroni, direttamente oppure indirettamente tramite interneuroni spinali intra- o intersegmentali.
La componente della via piramidale destinata al midollo spinale, il fascio corticospinale, prende origine da aree del lobo frontale (area motoria primaria 4 e area premotoria 6 di Brodmann, area motoria supplementare), del lobo parietale (soprattutto dall’area 3a che si trova appena al di dietro dell’area 4) e del lobo limbico (parte anteriore del giro del cingolo). La maggior parte (da 70 a 90%) delle fibre corticospinali provenienti da un emisfero cerebrale (circa un milione) si incrocia nel bulbo e discende nel funicolo dorsolaterale del midollo con le fibre destinate ai motoneuroni cervicali in posizione mediale, quelle destinate ai motoneuroni sacrali in posizione laterale, e quelle destinate ai motoneuroni toracici e lombari in posizione intermedia. La componente crociata del fascio corticospinale prende contatti diretti o indiretti in misura predominante con il gruppo laterale dei motoneuroni, e soprattutto con quelli che controllano le estremità distali e, in particolare, le mani e le dita. La sua funzione principale è relativa ai movimenti volontari, in maniera specifica ai movimenti indipendenti degli arti e, specialmente, ai movimenti manuali che richiedano il controllo differenziato delle singole dita. La componente del fascio corticospinale che non si incrocia a livello bulbare decorre nel funicolo anteriore del midollo e termina a tutti i livelli spinali entro o in vicinanza del gruppo mediale dei motoneuroni, sia dello stesso lato sia del lato opposto. Questo fascio corticospinale che non si incrocia nel bulbo, ma si distribuisce bilateralmente nel midollo, partecipa all’esecuzione di movimenti assiali e dei cingoli scapolare e pelvico, all’esecuzione di movimenti coordinati di più arti, e alle reazioni del tronco che forniscono il sostegno posturale ai movimenti di singoli arti (v. equilibrio).
Delle altre vie discendenti, il fascio rubrospinale si incrocia a livello mesencefalico e nel midollo decorre nel funicolo dorsolaterale assieme al fascio corticospinale crociato, con il quale condivide, in gran parte, gli stessi bersagli motoneuronali, peraltro limitatamente, almeno nell’uomo, al midollo cervicale. Il fascio rubrospinale coopera probabilmente con quello corticospinale crociato per quanto concerne i movimenti unilaterali dell’arto superiore.
Il fascio tettospinale origina dagli strati profondi del corpo quadrigemino anteriore, si incrocia a livello mesencefalico e discende nel funicolo ventrale del midollo spinale per arrestarsi nei segmenti cervicali contenenti i motoneuroni dei muscoli del collo. Poiché nel tronco dell’encefalo rami collaterali del fascio tettospinale si distribuiscono ai motoneuroni dei muscoli estrinseci degli occhi, si ritiene che la sua funzione sia quella di coordinare i movimenti oculari e i movimenti della testa nelle reazioni di orientamento, soprattutto in risposta a stimoli visivi, nonché di esplorazione dell’ambiente con lo sguardo.
La via vestibolospinale contiene fibre che originano nel nucleo vestibolare laterale di Deiters e discendono nel funicolo ventrale dello stesso lato rispetto all’origine, per distribuirsi direttamente o indirettamente ai motoneuroni del gruppo mediale a tutti i livelli segmentali. Altre fibre vestibolospinali originano dai nuclei vestibolari mediale e inferiore e decorrono, sia ipsilateralmente sia controlateralmente, nel funicolo ventrale fino ai segmenti mediotoracici. La funzione principale delle proiezioni spinali del nucleo di Deiters consiste nel contribuire al mantenimento della stazione eretta e dell’equilibrio posturale, trasmettendo informazioni dal labirinto vestibolare ai motoneuroni dei muscoli antigravitari del tronco e degli arti. Le proiezioni spinali dei nuclei vestibolari mediale e inferiore contribuiscono anch’esse all’integrazione delle risposte agli stimoli cinetici e statocinetici che provengono dal labirinto, ma limitatamente a movimenti del capo e del collo e in coordinazione con i movimenti oculari.
In senso lato, la locuzione ‘via reticolospinale’ fa riferimento a un complesso di vie discendenti eterogenee che corrono in tutti i funicoli del midollo, tranne che in quelli posteriori. Esse includono: proiezioni dal nucleo reticolare pontino, che fanno parte di un sistema corticoreticolospinale per la regolazione posturale e anche per l’esecuzione di movimenti volontari, almeno limitatamente ai muscoli assiali e prossimali degli arti; proiezioni dal nucleo bulbare gigantocellulare, con azioni prevalentemente inibitorie per la regolazione posturale; proiezioni dai nuclei reticolare intermedio e paragigantocellulare laterale ai neuroni pregangliari orto- e parasimatici per le regolazioni vegetative; proiezioni dai nuclei retro- e para-ambiguo e del nucleo del tratto solitario ai motoneuroni cervicali e toracici per i movimenti respiratori. Vengono incluse nelle vie reticolospinali anche le proiezioni noradrenergiche dal locus coeruleus e serotoninergiche dal rafe caudale che modulano in maniera aspecifica l’attività dei motoneuroni, e in modo più specifico la trasmissione ascendente di segnali sensitivi, soprattutto nocicettivi, nel corno posteriore. A questa regolazione centrifuga della sensibilità dolorifica (v. dolore) partecipano anche proiezioni discendenti della sostanza grigia periventricolare del mesencefalo, le quali inibiscono direttamente i neuroni da cui origina il sistema anterolaterale, e indirettamente, tramite interneuroni encefalinergici del corno posteriore, anche le afferenze primarie nocicettive. Questo sistema svolge la funzione di mediare almeno in parte l’effetto antidolorifico centrale delle sostanze oppiacee. Un’azione modulante nei confronti delle afferenze tattili e propriocettive viene attribuita alle fibre corticospinali della via piramidale, le quali nascono nella corteccia parietale e terminano nelle corna posteriori.
4. L’attività spinale riflessa e la generazione di attività ritmiche stereotipate
Storicamente le strutture nervose necessarie e sufficienti a produrre risposte riflesse a stimoli fisiologici sono state studiate nel midollo spinale isolato dall’encefalo. I tipi di riflessi spinali di cui sono meglio conosciute le basi nervose sono: il riflesso di stiramento (detto anche monosinaptico o miotatico); il riflesso di tensione (o miotatico inverso); il riflesso di flessione; infine, il riflesso di estensione crociata. Oltre a queste semplici risposte riflesse, che cessano al termine dello stimolo, il midollo è in grado di generare, in risposta a stimoli appropriati, attività muscolari coordinate ritmiche, che, pur non essendo autogenerate, sono capaci tuttavia di continuare autonomamente a lungo dopo la cessazione dello stimolo scatenante. Come si è visto, queste attività sono sostenute da complessi circuiti spinali i cui interneuroni sono in grado di attivare, secondo sequenze organizzate, muscoli sinergici e antagonisti di uno o più arti. Per es., il midollo spinale isolato può produrre, in risposta a stimoli tattili appropriati delle superfici cutanee di appoggio al suolo, attività ritmiche coordinate degli arti che sono tipiche dei movimenti di locomozione. Si ritiene pertanto che nella locomozione normale comandi discendenti dall’encefalo si limitino solamente a dare il via all’attività dei suddetti circuiti spinali specializzati. Altre attività coordinate e prolungate che possono essere avviate con stimoli appropriati del midollo isolato sono rappresentate dai movimenti ritmici di grattamento diretti a punti cutanei sottoposti a rapidi strisciamenti, e dal brivido in risposta al raffreddamento del canale vertebrale. Per contro il midollo, sebbene contenga tutti i motoneuroni dei muscoli respiratori, non possiede alcuna capacità di generare e mantenere i movimenti ritmici del respiro, la cui organizzazione dipende imprescindibilmente da neuroni del tronco dell’encefalo.
5. Cenni di patologia spinale
Una sezione spinale completa, conseguente a un trauma midollare da frattura vertebrale o ferita da arma da fuoco o da taglio, è seguita dalla perdita di tutte le sensazioni e di tutti i movimenti volontari dipendenti dai segmenti spinali al di sotto della sezione. Se il midollo è sezionato al di sopra di C3, il respiro cessa definitivamente e la sopravvivenza è possibile solo grazie alla respirazione artificiale. Tutti i riflessi mediati dai segmenti sottostanti alla sezione, incluso lo svuotamento riflesso della vescica e del retto, sono assenti per lunghi periodi, da giorni a settimane e addirittura mesi, dopo la sezione (areflessia da shock spinale). Questa assenza di riflessi è attribuita primariamente all’eliminazione di un’influenza facilitante esercitata dalle vie discendenti encefaliche sulle strutture spinali, mentre la ricomparsa nel tempo dei riflessi vegetativi e dei muscoli scheletrici dipende da meccanismi ancora poco conosciuti di recupero delle funzioni spinali. A lungo andare, però, questi meccanismi fanno sì che i riflessi del midollo spinale isolato diventino iperattivi, tanto da causare spasticità permanente in flessione o estensione e risposte di massa anziché localizzate.
Esistono patologie che colpiscono in modo selettivo componenti della sostanza grigia o bianca midollare, come per es. la sclerosi laterale amiotrofica o la poliomielite, che danneggiano i motoneuroni con conseguenti paralisi, o la tabe dorsale e l’anemia perniciosa, che alterando il sistema dei funicoli posteriori, si presentano con sintomi sensitivi e anche motori, e le degenerazioni ereditarie dei tratti spinocerebellari, che comportano disturbi di coordinazione motoria.
bibliografia
M.B. Carpenter, Core text of neuroanatomy, Baltimore, Williams and Wilkins, 19914 (trad. it. Napoli, EdiSES, 1995).
The human nervous system, ed. G. Paxinos, San Diego, Academic Press, 1990.
G. Moruzzi, Fisiologia della vita di relazione, Torino, UTET, 1981.
Principles of neural science, ed. E.R. Kandel, J.H. Schwartz, T.M. Jessell, Norwalk (CT), Appleton and Lange, 19913 (trad. it. Milano, Ambrosiana, 1994).
G.M. Shepherd, Neurobiology, New York, Oxford University Press, 1994.