Omeostasi
Omeostasi
Il fisiologo francese Claude Bernard (1813-1878) per primo sottolineò che nei Metazoi esistono due ambienti: l'ambiente esterno, nel quale è posto l'organismo, e l'ambiente interno, nel quale vivono gli elementi che costituiscono l'organismo. L'ambiente interno, rappresentato dal plasma e in senso più ampio da tutti i liquidi extracellulari, possiede caratteristiche tali da permettere l'esistenza delle condizioni fisico-chimiche necessarie per il perfetto funzionamento delle cellule e quindi degli organismi. Bernard ipotizzò che, se il funzionamento delle cellule dipende dalle condizioni fisico-chimiche ottimali dell'ambiente interno, queste dovevano essere il più possibile costanti, ed eseguì numerose ricerche per chiarirne i meccanismi. Il concetto di costanza dell'ambiente interno è riassunto nei seguenti passaggi delle Leçons sur les phénomènes de la vie communs aux animaux et végétaux (1878-1879): "La costanza dell'ambiente interno è la condizione della vita libera, indipendente: il meccanismo che la rende possibile è infatti quello che assicura all'ambiente interno il mantenimento di tutte le condizioni necessarie alla vita degli elementi" e "la costanza dell'ambiente interno richiede un perfezionamento tale dell'organismo che permetta di compensare istantaneamente e di equilibrare le variazioni esterne".
Né il concetto di milieu intérieur né quello della sua costanza sono nati da un risultato sperimentale o da un'intuizione improvvisa, ma si sono formati progressivamente, e con modifiche costanti, nell'arco di quasi trent'anni. Il germe del concetto è riconducibile a certi appunti di Bernard del 1851, nei quali egli parla delle condizioni che permettono la vita, e a due pagine del Traité de chimie anatomique et physiologique di Charles Robin, nelle quali l'autore usa l'espressione milieu de l'intérieur per indicare i fluidi dell'organismo, sottolineando che le loro alterazioni possono determinare distruzione delle parti solide. Gli anni cruciali sono però quelli che vanno dal 1854 al 1857: in quel periodo Bernard stava effettuando studi sulla composizione chimica del sangue, compresi quelli nei quali riportò che il glucosio è presente nel sangue indipendentemente dalla sua presenza nella dieta (un'osservazione che anticipò l'esperimento del fegato lavato e la scoperta del glicogeno). L'insieme di questi fatti, e di molti altri, portò alla prima enunciazione pubblica del concetto e dell'espressione milieu intérieur, il 9 e il 16 dicembre 1857, nel corso di due delle sue famosissime lezioni al Collège de France. Devono invece passare circa dieci anni prima che Bernard si esprima sulla costanza del mezzo interno. Circa cinquanta anni più tardi, il fisiologo statunitense W. Cannon (1871-1945) modificò leggermente il concetto di ambiente interno introducendo il termine 'omeostasi' per sottolineare che le condizioni non sono fisse, ma mantenute dinamicamente entro un ambito (anche se ristretto) da processi autoregolati.
Principî fondamentali delle teorie dei sistemi e del controllo
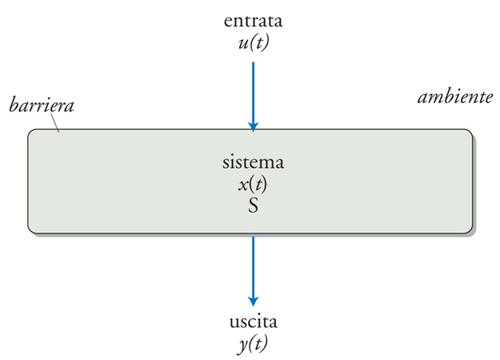
Un sistema è una struttura reale e circoscritta costituita da elementi uniti da interazioni misurabili. Se un sistema scambia materia o energia con l'ambiente, si dice che è aperto: tutti i sistemi biologici sono aperti e ciò conferisce loro la peculiarità di interagire con altri sistemi. Un sistema aperto (e quindi un sistema biologico) è in altre parole una struttura reale e circoscritta (per es., da una membrana, da una capsula connettivale, dalla cute) che possiede un ingresso (input), uno stato, e un'uscita (output) (fig. 3). Un concetto importante nella teoria dei sistemi è quello di funzione di trasferimento (od operatore), un'astrazione esprimibile in termini matematici, che rappresenta l'insieme dei processi che opera sugli input trasformandoli in output. L'input generalmente deriva da altri sistemi e influenza lo stato del sistema; l'output è determinato dallo stato del sistema ed è a sua volta l'input di altri sistemi (e/o dello stesso sistema). L'insieme delle connessioni tra sistemi consente la creazione di estese reti caratterizzate da strutture e comportamenti complessi; un organismo cosituisce il più grande supersistema. Per converso, ogni sistema può essere costituito da sottosistemi, che possono essere organizzati in maniera gerarchica. L'analisi dei sistemi viene spesso e convenientemente rappresentata mediante blocchi funzionali (fig. 4). Alcuni sistemi sono caratterizzati dal fatto che l'output corrisponde in ogni momento alla somma algebrica delle risposte individuali a ogni singolo input (principio di sovrapposizione); come corollario, input maggiori genereranno output che saranno maggiori esattamente nello stesso rapporto (principio di graduazione proporzionale). Sistemi di questo tipo vengono detti 'sistemi lineari'; di fatto tutti i sistemi biologici sono non lineari, ma in molti casi è possibile approssimarli a sistemi lineari e, poiché questi ultimi possono essere espressi in termini matematici, tali approssimazioni sono estremamente utili nel campo della modellistica biomedica.
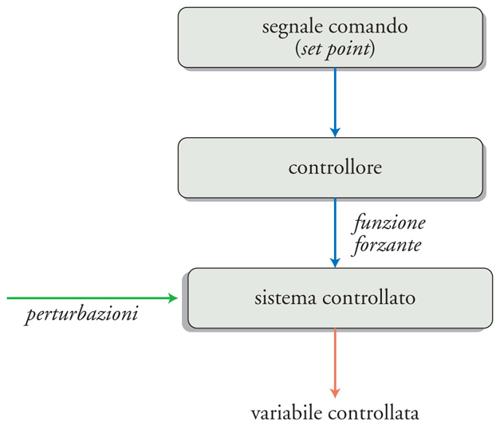
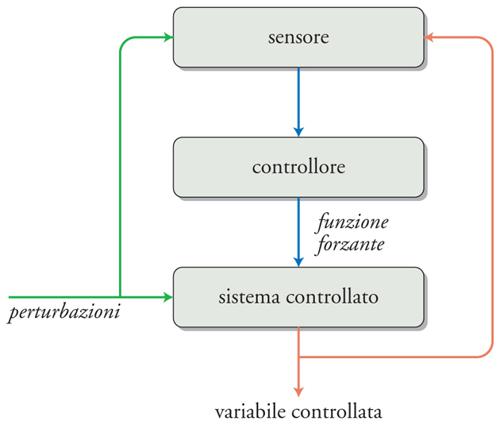
Un sistema è controllato quando i suoi ingressi sono manipolati in maniera tale da causare variazioni predeterminate (o da non causare variazioni) delle sue uscite. La fig. 4 illustra la struttura di un sistema di controllo che ha lo scopo di verificare i valori di alcune variabili perché siano mantenuti entro limiti prestabiliti. Alcune uscite di un dato sistema, dette 'variabili controllate', rappresentano un sottogruppo di tutte le uscite del sistema controllato; lo stato di questo sistema è sottoposto all'influenza di due fondamentali categorie di input, i disturbi e le funzioni forzanti. I disturbi (o perturbazioni) sono tutte le entrate non controllate; esse producono modificazioni non volute nello stato del sistema e di conseguenza della variabile controllata. Le funzioni forzanti (o forzanti) sono quelle che possono essere manipolate per provocare le variazioni desiderate, e rappresentano l'uscita di un altro sistema, detto 'controllore'. La funzione del controllore è di generare forzanti adeguate ai propri input, chiamati set point (o valore di riferimento o segnali comando). Perché il sistema di controllo operi efficacemente, è necessario che riceva un'altra categoria d'entrate, derivata da sensori in grado di definire lo stato del sistema sostanzialmente misurando la variabile controllata. Com'è illustrato nella fig. 5, i sensori possono rilevare o le perturbazioni stesse o la variabile controllata (cioè gli effetti che una perturbazione ha avuto sullo stato del sistema). Nel primo caso, si parla di 'sistema di controllo a feedforward', nel secondo di 'sistema di controllo a feedback'. Le differenze tra i due sono sostanziali. Nel caso di un controllo a feedforward la perturbazione viene rilevata dal sensore prima che induca i suoi effetti sullo stato del sistema e questo significa che il controllore deve essere in grado di calcolare gli effetti che la perturbazione indurrà sulla variabile regolata. I sistemi a feedforward hanno il grande vantaggio di poter evitare che la perturbazione eserciti i propri effetti, prevenendo quindi la necessità di interventi correttivi. Poiché i sistemi di controllo fisiologici sono quasi sempre non lineari e dinamici (ovvero variano con il tempo), e poiché molti potenziali disturbi dovrebbero essere rilevati per poter predire l'effetto sulla variabile controllata, ne consegue che i sistemi a feedforward richiedono complessi meccanismi predittivi; in realtà, con l'eccezione di alcuni meccanismi cerebrali, questo tipo di controllo è meno utilizzato nei sistemi fisiologici, anche se la sua relativa rarità potrebbe dipendere dalla scarsa conoscenza acquisita finora. È stato recentemente suggerito che i sistemi a feedforward finalizzati alla modificazione anticipata dello stato di un sistema e quindi di una sua variabile controllata siano definiti 'allostatici'.
Nel caso di un sistema di controllo a feedback, la perturbazione esercita la propria azione sul sistema, modificandone lo stato e quindi l'uscita, che viene rilevata dal sensore. Il vantaggio che un sistema di controllo a feedback ha rispetto a uno a feedforward è sostanzialmente legato al fatto che non dipende dall'esistenza di meccanismi predittivi, bensì è dovuto alla sua semplicità. Per questa ragione, la grande maggioranza dei sistemi di controllo fisiologici è a feedback. Ciò, ovviamente, non significa che questo tipo di sistema di controllo non abbia limitazioni; per esempio, esso sarà necessariamente più lento (perché deve rendersi palese la conseguenza della perturbazione) e tenderà a produrre oscillazioni a caso di un'azione correttiva eccessiva.
Prima di procedere allo studio dei sistemi di controllo fisiologici è utile sottolineare la fondamentale, anche se sottile, differenza che esiste tra due termini che vengono spesso usati come sinonimi: regolazione e controllo. Per regolazione si intende il processo o l'insieme dei processi che mantengono costante lo stato di un sistema o il valore di una determinata variabile, mentre per controllo si intende lo specifico meccanismo che viene utilizzato a tal fine. Un efficace esempio è rappresentato dai congegni capaci di regolare la velocità di crociera di un'automobile; essa viene mantenuta costante aumentando o diminuendo la quantità di carburante che arriva al motore. In questo caso, il sistema regola la velocità dell'auto controllando la quantità di carburante. Il controllo è quindi un mezzo per ottenere la regolazione.
Sistemi di controllo fisiologici
Sistemi di controllo fisiologici a feedback
L'omeostasi dell'organismo è il risultato dell'azione di un numero elevatissimo di regolatori, che operano simultaneamente, interagiscono e sono organizzati in livelli gerarchici. La stragrande maggioranza dei sistemi di controllo fisiologici è del tipo a feedback: un sensore rileva una delle uscite del sistema, la variabile controllata; l'output del sensore è proporzionale al valore della variabile regolata e al suo valore è sottratto il segnale di riferimento, o set point ‒ che è il valore desiderato della variabile regolata ‒ generando il segnale errore; il segnale errore viene poi amplificato, a volte ulteriormente elaborato, e inviato al sistema controllato come funzione forzante.
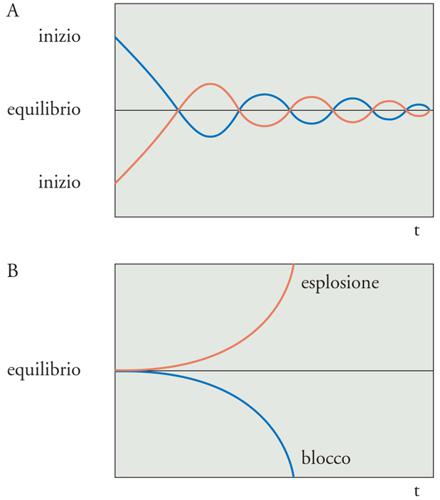
Il segnale errore può essere positivo o negativo: è positivo quando la variabile regolata è superiore al set point e negativo quando è inferiore. Se l'azione del controllore ha segno opposto a quello del segnale errore, essa viene detta 'negativa'; viceversa, se ha lo stesso segno del segnale errore essa viene definita 'positiva'. Nel primo caso si parla quindi di feedback negativo, nel secondo di feedback positivo. In altre parole, un sistema di controllo a feedback negativo è finalizzato a ridurre la differenza tra il valore della variabile regolata e il set point; un sistema così organizzato tende dunque a generare equilibrio, nel nostro caso a mantenere entro un certo ambito la variabile regolata (fig. 6A). Viceversa, in un sistema a feedback positivo l'azione del controllore tende ad amplificare la differenza e il sistema tende alla crescita o al declino esponenziale, fino all'esplosione o al blocco (fig. 6B). Esistono nei sistemi biologici esempi di controllo a feedback positivo, come per esempio quello che promuove le contrazioni dell'utero durante il parto quello relativo alla generazione dei potenziali d'azione. Nel primo caso, le contrazioni uterine spingono la testa del feto nel collo dell'utero, determinandone la distensione; la distensione del collo stimola la liberazione di ossitocina; l'ossitocina aumenta le contrazioni, determinando l'ulteriore spinta della testa del feto nel collo dell'utero. Nel secondo caso, la depolarizzazione della membrana delle cellule nervose e muscolari determina l'apertura dei canali per il Na+ voltaggio-dipendenti; questo provoca l'ingresso di Na+ all'interno della cellula; l'incremento di Na+ all'interno della cellula aumenta la depolarizzazione, che a sua volta determina l'apertura di altri canali. Com'è evidente dagli esempi riportati, i sistemi a feedback positivo non hanno di per sé alcun significato omeostatico. Solo i sistemi a feedback negativo, quindi, sono regolatori omeostatici.
Sistemi di controllo fisiologici a feedback negativo
I meccanismi di regolazione a feedback negativo sono diffusissimi nell'organismo e mostrano diversi livelli organizzativi. Un ottimo esempio di meccanismo a feedback negativo è rappresentato dalla regolazione della temperatura, per via delle sue analogie con sistemi di regolazione molto noti (dai bagni termostatati dei laboratori ai sistemi di climatizzazione delle abitazioni e delle automobili). Nell'uomo, il set point della temperatura è circa 37 °C; le eventuali variazioni della temperatura interna vengono rilevate da neuroni termosensibili dell'ipotalamo, quelle della temperatura cutanea sono rilevate da recettori cutanei, e queste informazioni sono inviate a specifiche regioni ipotalamiche. I neuroni termosensibili e i recettori cutanei funzionano dunque da sensori. Il confronto tra il valore della temperatura misurata e quello corrispondente al set point genera un segnale errore, che attiva il controllore e innesca meccanismi che sono capaci di modificare sia la generazione di calore da parte dei tessuti sia la dispersione termica (agendo sull'irrorazione sanguigna e sulla sudorazione).
L'azione dei meccanismi effettori (del controllore) globalmente considerata ha sempre segno opposto a quello della variazione: se cioè la temperatura aumenta, l'effetto del sistema sarà una sua riduzione; se, viceversa, essa diminuisce, il sistema la riporterà a un valore molto vicino a quello del set point. È evidente che in un caso (quando il sistema aumenta la temperatura) il risultato sarà ottenuto aumentando la produzione di calore e diminuendo la sua dispersione, mentre nell'altro caso (quando il sistema diminuisce la temperatura) verrà ridotta la produzione e aumentata la dispersione. Il sistema funziona anche con altri valori del set point: nella febbre, per esempio, l'azione dei pirogeni può aumentare il valore del set point, per esempio a 38 °C. In questo caso, il sistema funziona come se in una persona normale la temperatura fosse di 36 °C; quindi aumenta la produzione di calore e ne riduce la dispersione: i brividi che precedono il raggiungimento del nuovo livello della temperatura non sono altro che l'espressione dell'attivazione di un meccanismo finalizzato ad aumentare la produzione di calore. Il sistema che regola la temperatura corporea dell'uomo è quindi un perfetto esempio di sistema di regolazione a feedback negativo.
Non tutti gli animali si comportano come l'uomo. Infatti, com'è noto, esistono animali in cui la produzione d'energia e la sua dispersione sono regolate (Uccelli e Mammiferi) e animali che non possiedono questi meccanismi (Pesci, Anfibi e Rettili); i primi sono detti 'omeotermi', i secondi 'pecilotermi'. In mancanza di meccanismi termoregolatori, la temperatura corporea dei pecilotermi è poco diversa da quella dell'ambiente in cui questi animali si trovano; poiché la temperatura influenza in maniera critica la velocità delle reazioni chimiche, è evidente che in un pecilotermo il metabolismo, e quindi tutte le funzioni dell'organismo, sono strettamente correlate alla temperatura ambientale, per cui l'animale dipende dall'ambiente (basta pensare all'immobilità di qualunque anfibio o rettile durante l'inverno). Gli omeotermi non sono invece dipendenti dall'ambiente: risulta così piuttosto chiaro il significato dell'affermazione bernardiana secondo cui la regolazione dell'ambiente interno è la condizione della vita 'libera e indipendente'. I meccanismi omeostatici hanno quindi un forte significato adattativo e conferiscono un indubbio vantaggio evolutivo.
L'entità della riduzione dell'errore provocato dalla perturbazione è determinata da un parametro definito 'guadagno' (o amplificazione), che stabilisce il grado d'efficienza con cui un sistema di controllo mantiene costanti le condizioni. L'azione del sistema dipende anche da altri parametri; così, nonostante il guadagno sia costante, tale azione può dipendere dalla frequenza o dal tempo. L'analisi delle prestazioni del sistema termoregolatorio durante l'esercizio fisico fornisce un ottimo esempio delle straordinarie capacità che un sistema di regolazione a feedback negativo può mettere in atto. Durante l'esercizio fisico, la produzione di calore aumenta circa venti volte rispetto alle condizioni di riposo, mentre l'aumento della temperatura corporea misurabile è di circa 1,5 °C. In assenza di sistemi di regolazione a feedback, l'aumento del gradiente di temperatura tra il nucleo e la temperatura sarebbe lineare e quindi venti volte superiore a quello misurabile in condizioni di riposo. Assumendo una temperatura ambientale di 27 °C, il gradiente tra temperatura del nucleo centrale e temperatura ambientale è 10 °C: poiché in queste condizioni l'esercizio fisico aumenterebbe la temperatura del nucleo a 210 °C, il gradiente diventa 200 °C. L'errore sarebbe quindi di 173°C (210−37). Poiché l'errore misurato è invece di 1,5 °C, ne consegue che il guadagno del sistema termoregolatorio è enorme e l'errore è inferiore all'1%. La relazione tra la riduzione dell'errore e il guadagno può essere espressa matematicamente. Elevati guadagni comportano tuttavia il rischio di generare instabilità nel sistema, soprattutto perché nei sistemi reali la correzione avviene dopo un certo intervallo di tempo e può quindi non essere più totalmente appropriata. In questi casi, la correzione stessa può diventare un disturbo e in casi di sistemi a elevato guadagno il disturbo può essere propagato nel sistema. Ne possono risultare la saturazione del sistema o, più spesso, la generazione di oscillazioni.
Grande importanza è stata sin qui attribuita al ruolo che in un sistema di regolazione a feedback negativo svolge il set point; nonostante ciò, è bene precisare che il valore di riferimento non deve intendersi in maniera rigida e che gli schemi generalmente utilizzati per descrivere i sistemi di controllo sono spesso semplicistici quando vengono confrontati con la complessità dei sistemi biologici. Di solito, infatti, il set point è rappresentato da un singolo segnale; nella realtà di molti sistemi biologici, invece, esso è la risultante di una complessa serie di operazioni che si svolgono in sistemi distribuiti in catene neuronali localizzate in varie strutture nervose. Ne consegue che il set point è a sua volta variabile nel tempo e soggetto a influenze. I sistemi di controllo in cui il set point non è costante, ma varia con il tempo, vengono detti 'servomeccanismi' e in questi casi l'entrata al controllore non viene più chiamata set point ma 'segnale comando'; molti sistemi regolatori omeostatici a feedback negativo sono in realtà dei servomeccanismi. Per esempio, durante l'esercizio fisico, le cellule muscolari attive consumano molto più O2 e hanno bisogno di un maggior apporto di sostanze nutritive. L'attivazione metabolica delle cellule muscolari determina una variazione del set point e questo permette che il sistema organismo mantenga le condizioni ottimali per il funzionamento di alcuni propri componenti, in questo caso delle cellule muscolari striate dei muscoli attivi.
Meccanismi dei sistemi di controllo a feedback negativo
I meccanismi omeostatici a feedback negativo sono mediati da semplici riflessi (per es., quelli che assicurano la costanza della pO2 o contribuiscono al mantenimento della pressione arteriosa sistemica) o da fenomeni ormonali (per es., quelli che regolano la glicemia o la calcemia). A volte, inoltre, anche il comportamento contribuisce all'omeostasi.
Meccanismi riflessi. - Nel caso dei meccanismi omeostatici a feedback negativo mediati da riflessi, l'analogia tra la struttura di un sistema di controllo e l'arco diastaltico di un riflesso appare evidente. Il sensore che rileva il valore della variabile controllata (la pressione parziale dell'O2 nel sangue arterioso [PaO2] o la pressione arteriosa nei due casi presi come esempio) è rappresentato da specifici recettori (i chemocettori dei glomi aortici e carotidei o i barocettori dei seni carotidei, rispettivamente); il controllore è costituito dall'insieme delle cellule e delle fibre nervose (e questo implica che il set point è un segnale distribuito) che ricevono il segnale dai recettori, lo elaborano e lo trasmettono come funzione forzante al sistema controllato (il sistema arterioso o quello respiratorio, rispettivamente, nei due esempi) per riportare il valore della variabile controllata verso i valori di riferimento. La maggior parte delle funzioni fondamentali dell'organismo è controllata da meccanismi riflessi che stabiliscono sistemi di controllo omeostatici a feedback negativo e, per converso, un'importante quota della funzione nervosa è finalizzata alla regolazione dei meccanismi vitali. I meccanismi riflessi che regolano le funzioni vitali dell'organismo sono mediati sia dalla componente simpatica sia da quella parasimpatica del sistema nervoso autonomo.
Meccanismi ormonali. - Anche nel caso dei meccanismi omeostatici mediati da ormoni si riconoscono facilmente i diversi componenti di un sistema di controllo. Il sensore è in questo caso rappresentato da recettori (nel senso di proteine recettrici della membrana plasmatica o intracellulari) e il controllore dalle vie di traduzione del segnale della stessa cellula, che aumenta o diminuisce la produzione di ormoni (le funzioni forzanti), i quali a loro volta aumentano o riducono la variabile controllata (in questo caso, la glicemia o la calcemia). In realtà, sia la regolazione della glicemia sia quella della calcemia non sono mediate da un solo sistema ormonale, ma da almeno due. Molte variabili di grande importanza sono regolate esclusivamente da sistemi ormonali. In numerori casi, tuttavia, alla regolazione di una variabile contribuiscono sia meccanismi nervosi sia meccanismi ormonali: un esempio è rappresentato della pressione arteriosa.
Meccanismi comportamentali. - In alcuni casi, come in quello dei meccanismi che regolano il volume idrico e le riserve energetiche, il comportamento contribuisce l'omeostasi, aggiungendosi ma non sostituendosi ai meccanismi riflessi e ormonali. La sete e la fame rientrano in questo tipo di comportamenti, definiti omeostatici, che sono essenziali alla sopravvivenza dell'individuo.
Eterogeneità dei circuiti a feedback negativo
I circuiti a feedback negativo descritti finora possono essere classificati come circuiti semplici, ovvero circuiti nei quali la variabile controllata viene rilevata da un sensore che attiva il controllore di quella variabile. Esistono tuttavia molti casi nei quali la variabile controllata viene rilevata da più di un sistema e l'output di ognuno di questi sistemi influenza più meccanismi capaci di vagliare la variabile controllata. Tali sistemi di controllo vengono definiti 'a circuiti multipli'; un esempio è rappresentato dai meccanismi che regolano la concentrazione plasmatica del calcio. Il calcio plasmatico viene rilevato sia dalle paratiroidi sia dalle cellule C della tiroide; entrambi questi gruppi cellulari secernono un ormone (il paratormone e la calcitonina, rispettivamente) che agisce direttamente su bersagli multipli (rene e tessuto osseo) e indirettamente su altre cellule bersaglio (quelle intestinali); ne consegue che la regolazione della calcemia è operata da vari meccanismi di controllo. Il significato di queste forme più complesse d'organizzazione dei circuiti regolatori non è noto: una possibilità è che almeno in certi casi, per esempio quello della regolazione di uno ione fondamentale come il Ca2+, i circuiti multipli servano a introdurre un certo grado di ridondanza, conferendo una maggiore sicurezza al sistema.
Interazioni tra meccanismi omeostatici
La complessità dei sistemi regolatori dell'organismo è resa evidente anche dall'esistenza di articolate interazioni tra di essi. Per interazioni tra meccanismi omeostatici s'intende la condizione in cui più sistemi di controllo inviano funzioni forzanti allo stesso sistema controllato (organo o tessuto). In questi casi, le diverse funzioni forzanti possono indurre gli stessi effetti sul sistema bersaglio o esercitare effetti opposti (competizione). Si consideri, per esempio, la situazione che si verifica durante l'esercizio fisico. Per aumentare il flusso sanguigno ai muscoli in attività, il sistema di controllo cardiovascolare impone una vasocostrizione diffusa che include anche i vasi cutanei. Parallelamente, l'aumento della produzione di calore da parte dei muscoli attivi determina un innalzamento della temperatura corporea; per aumentare la termodispersione, e quindi mantenere relativamente costante la temperatura corporea, il sistema di controllo termoregolatore genera segnali che impongono la vasodilatazione cutanea. Si crea così un'interazione competitiva tra due sistemi di regolazione omeostatica. In realtà, fino a quando non viene saturato l'insieme dei meccanismi capaci di aumentare il flusso sanguigno, le due diverse esigenze non sono in diretta competizione. Se tuttavia, per esempio durante l'esercizio strenuo, i meccanismi capaci di aumentare il flusso sanguigno sono prossimi ai loro limiti massimi, allora i due sistemi entrano in reale competizione, perché i muscoli richiedono più sangue e quindi si impone la vasocostrizione cutanea, mentre l'organismo ha necessità di disperdere l'eccesso di calore prodotto dai muscoli ricorrendo alla vasodilatazione cutanea: in questo caso, prevalgono le esigenze cardiovascolari che impongono la costrizione dei vasi cutanei, con conseguente aumento della temperatura corporea.
Omeostasi e controllo adattativo
Da quanto descritto emerge che i meccanismi omeostatici hanno un fondamentale significato adattativo, in quanto permettono il mantenimento dei parametri vitali entro limiti compatibili con il perfetto funzionamento dell'organismo anche in presenza di significative variazioni dell'ambiente esterno. La conoscenza di tali meccanismi ha inoltre un notevole significato clinico, sia sul piano applicativo (basti pensare al modo con il quale un parametro viene considerato normale o a come sia possibile risalire alle cause dell'alterazione di una qualunque funzione conoscendo i meccanismi che la regolano) sia su quello teorico (per es., per la definizione di normalità o di malattia).
I meccanismi omeostatici di regolazione, tuttavia, non esauriscono il ventaglio di meccanismi che permettono l'adattamento dell'organismo all'ambiente. Un esempio di controllo adattativo non basato sui classici meccanismi omeostatici a feedback è rappresentato dall'ipertrofia di un gruppo muscolare in risposta all'allenamento. In questo caso, è evidente che il principale elemento differenziale è da ricercare nel dominio temporale, solitamente breve nelle risposte omeostatiche ma significativamente più lungo per quanto riguarda l'ipertrofia.
Un altro esempio è rappresentato dalla degeneranza. Con tale termine s'intende la capacità di elementi biologici strutturalmente diversi di eseguire la stessa funzione (un concetto diverso da quello di ridondanza, in cui elementi identici eseguono la stessa funzione); gli esempi sono numerosi nel sistema nervoso centrale, nel sistema immunitario e, ad altri livelli, nel metabolismo e nei meccanismi genici (dove si ritiene possano spiegare perché, in circa il 30% dei casi, il fenotipo di animali knock out non risulti modificato). L'importanza dei meccanismi degeneranti risiede nel fatto che essi sono di tipo selettivo, una caratteristica che li rende estremamente adatti a fronteggiare modificazioni non previste dell'ambiente. All'adattamento contribuiscono anche meccanismi che invece di ripristinare il valore di una data variabile tendono a modificarla. Si è detto in precedenza dei sistemi allostatici, ossia di sistemi a feedforward finalizzati alla modificazione anticipata dello stato di un sistema e quindi di una sua variabile controllata. È evidente che i sistemi allostatici, e in genere qualunque sistema caratterizzato dalla possibilità di anticipare gli effetti di una perturbazione, devono possedere un'elevata capacità computazionale, la possibilità di valutare la qualità della risposta e soprattutto di confrontarla con quelle ottenute in occasioni precedenti: questi sistemi devono in altre parole essere capaci di apprendimento (→ Apprendimento. Basi biologiche dell'apprendimento e Apprendimento. Basi molecolari dell'apprendimento). È intuitivo che un sistema capace di apprendimento abbia maggiori possibilità adattative, e che un organismo più ricettivo sia capace di adattarsi meglio alle mutevoli condizioni dell'ambiente.
Bibliografia
Adolph 1961: Adolph, Edward F., Early concepts of physiological regulations, "Physiological reviews", 41, 1961, pp. 737-770.
Ashby 1956: Ashby, William R., An introduction to cybernetics, London, Chapman & Hall, 1956.
Bernard 1878-1879: Bernard, Claude, Leçons sur les phénomènes de la vie communs aux animaux et végétaux, Paris, Baillière, 1878-1879.
Canguilhem 2003: Canguilhem, Georges, Le normal et le pathologique, Paris, Presses Universitaires de France, 2003.
Cannon 1929: Cannon, Walter B., Organization for physiological homeostasis, "Physiological reviews", 9, 1929, pp. 399-427.
Carpenter 2004: Carpenter, Roger H., Homeostasis: a plea for a unified approach, "Advances in physiology education", 28, 2004, pp. 180-187.
Conti 2001: Conti, Fiorenzo, Claude Bernard: primer of the second biomedical revolution, "Nature reviews. Molecular cell biology", 2, 2001, pp. 703-708.
Conti 2005: Conti, Fiorenzo, Omeostasi e sistemi fisiologici di regolazione e controllo, in: Fisiologia medica, a cura di Fiorenzo Conti, Milano, Edi-Ermes, 2005.
Edelman, Gally 2001: Edelman, Gerald M. - Gally, Joseph A., Degeneracy and complexity in biological systems, "Proceedings of the National Academy of Sciences USA", 98, 2001, pp. 13763-13768.
Grmek 1997: Grmek, Mirko D., Le legs de Claude Bernard, Paris, Fayard, 1997.
Hochachka, Somero 2002: Hochachka, Peter W. - Somero, George N., Biochemical adaptation. Mechanism and process in physiological evolution, New York, Oxford University Press, 2002.
Holmes 1967: Holmes, Frederic L., Origins of the concept of the milieu intérieur, in: Claude Bernard and experimental medicine, edited by Francisco Grande and Maurice B. Visscher, Cambridge (Mass.), Schenkman, 1967, pp. 179-191.
Langley 1965: Langley, Leroy L., Homeostasis, New York, Reinhold, 1965.
Noble 2002: Noble, Denis, Modeling the heart - from genes to cells to the whole organ, "Science", 295, 2002, pp. 1678-1682.
Schulkin 2003: Schulkin, Jay, Rethinking homeostasis. Allostatic regulation in physiology and pathophysiology, Cambridge (Mass.), MIT Press, 2003.
Wiener 1953: Wiener, Norbert, La cibernetica, Milano, Bompiani, 1953.