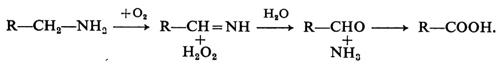Sistema nervoso autonomo
Sistema nervoso autonomo
di Ulf S. von Euler e Alberto Cangiano
Sistema nervoso autonomo
sommario: 1. Organizzazione generale: a) il sistema parasimpatico; b) il sistema simpatico; c) distribuzione dei nervi del sistema autonomo; d) caratteristiche funzionali dei nervi del sistema autonomo. 2. I neurotrasmettitori del sistema autonomo: a) acetilcolina; b) noradrenalina; c) altri neurotrasmettitori; d) analisi. 3. Liberazione dei neurotrasmettitori alle terminazioni nervose: a) fibre colinergiche; b) fibre adrenergiche; c) proprietà delle particelle adrenergiche di deposito; d) interazione con le prostaglandine; e) falsi trasmettitori; f) liberazione del trasmettitore causata da fattori diversi dagli impulsi nervosi. 4. Inattivazione del trasmettitore dopo la sua liberazione: a) sistema parasimpatico; b) sistema simpatico. 5. Aspetti generali degli effetti della stimolazione dei nervi del sistema autonomo: a) azioni eccitatorie e inibitorie; b) recettori α e β; c) natura dei recettori α e β e del meccanismo d'azione del trasmettitore; d) frequenza di stimolazione e suo effetto; tono parasimpatico e simpatico; e) ipersensibilità da denervazione. 6. Effetti specifici dei nervi autonomi sui vari organi: a) sistema cardio vascolare; b) occhio; c) sistema gastrointestinale; d) polmoni. 7. Valutazione dell'attività dei nervi del sistema autonomo. 8. Midollare del surrene e cellule cromaffini: a) ormoni della midollare del surrene; b) funzione degli ormoni della midollare del surrene; c) secrezione della midollare del surrene; d) meccanismo di liberazione. 9. Funzioni centrali del sistema autonomo: a) funzioni autonome dei centri dell'ipotalamo e di altre parti del cervello; b) funzioni centrali dei neuroni monoamminergici. 10. Farmacologia del sistema autonomo: a) sistema parasimpatico; b) sistema simpatico; c) farmaci nicotinici. 11. Controllo dello sviluppo del sistema autonomo: a) introduzione; b) sviluppo embrionale; c) sviluppo postnatale; d) Nerve Growth Factor (NGF). □ Bibliografia.
1. Organizzazione generale
Il sistema nervoso autonomo rappresenta una parte del sistema nervoso, distinta sia dal punto di vista anatomico che funzionale. Storicamente tale distinzione risale al Bichat, che verso il 1800 distinse tra la vie animale e la vie végétative, corrispondenti alla vie de relation e la vie de nutrition. Il sistema nervoso autonomo, spesso chiamato sistema nervoso vegetativo, da un punto di vista anatomico è caratterizzato da una speciale organizzazione dei suoi nervi, che consiste nell'accoppiamento di due neuroni, comprendente i nervi pregangliari e quelli postgangliari, collegati per mezzo di sinapsi. Un'osservazione importante ai fini della comprensione di tale principio fu fatta allorquando J. N. Langley trovò che l'alcaloide nicotina causava un'interruzione della conduzione tra i neuroni pre- e postgangliari. In tal modo fu possibile scoprire dove erano localizzate le connessioni sinaptiche tra i due tipi di neuroni e avere un'idea dell'organizzazione generale del sistema nervoso autonomo. Fu anche notata la somiglianza fra l'azione dell'ormone della midollare del surrene, l'adrenalina, a quel tempo appena scoperta, e l'effetto della stimolazione di un gruppo di nervi autonomi, i cosiddetti nervi simpatici. Tali osservazioni offrirono una base che permise di dividere il sistema nervoso autonomo in due parti diverse sia sul piano anatomico che funzionale, cioè il sistema simpatico e il sistema parasimpatico. Quest'ultimo fu distinto in una parte craniale o tettale e in una bulbosacrale. Langley considerò come un'entità distinta anche il sistema nervoso autonomo dei tratti gastrointestinali, che chiamò sistema enterico.
In generale il sistema nervoso autonomo, mantenendo l'omeostasi interna, esercita il controllo integrato e il coordinamento delle numerose funzioni che consentono all'organismo di agire come un tutto unico. Esso dunque controlla la temperatura del corpo, che determina la velocità di ogni reazione chimica, regola la circolazione del sangue a una pressione adeguata e la gettata cardiaca secondo le esigenze metaboliche dell'organismo, mantiene l'equilibrio idrico e controlla i movimenti intestinali e le secrezioni ghiandolari. Inoltre regola la secrezione di vari ormoni che sono importanti per l'escrezione dei prodotti di rifiuto, la riproduzione, il comportamento e altre funzioni.
Per espletare tutte queste funzioni il sistema nervoso autonomo deve avere appropriate connessioni locali con la maggior parte delle cellule e dei tessuti e anche con varie parti del sistema nervoso centrale. I principali centri di controllo del sistema autonomo sono localizzati nell'ipotalamo e nel tronco dell'encefalo, dove si riuniscono e si collegano fra loro i centri per l'assunzione di cibo e di liquidi, per il sonno, per la regolazione dei liquidi, per la circolazione, per la temperatura e per altre funzioni. Altre parti del cervello, come la corteccia cerebrale, hanno connessioni nervose con i centri ipotalamici, così che gli impulsi che da essi provengono possono raggiungere il sistema autonomo e influenzare le sue funzioni.
a) Il sistema parasimpatico
Il sistema parasimpatico è formato da una porzione craniale e da una sacrale. Le porzioni craniali del sistema parasimpatico sono rappresentate dai nuclei del terzo, settimo, nono e decimo nervo encefalico, dai quali le fibre nervose passano alla periferia. I centri spinali sono localizzati nella porzione sacrale del midollo spinale. Da un punto di vista quantitativo il nervo parasimpatico più importante è il vago, che innerva la regione toracica e una vasta porzione della regione addominale. Tuttavia nel vago decorrono pure alcune fibre nervose che vanno ai muscoli scheletrici volontari della faringe e della laringe, e vi si trovano anche alcune fibre simpatiche pregangliari che vanno al cuore. Gli organi che ricevono la loro innervazione parasimpatica attraverso il vago sono: il cuore e i polmoni (i bronchi), l'esofago, lo stomaco, il piccolo intestino e la metà prossimale del grosso intestino, il fegato e il pancreas, la porzione prossimale degli ureteri.
Anche lungo il terzo nervo encefalico (oculomotore) decorrono fibre parasimpatiche che vanno ai muscoli ciliari e agli sfinteri pupillari. Nel settimo nervo encefalico (facciale), le fibre si dirigono alle ghiandole lacrimali e nasali e alle ghiandole salivari sottomascellare e sottolinguale. La ghiandola parotide riceve la sua innervazione dal nono nervo encefalico (glossofaringeo).
I nervi parasimpatici della regione sacrale sono rappresentati dai nervi erigendi, i quali mandano fibre alla porzione distale del colon e al retto, come pure alla vescica urinaria e alla porzione inferiore degli ureteri. L'apparato genitale esterno è innervato da fibre della stessa provenienza.
Nel sistema parasimpatico le fibre pregangliari, di regola, decorrono senza interrompersi fino ai vari organi e formano le loro connessioni sinaptiche in stretta vicinanza con questi o persino dentro l'organo stesso. Per questa ragione le fibre postgangliari sono di norma piuttosto corte; le fibre simpatiche postgangliari, invece, nella maggior parte dei casi hanno origine da gangli che sono localizzati al di fuori degli organi. Solo in pochi casi i nervi postgangliari parasimpatici sono di lunghezza tale da formare un nervo anatomicamente separato, per esempio dal ganglio otico alla ghiandola parotide e dal ganglio ciliare all'occhio.
b) Il sistema simpatico
Il sistema simpatico ha una rappresentazione piuttosto ampia nel cervello, come dimostrato dalle tecniche istochimiche che permettono di identificare i nervi simpatici mediante la fluorescenza che emettono a seguito del trattamento dei tessuti con vapori di formaldeide (v. Falck, 1962). Queste parti cerebrali sono connesse con la porzione spinale che è localizzata nelle corna laterali del midollo spinale tra i segmenti T1 e L1. Le fibre pregangliari, mieliniche, emergono dal midollo spinale attraverso le radici ventrali e procedono nei rami comunicanti bianchi verso le catene simpatiche che sono localizzate, una per lato, immediatamente al di fuori e di fronte alla colonna vertebrale. Una gran parte di queste fibre forma connessioni o sinapsi con i neuroni postgangliari della catena simpatica. Le sinapsi sono disposte in maniera segmentale in una serie di gangli, dai quali le fibre postsinaptiche simpatiche, che sono amieliniche, passano ai nervi spinali misti, formati da fibre afferenti ed efferenti, che si trovano vicino alla colonna vertebrale, e procedono insieme con i tronchi nervosi misti verso la periferia. Qui essi si separano dai nervi motori o sensitivi e raggiungono le cellule muscolari lisce, le cellule adipose, o le cellule ghiandolari. Siccome le fibre postgangliari sono molto sottili, possono essere presenti in grande numero e formare circa l'8% delle fibre dei nervi misti. Tuttavia, alcune fibre simpatiche pregangliari passano attraverso la catena simpatica e vanno, attraverso i nervi splancnici, verso speciali gangli più grandi, i cosiddetti gangli prevertebrali, situati nella cavità addominale. I gangli prevertebrali maggiori sono il ganglio celiaco e i gangli mesenterici: il primo è la stazione sinaptica delle fibre che vanno a un certo numero di visceri come il fegato, la milza, lo stomaco, il pancreas e il rene; gli altri inviano fibre alla porzione inferiore dell'intestino e alla vescica. Gli organi della riproduzione ricevono la loro innervazione simpatica attraverso il nervo ipogastrico, che si connette con le fibre postgangliari in vicinanza degli organi.
Nel collo i gangli cervicali della catena simpatica sono le stazioni sinaptiche delle fibre che vanno all'occhio, alle ghiandole salivari, alla pelle della faccia e della testa, al cuore.
In generale le sinapsi sono localizzate piuttosto centralmente, e pertanto le fibre postgangliari possono avere una considerevole lunghezza. Un'eccezione è rappresentata dall'innervazione degli organi della riproduzione: infatti i nervi postgangliari sono, in questo caso, corti e sono diversi anche per altri aspetti.
Nel caso dei nervi soprarenali, le fibre pregangliari innervano le cellule cromaffini della midollare del surrene, che possono essere considerate come omologhe dei neuroni gangliari. Ad esempio esse possono anche avere durante la vita embrionale delle estensioni assonali costituenti una specie di fibre nervose. Questo fenomeno può essere osservato anche dopo trapianto di cellule cromaffini nella camera anteriore dell'occhio e, dopo trattamento con Nerve Growth Factor (v. cap. 11), nella midollare surrenale in situ (v. Abe e Levi-Montalcini, 1979). L'affinità delle cellule cromaffini con i neuroni è dimostrata anche dal fatto che esse, pur essendo normalmente sprovviste di prolungamenti cellulari, sono dotate del meccanismo del potenziale d'azione (v. Brandt e altri, 1976).
c) Distribuzione dei nervi del sistema autonomo
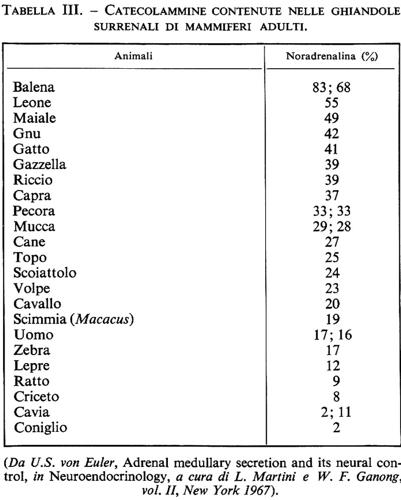
Il piccolo diametro e la mancanza di caratteri particolari dei nervi postgangliari rendono difficile costruire una mappa della loro distribuzione alla periferia. Per mezzo della tecnica istochimica di Falck e Hillarp (v. Falck, 1962) si può far sì che la noradrenalina che si trova nelle fibre adrenergiche divenga fortemente fluorescente, rendendole così visibili e facilmente identificabili. Dalle fotografie dei preparati fluorescenti è possibile ottenere una misura relativa delle fibre adrenergiche che innervano un organo o una porzione di Organo. I risultati così ottenuti sono in buon accordo con quelli ricavati dall'analisi chimica del contenuto di noradrenalina degli organi. Come illustrato dalla tab. I, si osservano notevoli variazioni nell'innervazione adrenergica dei diversi Organi. Così, il cuore e la milza, come pure le ghiandole salivari, in genere contengono 1-2 μg di noradrenalina per g di tessuto, mentre il polmone possiede solo 1/10 di questa quantità e il muscolo scheletrico ancora meno. Un contrasto particolarmente evidente si osserva negli organi genitali maschili; infatti il testicolo è quasi privo di noradrenalina, mentre il suo dotto efferente, il vas deferens, in molti animali ne contiene circa 10 μg per g. Quest'ultimo è l'organo che riceve la più ricca innervazione adrenergica, il che dà una misura dell'importanza di questa innervazione ai fini delle sue vigorose contrazioni. In generale si può postulare che la notevole variazione che esiste nell'innervazione dei diversi organi rifletta la necessità funzionale di questo tipo di innervazione, particolarmente per il letto vascolare.
Il sistema parasimpatico non può essere visualizzato così prontamente. Come già ricordato, le sottili fibre postgangliari sono in genere molto brevi. Il loro neurotrasmettitore specifico non è di per sé utilizzabile per una reazione di identificazione; tuttavia l'acetilcolina (ACh) è in genere presente con un enzima che la inattiva, l'acetilcolinesterasi, che può essere usato, dopo trattamento con inibitori specifici, per una reazione istochimica, basata sulla formazione di un composto rame-tiocolina a livello della membrana dell'assone.
L'analisi dei nervi parasimpatici mostra che questi contengono una considerevole quantità di acetilcolina, come prevedibile. Questo, tuttavia, non può essere considerato un infallibile indizio della presenza di un'innervazione colinergica, dal momento che alcuni organi, come la milza del cavallo e la placenta (che non ha innervazione), contengono quantità relativamente grandi di acetilcolina.
d) Caratteristiche funzionali dei nervi del sistema autonomo
Nel 1846 i fratelli E. ed E. H. Weber scoprirono che la stimolazione elettrica dei nervi vaghi nel collo provocava l'arresto del cuore. Più tardi fu dimostrato che la stimolazione delle fibre simpatiche che vanno al cuore causava un'accelerazione e un rinforzo del battito cardiaco. Dopo la scoperta, nel 1895, dell'azione esercitata da estratti di midollare sul sistema cardiovascolare, gradualmente si sviluppò il concetto che i nervi del sistema autonomo potessero agire liberando una piccola quantità di una sostanza la cui azione era simile all'azione stimolante dell'adrenalina e a quella inibitoria dell'acetilcolina che, come era stato scoperto, imitavano l'azione rispettivamente del simpatico e del vago. I classici esperimenti di Loewi (v., 1921) fornirono la prova definitiva della correttezza di questo concetto. Loewi dimostrò che, se il liquido di perfusione di un cuore isolato di rana prelevato durante la stimolazione del vago veniva trasferito a un secondo cuore, questo veniva inibito o cessava di battere; la stimolazione simpatica, d'altra parte, liberava un agente che accelerava il secondo cuore.
La natura del neurotrasmettitore chimico fu successivamente chiarita. Nel caso di stimolazione del vago e anche di altri nervi parasimpatici l'agente attivo ha le proprietà dell'acetilcolina. Negli esperimenti di Loewi sul cuore di rana il trasmettitore accelerante fu mostrato essere l'adrenalina, come postulato originariamente, sebbene questo costituisca un'eccezione. Nei Mammiferi e nella maggior parte degli altri animali il neurotrasmettitore è la noradrenalina, che è l'analogo non metilato dell'adrenalina.
La scoperta della natura dei due neurotrasmettitori nei sistemi simpatico e parasimpatico ha fatto avanzare enormemente la nostra conoscenza circa le loro funzioni, e ha anche creato una solida base per l'uso di farmaci intesi a modificare l'attività di questi sistemi.
Dopo la dimostrazione che le fibre del sistema autonomo agiscono liberando i mediatori chimici noradrenalina e acetilcolina, è stato proposto di chiamare le fibre col nome della loro sostanza trasmettitrice, e cioè fibre adrenergiche e colinergiche (v. Dale, 1934), anche perché le fibre pregangliari in ambedue i sistemi sono colinergiche. Il neurotrasmettitore pregangliare, l'acetilcolina, attiva quindi la fibra postgangliare ed evoca impulsi nervosi che si dirigono alle parti terminali delle fibre postgangliari provocando la liberazione del trasmettitore specifico.
2. I neurotrasmettitori del sistema autonomo
a) Acetilcolina
L'acetilcolina è essenzialmente un derivato dello ione tetrametilammonio, e ha azione sia nicotinica sia muscarinica. Nel 1914 Dale trovò nell'estratto di segale cornuta una sostanza che agiva come la muscarina e che egli riuscì a identificare come acetilcolina, sostanza sintetizzata diversi anni prima: le azioni dell'acetilcolina e della stimolazione del vago erano simili; inoltre, ambedue gli effetti erano bloccati dall'atropina ed erano particolarmente labili. Nel 1921 Loewi dimostrò che la stimolazione del vago nel cuore di rana portava alla liberazione, nel liquido di perfusione, di una sostanza che agiva come l'acetilcolina.
Di grande importanza per l'identificazione del neurotrasmettitore colinergico fu la scoperta che il suo effetto era fortemente rinforzato e prolungato dall'alcaloide fisostigmina (eserina).
L'acetilcolina, che ha peso molecolare 146,2, ha la seguente formula:
Questa sostanza si trova nei nervi colinergici postgangliari, come i corti nervi ciliari, in quantità di 3-8 μg per g, che sono pressappoco le stesse riscontrate nei nervi pregangliari. Piccole quantità di acetilcolina si trovano anche nei nervi adrenergici (v. anche cap. II, § b). Sembra ormai provato che l'acetilcolina presente nei nervi colinergici è immagazzinata in particelle subcellulari (vescicole a contenuto chiaro, a differenza delle vescicole granulari adrenergiche) di tipo simile a quelle che si trovano nei sinaptosomi del cervello e nei nervi motori che vanno ai muscoli scheletrici. Come la noradrenalina, l'acetilcolina forma con i fosfolipidi un complesso solubile in etere.
La biosintesi dell'acetilcolina avviene nelle terminazioni degli assoni con l'aiuto di un enzima, la colinoacetilasi, che catalizza la reazione tra colina e acetato attivo, quest'ultimo in forma di acetilcoenzima A (v. Nachmansohn e Machado, 1943). L'enzima che serve per la sintesi ha origine nel corpo cellulare e scende lungo l'assone verso la periferia.
Tra gli inibitori della sintesi dell'acetilcolina, il cosiddetto emicolinio (HC-3) riduce la produzione del trasmettitore; in dosi più alte l'HC-3 causa paralisi neuromuscolare. Si ritiene che l'HC-3 competa con l'acetilcolina per i siti di legame nei depositi, impedendo in tal modo che si ricostituiscano le scorte di trasmettitore. L'effetto dell'HC-3 può essere efficacemente prevenuto mediante somministrazione di colina. Dal momento che l'HC-3 ha proprietà simili a quelle della tossina botulinica, si ritiene che esso agisca prima della giunzione.
Anche il trietil-analogo della colina ha proprietà emicolinio-simili ed è stato ipotizzato che possa agire, dopo acetilazione, come un ‛falso trasmettitore'. Lo ione tetraetilammonio inibisce anch'esso la sintesi dell'acetilcolina nei gangli, ma questa azione è contrastata dalla colina.
b) Noradrenalina
La noradrenalina è sintetizzata nei neuroni adrenergici a partire dalla tirosina, che è idrossilata a diidrossifenilalanina (dopa) mediante l'enzima tirosinaidrossilasi. Questo composto viene decarbossilato dall'enzima 1-amminoacido-decarbossilasi a dopammina, trasformata a sua volta in noradrenalina da un enzima, dopammina-β-idrossilasi, che si trova nelle vescicole di deposito come parte delle proteine della membrana.
La noradrenalina fu ottenuta per sintesi chimica nel 1904 e più tardi identificata con il neurotrasmettitore adrenergico (v. von Euler, 1946). Chimicamente la noradrenalina è un'ammina primaria di peso molecolare 169,2 che può esistere in due enantiomeri; la forma naturale è la levogira. La sua configurazione assoluta corrisponde alla D(−)-noradrenalina. Viene prontamente ossidata in mezzo alcalino e con tracce di ioni metallici; con iodio essa forma un composto rosso, iodonoradrenocromo, che può essere usato a scopo di saggio analitico. Le forme (+) e (−) possono essere separate in base alla diversa solubilità dei bitartrati.
La biosintesi è regolata da un sistema a retroazione che opera mediante i prodotti formati. Dunque la noradrenalina e la dopammina inibiscono l'azione della tirosinaidrossilasi, che è lo stadio che limita la velocità della sintesi. Per l'inibizione della sintesi con farmaci si veda il cap. 10, § b, 2.
c) Altri neurotrasmettitori
Benché i trasmettitori principali siano l'acetilcolina per il parasimpatico e la noradrenalina per il simpatico, è stato dimostrato che anche altri composti hanno la funzione di trasmettitore nel sistema autonomo.
La dopammina, immediato precursore della noradrenalina, ha funzione di trasmettitore in almeno tre sistemi di vie nel sistema nervoso centrale (v. cap. 9, § b). Per quanto concerne il sistema nervoso periferico, si è trovato che la dopammina agisce come trasmettitore dell'azione sinaptica di un interneurone situato nei gangli simpatici. Nel ganglio cervicale superiore, ad esempio, gli assoni pregangliari colinergici, oltre a eccitare i neuroni postgangliari attraverso recettori nicotinici e muscarinici, vanno ad attivare un interneurone (mediante sinapsi muscariniche): questo a sua volta libera dopammina, che inibisce il neurone postgangliare. Tale inibizione è dovuta a iperpolarizzazione (PPSI-I) ed è mediata da un aumento dell'AMP ciclico, secondo il meccanismo del ‛secondo messaggero' che sarà esposto dettagliatamente nel cap. 5, § c. Benché il neurone pregangliare abbia un'azione principalmente eccitatoria su quello postgangliare (al fine di trasmettere l'impulso nervoso), esso può anche modulare tale azione attraverso l'interneurone dopamminergico inibitorio.
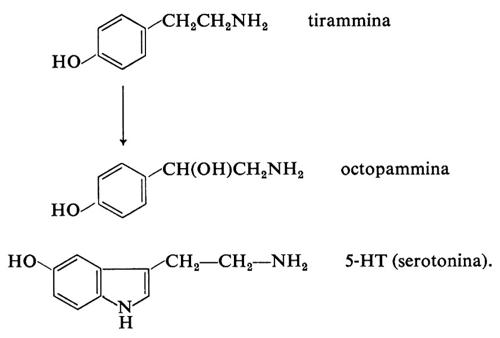
L'adrenalina, oltre a essere secreta come ormone della midollare surrenale, è anche il mediatore chimico di alcune vie nel sistema nervoso centrale (v. cap. 5, § b). In certi animali (rana, rospo) è l'adrenalina che funge da trasmettitore, invece della noradrenalina. In alcune parti dell'encefalo il metodo dell'istofluorescenza ha rivelato la presenza di neuroni contenenti S-idrossitriptammina (5-HT o serotonina), che agisce qui come trasmettitore (v. cap. 9, § b). Si pensa anche che la 5-HT abbia funzione di neurotrasmettitore nel tubo digerente, dove forse medierebbe la trasmissione sinaptica tra neurone afferente ed efferente del riflesso intramurale mienterico (contrazione locale da distensione). L'octopammina, il prodotto β-idrossiderivato della tirammina, ha funzione di trasmettitore in Octopus e probabilmente in altri animali. Le formule chimiche della tirammina, dell' octopammina e della 5-HT sono le seguenti:
Un terzo componente del sistema autonomo, oltre ai due classici colinergico e adrenergico, è stato messo in evidenza particolarmente nell'apparato digerente. Esso è costituito da neuroni postgangliari nè adrenergici, nè colinergici: poiché vi sono buone prove che essi liberino un nucleotide purinico, molto probabilmente l'ATP, sono stati chiamati ‛punnergici' (v. Burnstock, 1972). L'ATP viene liberato a livello di alcune giunzioni neuromuscolari del muscolo liscio del tubo digerente, dove produce inibizione dovuta a iperpolarizzazione da aumento della conduttanza di membrana allo ione potassio. Un esempio è dato dall'inibizione della motilità gastrica in risposta alla stimolazione vagale, che non è bloccata nè dall'atropina nè da farmaci che antagonizzano l'azione dei nervi simpatici. Tuttavia i neuroni purinergici sono presenti in tutto il tratto gastrointestinale, e sembrano inoltre innervare la trachea, i polmoni, la vescica e parti dell'apparato cardiovascolare. È stato anche proposto che siano i nervi ‛purinergici' piuttosto che quelli adrenergici a costituire il principale sistema inibitorio antagonistico a quello eccitatorio colinergico, durante la propulsione del bolo alimentare attraverso il tubo digerente. Ad esempio, alcuni dati suggeriscono che essi siano coinvolti nel rilasciamento riflesso dello sfintere gastro-esofageo, nel ‛rilasciamento recettivo' dello stomaco, nella fase di ‛inibizione discendente' della peristalsi (che non è influenzata dalla denervazione simpatica) e nel rilasciamento riflesso dello sfintere anale.
È stato infine scoperto in questi ultimi anni che molti polipeptidi agiscono probabilmente come neurotrasmettitori in varie parti del sistema nervoso sia centrale che periferico, incluso il sistema autonomo. Il grande fiorire di queste ricerche è essenzialmente dovuto all'introduzione delle tecniche immunologiche nella visualizzazione di diversi tipi di composti nel tessuto nervoso (e in altri tessuti); questo indirizzo di studi ha preso il nome di immunoistochimica. Trattando sezioni di tessuto nervoso con anticorpi preparati contro vari peptidi (previamente coniugati con proteine per renderli antigenici) e resi visibili con traccianti fluorescenti (immunofluorescenza) o di altro tipo, è possibile marcare vari neuroni e dimostrare così la presenza in tali cellule di un particolare peptide. La lista dei peptidi che possono essere considerati candidati trasmettitori ha ormai oltrepassato la ventina. Molti peptidi ora identificati nel tessuto nervoso erano già conosciuti come ormoni: ormoni dell'apparato digerente quali gastrina, colecistochinina, VIP (vasoaclive intestinal polypeptide); l'angiotensina II; ormoni ipofisari quali ACTH (adrenocorticotropo), TSH (tirotropo) e STH (somatotropo); l'insulina; infine ormoni già noti come neurosecreti ipotalamici quali TRH (ormone liberante l'ormone tirotropo), LHRH (ormone liberante l'ormone luteinizzante), somatostatina o GIH (ormone inibente la liberazione dell'ormone somatotropo), ossitocina e vasopressina (v. ormoni nei vertebrati). Altri peptidi aventi una vasta distribuzione sono la sostanza P e le due encefaline, leucina-encefalina e metionina-encefalina (v. neuroendocrinologia; v. neurosecrezione).
Di particolare interesse è stata la scoperta di peptidi in neuroni che contengono anche un mediatore chimico ben noto, come l'acetilcolina, la noradrenalina, la dopammina e la serotonina. Esempi di questa coesistenza sono, per il sistema nervoso periferico, i seguenti: acetilcolina-VIP nei gangli autonomi e nelle ghiandole esocrine; noradrenalina-encefalina nel ganglio cervicale superiore; noradrenalina-somatostatina nella midollare surrenale; acetilcolina-LHRH nei gangli simpatici di rana; adrenalina-encefalina nella midollare surrenale. Per il sistema nervoso centrale, si possono citare: serotonina-sostanza P nel bulbo; serotonina-TRH ugualmente nel bulbo; dopammina-colecistochinina nelle aree d'origine delle vie dopamminergiche centrali (v. cap. 9, § b).
Il ruolo di neurotrasmettitore è per alcuni peptidi reso probabile da sufficienti dati sperimentali (ad esempio la sostanza P come trasmettitore centrale dei neuroni sensitivi primari); in altri casi, invece, è ancora solo ipotetico. Tali peptidi, d'altra parte, potrebbero avere, invece che il ruolo di trasmettitore, quello di modulatore, termine ancora non perfettamente precisato con cui s'intendono agenti che modificano la quantità di trasmettitore liberato da altre vie (agendo su recettori presinaptici sensibili al modulatore) o modificano la risposta delle cellule bersaglio a questi trasmettitori. I modulatori possono essere liberati anche a distanza dal luogo di azione.
Per quanto riguarda il sistema nervoso autonomo esistono già buone prove sperimentali che peptidi coesistenti in determinati neuroni assieme a un trasmettitore classico producono azioni postsinaptiche ben definite. Jan, Jan e Kuffler hanno recentemente portato prove che l'ormone LHRH è cotrasmettitore nei neuroni pregangliari dei gangli simpatici di rana, il cui trasmettitore classico è naturalmente l'acetilcolina. La stimolazione degli assoni pregangliari, infatti, oltre a produrre i potenziali sinaptici PPSE rapido, PPSI lento e PPSE lento produce anche un quarto potenziale sinaptico eccitatorio (PPSE) a carattere più tardivo e di durata molto maggiore degli altri (5-10 minuti). Kuffier e collaboratori hanno appunto mostrato che tutte le caratteristiche di questo PPSE lento e tardivo sono riproducibili mediante applicazione sui neuroni postgangliari dell'ormone LHRH (v. Jan e altri, 1980).
Un altro sistema ben studiato è quello costituito dai neuroni colinergici dei gangli simpatici che innervano le ghiandole sudoripare. Essi liberano, oltre all'acetilcolina (ACh), anche VIP, e studi recentissimi suggeriscono che la coesistenza di ACh e VIP sia un carattere generale dei neuroni autonomi che innervano le ghiandole esocrine. ACh e VIP liberati dalle stesse terminazioni agiscono sinergicamente nel produrre la secrezione, ma su cellule bersaglio diverse. L'ACh agisce direttamente sulle cellule secretorie (azione bloccata dall'atropina), il VIP invece indirettamente inducendo vasodilatazione (azione resistente all'atropina). (Per una rassegna sintetica sui peptidi neuronali v. Hökfelt e altri, Peptidergic..., 1980).
È giusto ricordare che le tecniche di immunoistochimica sopra descritte si sono rivelate recentemente molto utili anche per distinguere, nell'ambito dei neuroni contenenti catecolammine, i neuroni dopamminergici, quelli noradrenergici e quelli adrenergici. Questo è stato possibile appunto con l'immunoistochimica, utilizzando antisieri contro gli enzimi che operano il passaggio da tirosina a dopa (tirosinaidrossilasi: TH), da dopa a dopammina (dopadecarbossilasi: DDC), da dopammina a noradrenalina (dopammina-β-idrossilasi: DBH) e da noradrenalina ad adrenalina (feniletanolammina-N-metiltransferasi: PNMT). Così, una cellula adrenergica contiene tutti e quattro gli enzimi, mentre una cellula noradrenergica non possiede l'ultimo enzima (PNMT) e una cellula dopamminergica contiene solo i primi due (TH e DDC). Trattando sezioni consecutive con i vari antisieri e confrontando i risultati ottenuti, si può stabilire quale catecolammina una data cellula è in grado di produrre. Con questo metodo sono stati anche identificati neuroni dopamminergici, noradrenergici e adrenergici nell'encefalo (v. cap. 9, § b), ed è stato possibile mostrare che nella midollare surrenale vi sono cellule che producono adrenalina e altre che producono solo noradrenalina.
d) Analisi
1. Acetilcolina. - L'analisi biologica dell'acetilcolina negli estratti di tessuto è facilitata dal fatto che alcuni organi hanno un'alta sensibilità a questo composto. L'azione inibitoria sul cuore di rana, l'effetto contrattile sull'intestino isolato di molti animali, la contrazione del muscolo dorsale della sanguisuga o del retto addominale della rana possono essere usati a scopo analitico. Per differenziare questa azione da effetti simili di altri composti biologicamente attivi si utilizzano l'atropina o la iosciammina, che hanno effetto bloccante sull'azione muscarinica, oppure la fisostigmina (eserina) o la prostigmina, che hanno effetto facilitatorio.
La dimostrazione istochimica dell'acetilcolinesterasi con l'ausilio della tecnica con rame-tiocolina è spesso usata come un indicatore dell'acetilcolina, dal momento che l'enzima che porta all'idrolisi in genere si trova nelle zone dove viene liberata acetilcolina.
2. Noradrenalina. - La noradrenalina può essere saggiata biologicamente su diversi organi isolati, o sulla pressione sanguigna del gatto o del ratto: tale sistema permette la stima di quantità dell'ordine del nanogrammo. Si possono purificare estratti di tessuto con l'adsorbimento su allumina, che adsorbe selettivamente le catecolammine a pH 8,2, e con successiva eluizione con un acido.
Quando noradrenalina o adrenalina sono presenti in concentrazioni che eccedono 20 μg per ml, come succede spesso negli estratti surrenali, le due sostanze possono essere saggiate con metodo colorimetrico dopo trasformazione in uno iodocromo rosso. Per piccole quantità la tecnica fluorimetrica è quella usata più comunemente. Dopo ossidazione con ferricianuro, il noradrenocromo formato viene trasformato nel corrispondente triidrossindolo (noradrenolutina), che dà una forte fluorescenza con una lunghezza d'onda di attivazione di 395 nm e con un'emissione di 515 nm. Si può anche usare un metodo diretto spettrofotofluorimetrico.
Da miscugli la noradrenalina e l'adrenalina possono essere separate mediante cromatografia e saggiate separatamente. In molti casi il miscuglio può essere saggiato usando due tipi di saggi biologici con diversi rapporti di attività per la noradrenalina e l'adrenalina, per es. la pressione arteriosa del gatto e il cieco rettale del pulcino, oppure mediante due diversi tipi di filtri per la misura fluorimetrica. Dai dati ottenuti si possono calcolare rapidamente le quantità delle due ammine.
Dal momento che la noradrenalina viene in parte metabolizzata nel tessuto, debbono essere ulteriormente separati i composti catecolamminici eluiti dall'allumina e i derivati non catecolamminici, per poter determinare quantitativamente tutti i prodotti. A tal fine si può impiegare la cromatografia a scambio ionico.
3. Liberazione dei neurotrasmettitori alle terminazioni nervose
a) Fibre colinergiche
Le terminazioni nervose colinergiche contengono in grande quantità piccole vescicole, le cosiddette vescicole sinaptiche. Queste sono state in parte isolate ed è stato trovato che contengono acetilcolina sotto forma di legame complesso dal quale, mediante stimolazione del nervo, può essere liberata alle giunzioni sinaptiche nei gangli e nel sistema nervoso centrale e alle terminazioni delle fibre postgangliari colinergiche. L'entrata degli ioni calcio è il processo iniziale che provoca la liberazione del trasmettitore.
Il turnover dell'acetilcolina durante la stimolazione del nervo del ganglio cervicale superiore è stato valutato intorno al 10%, per minuto, della quantità a riposo. Sembra che l'acetilcolina di recente formazione sia liberata più prontamente, in seguito a stimolazione nervosa, di quella sotto forma di deposito. Dopo liberazione e idrolisi del trasmettitore a colina e acido acetico, circa metà della colina è ricaptata e utilizzata per una nuova sintesi. Sembra che la sintesi sia regolata dalla concentrazione intracellulare del trasmettitore, dal momento che il suo contenuto non può salire al di sopra di un certo livello, oppure che le capacità di deposito siano limitate.
b) Fibre adrenergiche
Le parti terminali delle fibre nervose adrenergiche mostrano una forma a rosario dovuta al periodico ripetersi di rigonfiamenti o varicosità (v. Hillarp, 1946) che, come mostrano le fotografie al microscopio elettronico, contengono un gran numero di piccole vescicole aventi un diametro da 0,03 a 0,15 μm. Queste vescicole, benché più piccole, hanno diverse caratteristiche in comune con quelle che si trovano nelle cellule cromaffini. Esse servono come deposito per la conservazione del trasmettitore e prendono parte alla fase finale della sintesi allo stesso modo delle vescicole delle cellule cromaffini (v. cap. 8).
Le vescicole di deposito di questo tipo si trovano lungo tutto il neurone adrenergico, dal corpo cellulare alle porzioni terminali, sebbene si accumulino in quest'ultima zona. Generalmente si ritiene che le vescicole siano formate dall'apparato di Golgi e che siano trasportate verso la periferia dal flusso assoplasmatico.
Le vescicole spesso mostrano una porzione centrale più densa alla microscopia elettronica (per questo sono chiamate vescicole granulari); in essa si pensa sia contenuto il neurotrasmettitore, che si colora in nero con l'acido osmico. Come risultato dell'impulso nervoso, la membrana dell'assone subisce un cambiamento che consiste in una breve temporanea alterazione della carica elettrica su ambedue i suoi lati (depolarizzazione). A causa di questo cambiamento gli ioni calcio entrano nella membrana e provocano la liberazione del trasmettitore, che diffonde al di fuori e raggiunge l'area recettrice delle cellule effettrici. Dal momento che i rigonfiamenti contengono il trasmettitore in forma legata, probabilmente in un complesso con altri elementi costituenti, esso deve essere dissociato nello stesso momento in cui si ha l'impulso nervoso. In genere i rigonfiamenti terminali formano una specie di giunzione sinaptica con la cellula effettrice, per esempio una cellula muscolare liscia, permettendo in tal modo che il trasmettitore liberato raggiunga il recettore quasi istantaneamente. Dopo la fine dell'impulso nervoso la membrana assonale si ripolarizza immediatamente e una parte del trasmettitore liberato è nuovamente captata dall'assone e, in certa misura, immagazzinata nelle vescicole.
Questa ricaptazione è considerata un fattore importante nell'economia del sistema di trasmissione e allo stesso tempo collabora nel far cessare l'azione del trasmettitore. Nel sistema colinergico il trasmettitore è normalmente scisso dall'azione idrolitica dell'acetilcolinesterasi che così termina l'azione del trasmettitore; in questo caso, tuttavia, una notevole parte della colina è captata e serve come precursore per la nuova sintesi.
Mentre è stato provato che le vescicole di deposito nelle cellule cromaffini scaricano la maggior parte del loro contenuto, compresi nucleotidi e proteine, direttamente nello spazio extracellulare, cosa che le rende incapaci di servire nuovamente come deposito, sembra che le vescicole dei nervi adrenergici liberino solo una piccola parte del loro contenuto oltre al trasmettitore stesso. Queste vescicole sono perciò capaci di captare e legare il trasmettitore ripetutamente, per ricattura del trasmettitore già liberato o della noradrenalina appena sintetizzata nella terminazione nervosa. Sembra pertanto che il processo di liberazione implichi un rilascio selettivo del trasmettitore sia dalle vescicole di deposito sia da un deposito secondario, probabilmente nella membrana dell'assone.
c) Proprietà delle particelle adrenergiche di deposito
Quando il nervo è stimolato, il trasmettitore adrenergico viene liberato dalle terminazioni nervose a una velocità che dipende dalla frequenza di stimolazione. Il trasmettitore viene accumulato principalmente nelle particelle di deposito, ma sembra che una frazione più piccola sia associata alla membrana dell'assone, dove si trova disponibile per l'immediata liberazione quando la membrana dell'assone è eccitata. Dopo la liberazione, questo piccolo deposito è continuamente riempito dai depositi delle vescicole e dal trasmettitore di recente sintesi. Entro certi limiti, la piccola riserva della membrana può anche captare il trasmettitore in eccesso già liberato. Dopo la liberazione, una parte del trasmettitore è inattivata da enzimi, un'altra parte è rimossa per diffusione e portata via dal sangue e dalla linfa, un'altra parte ancora e captata dalle cellule adiacenti, incluso l'assone dal quale è stato secreto. In questo modo l'azione viene terminata e allo stesso tempo parte del trasmettitore può essere riutilizzata.
La ricaptazione del trasmettitore può essere prevenuta efficacemente con un certo numero di farmaci, quali la cocaina, la demetilimiprammina, la fenossibenzammina, la protriptilina e altri. L'inibizione della ricaptazione provoca un aumento nella quantità del trasmettitore che si può recuperare nel sangue proveniente da quella zona. Sotto questo aspetto la fenossibenzammina è particolarmente attiva (v. cap. 10, § b, 6).
Le particelle di deposito presenti nei nervi adrenergici possono essere separate mediante omogeneizzazione dei nervi o del tessuto al quale arrivano questi nervi, e successiva rimozione del materiale più grossolano per centrifugazione differenziale, o mediante centrifugazione a gradiente di densità. Incubando le particelle in mezzi adatti, esse liberano il loro contenuto in noradrenalina a una velocità che dipende dalla temperatura, con un tempo di dimezzamento di circa 50 minuti a 20 °C e 5 minuti a 37 °C. A 0 °C la liberazione di noradrenalina è trascurabile e a 10 °C è molto lenta. In presenza di noradrenalina nel mezzo, la liberazione netta diminuisce in conseguenza della simultanea ricaptazione, e a una concentrazione di 10-4 M si ha equilibrio tra liberazione e ricaptazione.
La ricaptazione di noradrenalina è notevolmente facilitata dall'aggiunta di adenosin-5′-trifosfato (ATP) e di ioni magnesio. Dopo deplezione parziale delle particelle, per esempio incubando 10 minuti a 37 °C, esse possono captare noradrenalina se sottoposte a una nuova incubazione in presenza di ATP e Mg2+. L'adrenalina e alcune delle altre ammine simpaticomimetiche, come la α-metilnoradrenalina, l'isopropilnoradrenalina, il metaraminolo o l'octopammina, possono essere captate e conservate, competendo con la noradrenalina per i siti di deposito.
Un certo numero di farmaci ha effetto sulla liberazione e captazione di noradrenalina nelle particelle. Le ammine che agiscono indirettamente, come la tirammina, liberano il trasmettitore e inibiscono anche la sua captazione. La reserpina previene la captazione e porta, alla fine, allo svuotamento delle particelle. La nicotina e l'acetilcolina, che liberano il trasmettitore dai nervi, non hanno azione sulle particelle. D'altra parte un certo numero di inibitori metabolici inibiscono sia la liberazione sia la captazione della noradrenalina, e ciò suggerisce che questi processi siano regolati metabolicamente (v. cap. 10).
d) Interazione con le prostaglandine
È stato dimostrato che la stimolazione dei nervi simpatici provoca liberazione non solo di noradrenalina, ma anche di prostaglandine di tipo E (PGE). L'aggiunta di PGE al liquido che perfonde un organo isolato, come la milza o il cuore, diminuisce la fuoruscita del trasmettitore e inibisce la risposta dell'organo alla stimolazione del nervo simpatico. Pertanto si è ritenuto che la PGE agisca come un inibitore fisiologico della neurotrasmissione adrenergica. Questo concetto è sostenuto dai seguenti fatti: 1) il liquido di perfusione raccolto durante la stimolazione dei nervi simpatici che vanno al cuore provoca l'inibizione della secrezione del trasmettitore; 2) il fattore attivo mostra le caratteristiche chimiche della PGE. Se si previene la sintesi della PGE, nel cuore, l'azione inibitoria del liquido di perfusione raccolto durante la stimolazione nervosa scompare. L'azione inibitoria della PGE sulla liberazione del trasmettitore sembra essere associata con un'alterazione del trasporto degli ioni calcio ed è contrastata dall'aumento della concentrazione di calcio nel mezzo.
La liberazione di PGE conseguente alla stimolazione dei nervi adrenergici è prevenuta dalla fenossibenzammina. Perciò si è ritenuto che l'aumentata liberazione del trasmettitore che si verifica stimolando il nervo in presenza di questo farmaco sia dovuta alla scomparsa dell'effetto inibitore o frenante della PGE.
L'effetto inibitore della PGE sulla liberazione di trasmettitore è stato dimostrato anche nel caso del trasmettitore colinergico, l'acetilcolina. Nel cuore isolato e perfuso la PGE riduce pertanto l'effetto rallentante della stimolazione del vago.
e) Falsi trasmettitori
Normalmente i nervi adrenergici e le loro terminazioni contengono il neurotrasmettitore noradrenalina, che è continuamente sintetizzato e immagazzinato nelle specifiche particelle di deposito. L'analisi degli organi dopo un ‛iniezione di adrenalina, tuttavia, mostra che il contenuto di noradrenalina è diminuito ed è stato sostituito da un'equivalente quantità di adrenalina. Questo scambio è dovuto al fatto che le particelle di deposito sono capaci di captare e immagazzinare adrenalina nello stesso modo della noradrenalina. La quantità di noradrenalina sostituita dipende dalle concentrazioni relative delle due ammine che competono per i siti di deposito. La stimolazione del nervo provoca la liberazione dell'adrenalina dalle terminazioni nervose in maniera simile a quella della noradrenalina e perciò serve come ‛falso trasmettitore'. Dopo un po' di tempo la situazione ritorna gradualmente alla normalità, perché l'adrenalina liberata è ricaptata dalla membrana dell'assone meno prontamente della noradrenalina. Inoltre, la noradrenalina sintetizzata in continuazione si troverà in una concentrazione più favorevole e gradualmente rimpiazzerà l'adrenalina.
Anche altre ammine possono essere captate e immagazzinate nelle terminazioni nervose adrenergiche. Così la tirammina dopo β-idrossilazione a octopammina può prendere il posto della noradrenalina. Questo avviene in piccola parte anche normalmente. Se vengono somministrate le ammine α-metilnoradrenalina (Corbasil) e metaraminolo, anche queste vengono immagazzinate e possono essere liberate come ‛falsi trasmettitori'. Si è ritenuto che gli effetti terapeutici dell'α-metildopa nell'ipertensione siano in parte dovuti all'accumulo di α-metilnoradrenalina, che sostituisce parzialmente la noradrenalina nelle terminazioni nervose adrenergiche dopo decarbossilazione e β-idrossilazione del farmaco.
L'ammina isopropilnoradrenalina, che in linea di principio potrebbe servire come falso trasmettitore, se somministrata in vivo non agisce come tale a causa della sua incapacità di penetrare nella membrana dell'assone.
f) Liberazione del trasmettitore causata da fattori diversi dagli impulsi nervosi
Anche se poco si sa sulla liberazione di acetilcolina determinata da fattori non associati all'eccitazione nervosa, nel sistema adrenergico queste azioni hanno un notevole interesse sia teorico sia pratico.
Alcune ammine, simili alle catecolammine, esercitano azioni fisiologiche simili a quelle osservate per l'adrenalina o la noradrenalina (ammine simpaticomimetiche). Ad esempio, l'ammina monofenolica tirammina, che si forma dalla decarbossilazione della tirosina ed è comunemente presente nel materiale biologico, provoca effetti simili a quelli della noradrenalina, ed è stato provato che ciò dipende dalla liberazione del neurotrasmettitore adrenergico, in parte per scambio ai siti di deposito e in parte per inibizione della ricaptazione. In quest'ultimo caso il trasmettitore liberato sarà presente in concentrazione maggiore in vicinanza del recettore e così eserciterà un'azione più forte. Un effetto di liberazione dello stesso tipo si osserva con diverse ammine, principalmente la feniletilammina e l'amfetammina.
Normalmente una certa parte della tirammina, che raggiunge le fibre nervose adrenergiche ed è da queste captata, sarà inattivata nel nervo dall'enzima monoamminossidasi, presente nei mitocondri che si trovano sempre nei rigonfiamenti delle terminazioni nervose. Tuttavia, se questo enzima viene inibito, cosa che può essere ottenuta con alcuni farmaci antidepressivi come l'iproniazide, la nialammide e altri, la tirammina può avere effetti rilevanti liberando noradrenalina. Dato che la tirammina è presente in gran quantità in alcuni cibi, come per esempio in vari tipi di formaggio o in alcuni vini (Chianti), l'effetto dell'inibitore della MAO può essere rischioso, in quanto può stimolare il cuore e determinare un innalzamento della pressione arteriosa.
4. Inattivazione del trasmettitore dopo la sua liberazione
a) Sistema parasimpatico
Un problema di importanza biologica generale è rappresentato dal modo in cui l'azione prodotta da un trasmettitore chimico viene a cessare. Per quanto concerne i rapidi spostamenti necessari nei movimenti muscolari, spesso si richiede una cessazione immediata dell'attività dell'acetilcolina, che è attuata grazie alla presenza quasi ubiquitaria di un enzima idrolizzante, l'acetilcolinesterasi (AChE), capace di scindere il trasmettitore acetilcolina in colina, che ha un'azione debole, e acido acetico. Questa reazione avviene ad alta velocità, e perciò l'azione del trasmettitore viene meno, in pratica, immediatamente dopo che l'impulso nervoso è terminato. L'AChE è presente in tutti i siti in cui viene liberata ACh, cioè vicino a tutte le terminazioni nervose che appartengono al sistema motorio e anche al sistema autonomo, nelle aree sinaptiche e ai siti postgiunzionali, dove terminano le fibre colinergiche postgangliari e cioè nel cuore, nei vasi sanguigni, nelle ghiandole, ecc.
L'importanza di questa inattivazione è messa in evidenza dai gravi e fatali effetti che seguono l'inattivazione dell'enzima idrolizzante. Si conoscono molti gruppi di anticolinesterasici, alcuni dei quali sono usati come insetticidi o sono stati usati o proposti come veleni nell'industria chimica bellica (v. cap. 10, § a, 3).
Le colinesterasi possono essere classificate come acetilcolinesterasi e butirrilcolinesterasi (che in precedenza sono state spesso chiamate ‛non specifiche'), a seconda dell'effetto ottimale sul substrato. L'AChE è inibita da alte concentrazioni di ACh; ciò dipende dal fatto che il substrato si attacca in due punti all'enzima. Sebbene, in generale, il tessuto nervoso contenga AChE e gli altri tessuti BChE, i gangli del sistema autonomo le contengono entrambe; i due tipi di colinesterasi differiscono anche perché reagiscono in maniera diversa all'azione degli inibitori.
L'AChE si trova nei mitocondri, nel reticolo endoplasmatico e nella membrana cellulare, fatto che prova che questo enzima si fissa alle membrane. Esso è stato ottenuto in forma cristallina e ha un peso molecolare di 260.000; è uno dei più potenti enzimi conosciuti, essendo in grado di idrolizzare 730 nmoli di ACh per mg di proteina enzimatica per ora.
Il centro attivo dell'enzima ha un sito anionico che attrae la carica positiva dell'ACh, e un sito estereo che lega l'atomo di carbonio carbonilico dell'ACh.
b) Sistema simpatico.
1. Monoamminossidasi (MAO). - Il trasmettitore simpatico, la noradrenalina, è inattivato mediante ricaptazione e successivo legame nel tessuto, principalmente nelle terminazioni nervose, mediante coniugazione con acido solforico o glucuronico, e attraverso l'azione di due differenti tipi di enzimi, la monoamminossidasi (MAO) e la catecol-O-metiltransferasi (COMT). La MAO agisce causando la deamminazione ossidativa della catena laterale della noradrenalina, che determina il distacco di 1 mole di ammoniaca. Si forma un'aldeide intermedia che è trasformata dall'aldeidedeidrogenasi in acido dudrossimandelico:
Quest'ultimo è in parte escreto come tale nell'urina. La MAO è ampiamente distribuita nell'organismo (v. Blaschko, 1942) ed è estremamente attiva nel fegato e nelle ghiandole salivari, nonché nel rene e nell'intestino. Anche il sistema nervoso contiene questo enzima, il che è un dato interessante data l'importanza delle ammine nel sistema nervoso centrale. La MAO si trova anche nei mitocondri e, poiché questi sono normalmente presenti nei rigonfiamenti delle terminazioni dei nervi adrenergici, si è supposto che abbia un ruolo nell'inattivazione del trasmettitore in eccesso e del suo precursore, dopammina, nelle terminazioni nervose. In certe condizioni questa inattivazione può avere notevole importanza, per esempio dopo somministrazione di farmaci, come la reserpina, che inibiscono o prevengono il legame del trasmettitore ai granuli di deposito. In questo caso il trasmettitore è rapidamente inattivato e lascia le terminazioni nervose sotto forma di metaboliti acidi.
Si ritiene generalmente che la maggior parte del trasmettitore liberato sia captata rapidamente dalle terminazioni nervose, dove esso viene in parte legato di nuovo ai granuli di deposito e in parte inattivato dalla MAO.
Dal momento che l'effetto potenziatore degli inibitori della MAO (iproniazide, nialammide, feniprazina, tranilcipromina) sulla stimolazione adrenergica è solo modesto o del tutto nullo, si è concluso che l'inattivazione da parte di questo enzima deve avere solo un ruolo sussidiario. Gli inibitori della MAO, d'altra parte, agiscono come farmaci antidepressivi probabilmente aumentando la concentrazione del trasmettitore adrenergico nell'area del recettore del sistema nervoso centrale. La noradrenalina non è un substrato altrettanto buono della tirammina o della dopammina per la MAO.
In certe condizioni gli inibitori della MAO possono causare un forte aumento dell'azione del trasmettitore dei nervi adrenergici. Così dopo reserpina, che di per sé ha scarsa azione sull'attività simpatica e spesso la deprime, un inibitore della MAO, che da solo ha altrettanto scarsa azione sull'attività simpatica, può causare un aumento notevole degli effetti della stimolazione simpatica con tachicardia e aumento della pressione. Una combinazione di questi farmaci può pertanto essere rischiosa per la salute.
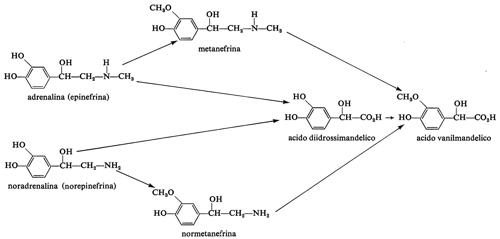
2. Catecol-O-metiltransferasi. - Questo enzima venne scoperto in seguito all'osservazione che pazienti con tumori delle cellule cromaffini (feocromocitoma) dopo somministrazione di noradrenalina o adrenalina eliminavano con l'urina grandi quantità di acido 3-metossi-4-idrossimandelico. Anche le ammine 0-metilate corrispondenti, normetanefrina e metanefrina, erano normalmente reperite nelle urine, in parte in forma coniugata, in aggiunta alla 3-metossitirammina e al 3-metossi-4-idrossifenilglicol (v. Axelrod, 1965). In condizioni normali una gran parte della noradrenalina secreta dai nervi adrenergici nell'uomo è 0-metilata ed è eliminata nell'urina come acido 3-metossi-4-idrossimandelico o acido vanilmandelico (VMA), secondo lo schema di degradazione dell'adrenalina e della noradrenalina (v. schema a pag. 701).
Formula
Dopo trattamento con un inibitore della MAO, la quantità di VMA è ridotta e viene escreta una quantità maggiore di normetanefrina, e ciò indica che la maggior parte dell'inattivazione è dovuta alla COMT. In condizioni normali la quantità di VMA eliminata nell'urina raggiunge i 3-6 mg al giorno e costituisce pertanto il metabolita più importante della noradrenalina. Il VMA è perciò usato spesso come misura relativa della secrezione delle catecolammine nel corpo. La COMT causa 0-metilazione di tutti i derivati del catecolo e per la sua azione è necessaria la presenza di S-adenosilmetionina e ioni Mg2+ o altri cationi bivalenti. D'altra parte i monofenoli come la tirammina non vengono O-metilati. Si pensa che il metallo bivalente agisca come un agente chelante per associare l'enzima, il substrato e il cofattore. Il gruppo metile elettrofilo della S-adenosilmetionina è presumibilmente trasferito al gruppo idrossi da uno spostamento nucleofilo, dal momento che il gruppo 3-idrossi è normalmente fortemente nucleofilo. Polifenoli come il pirogallolo inibiscono l'azione della COMT e agiscono come substrati. Anche i composti a sette anelli, come il tropolone, agiscono come inibitori formando chelati stabili con i cationi bivalenti.
La COMT è presente nella maggior parte degli organi e tessuti, compresi i nervi e il sistema nervoso centrale. L'enzima è presente nel citoplasma ma non nei mitocondri come la MAO. Nell'utero gravido l'attività della COMT aumenta. Si pensa che, mentre la MAO deammina le catecolammine intraneurali, la COMT agisca soprattutto sulle catecolammine liberate circolanti. L'inattivazione provocata dalla COMT è un processo rapido.
La noradrenalina abbandona molto lentamente il sistema nervoso centrale o il liquido cerebrospinale; tuttavia, i metaboliti deamminati scompaiono più rapidamente dal sistema nervoso centrale.
Dal momento che la quantità di noradrenalina radioattiva, liberata mediante stimolazione nervosa da un organo previamente caricato e riscontrabile nel sangue venoso che ne fuoriesce, è accompagnata da una piccola quantità di ammina 0-metilata, ma non da prodotti deamminati, è chiaro che una parte del trasmettitore liberato è 0-metilata, ma che la maggior parte abbandona l'organo come ammina non modificata. Sia la deamminazione che la 3-metossilazione, pertanto, avvengono durante il passaggio del sangue circolante attraverso i tessuti, particolarmente il fegato e il rene.
3. Coniugazione. - Una parte considerevole delle catecolammine liberate dai nervi in seguito a stimolazione e di quelle liberate dalla midollare del surrene è coniugata ed escreta nelle urine sotto forma di solfati o glucuronati.
4. Inattivazione per captazione da parte dei tessuti. - Da un punto di vista funzionale l'azione del trasmettitore può essere fatta terminare da tutti i meccanismi che rimuovono la sostanza attiva dall'area a cui è destinata, cioè i recettori delle cellule effettrici. Ciò può avvenire, come descritto, mediante degradazione o trasformazione enzimatica, ma anche semplice rimozione. Si hanno prove convincenti che la terminazione nervosa adrenergica permette alla noradrenalina di passare rapidamente attraverso la membrana dell'assone ed entrare nell'assoplasma, dove può legarsi ai granuli specifici di riserva o anche, momentaneamente, a qualche altro composto dell'assoplasma. Una parte del trasmettitore adrenergico, liberato in conseguenza di un treno di stimoli, agisce sui recettori, mentre la parte ‛in eccesso' rientra rapidamente nel neurone e scompare dall'area a cui è destinata. Tale concetto è ampiamente basato sui risultati di esperimenti con cocaina e desiprammina che, bloccando la captazione dell'ammina attraverso la membrana dell'assone, mantengono una più alta concentrazione del trasmettitore vicino ai recettori e causano un potenziamento dell'azione. Dopo carico di un organo con noradrenalina radioattiva, che si lega principalmente alle terminazioni nervose, una certa quantità di questa viene liberata in seguito a stimolazione nervosa insieme con l'ammina non marcata. Se il tessuto è stato esposto a un inibitore della captazione, come cocaina o desiprammina, la quantità di trasmettitore che si recupera nel sangue venoso proveniente dall'organo risulta quasi raddoppiata. Una certa quantità del trasmettitore liberato può essere assorbita da cellule di altri tessuti e momentaneamente legata o inattivata da enzimi.
5. Aspetti generali degli effetti della stimolazione dei nervi del sistema autonomo
a) Azioni eccitatorie e inibitorie
Il sistema nervoso autonomo regola in maniera precisa diverse funzioni dell'organismo; tale controllo si esercita per mezzo sia di stimolazioni sia di inibizioni. Nel caso del sistema cardiovascolare, per esempio, le funzioni cardiache e vascolari sono modulate da una serie di azioni riflesse che regolano la frequenza del battito, la forza della contrazione e il diametro dei vasi attraverso la mediazione dei nervi autonomi e dei loro trasmettitori. La stimolazione del vago o l'acetilcolina producono l'inibizione del cuore, mentre la stimolazione simpatica aumenta la frequenza cardiaca e la forza contrattile. L'azione opposta dei due sistemi è caratteristica e fornisce una precisa regolazione delle funzioni. La stimolazione simpatica di norma causa la contrazione della muscolatura liscia dei vasi, a eccezione dei vasi del cuore che vengono invece dilatati. La dilatazione coronarica da stimolazione simpatica è tuttavia in massima parte di origine indiretta, essendo dovuta all'azione di metaboliti (forse adenosina) che si accumulano nel tessuto a causa del concomitante aumento dell'attività contrattile miocardica. La maggior parte dell'albero vascolare è fornita solo di nervi simpatici, e pertanto la vasodilatazione è ottenuta mediante una diminuzione del tono simpatico. Tuttavia, nervi vasodilatatori specifici del sistema parasimpatico si trovano in certe ghiandole che richiedono un aumentato flusso ematico al fine di permettere la secrezione di una maggior quantità di liquido, come nelle ghiandole salivari o in altre dell'apparato digerente. Fibre nervose simpatiche vasodilatatrici si trovano nel muscolo scheletrico, e in questo caso il neurotrasmettitore è l'acetilcolina. Le fibre muscolari lisce dei muscoli dell'iride vengono contratte da nervi sia simpatici sia parasimpatici, ma dal momento che essi sono sistemati in maniera radiale e circolare, rispettivamente, vengono ottenuti effetti opposti, resi più efficaci dall'inibizione del muscolo antagonista.
Pertanto la stimolazione dei nervi simpatici può causare sia contrazione sia inibizione della muscolatura liscia a seconda del tipo di accoppiamento tra recettore e sistema di contrazione-rilasciamento. Ciò vale anche per la stimolazione parasimpatica mediata dall'acetilcolina. Si è osservato che l'azione stimolante sulla muscolatura liscia esercitata dalla noradrenalina o dall'acetilcolina è accompagnata da una depolarizzazione della membrana muscolare e dalla comparsa di potenziali d'azione, mentre l'inibizione è accompagnata da iperpolarizzazione e scomparsa dei potenziali d'azione.
b) Recettori α e β
La noradrenalina liberata dalle terminazioni nervose simpatiche e l'adrenalina immessa in circolo dalla midollare surrenale vanno ad agire su siti reattivi (recettori) delle cellule effettrici, iniziando una serie di eventi che portano alla risposta caratteristica del tessuto. Le azioni delle catecolammine sono complesse, talora eccitatorie, talaltra inibitorie, e si esercitano su cellule effettrici sia diverse sia dello stesso tipo (per es. fibre muscolari lisce) in organi diversi o in specie diverse. Si è potuta comprendere parte di questa complessità dimostrando che i recettori adrenergici possono essere distinti in due categorie principali in base a vari criteri e anzitutto al tipo di farmaco che ne blocca specificamente l'attivazione. I recettori α vengono bloccati da sostanze quali l'ergotammina, la fentolammina, la dibenammina, la fenossibenzammina e la dibenzilina, per questo chiamate α-bloccanti. I recettori β trovano il loro bloccante elettivo nel propranololo, nel pronetalolo e nel sotalolo, conseguentemente denominati β-bloccanti
La diversità dei due tipi di recettori è inoltre confermata dalla loro diversa sensibilità alle catecolammine e loro agonisti. I recettori α sono più sensibili all'adrenalina (A) e alla noradrenalina (NA) e assai poco a un loro agonista esogeno (cioè non presente nell'organismo) chiamato isoprenalina (I) o isoproterenolo (isopropilnoradrenalina): l'ordine di efficacia sui recettori α è quindi A ≥ NA > I. I recettori β sono invece massimamente sensibili all'isoprenalina e meno alla NA e A: per quanto concerne la relativa efficacia di queste ultime, si distinguono recettori B1 (situati nel cuore e nelle cellule adipose), in cui l'ordine di efficacia è isoprenalina > NA > A, e recettori B2 (situati nei bronchi e nei vasi sanguigni), in cui l'ordine è isoprenalina > A > NA. La diversità tra recettori B1 e B2 è anche dimostrata dall'esistenza, oltre ai β-bloccanti generali quali il già menzionato propranololo, di bloccanti specifici per i recettori β, ad esempio del cuore o dei vasi sanguigni.
Esiste infine una buona correlazione, benché non assoluta, tra il tipo di recettore e il segno dell'effetto (eccitatorio o inibitorio) prodotto dalla sua attivazione: i recettori α sono per lo più eccitatori e quelli β inibitori. Questa è anzi la regola per la muscolatura liscia dei vasi sanguigni. Esistono tuttavia rimarchevoli eccezioni, quando si consideri la totalità degli effettori adrenergici: l'azione eccitatoria sul cuore (aumento della frequenza e della forza delle contrazioni miocardiche) delle catecolammine (NA e A) è dovuta all'attivazione di β-recettori ed è pertanto imitata dall'isoprenalina e bloccata dal propranololo. Per quanto concerne invece gli α-recettori, generalmente ad azione eccitatoria, l'eccezione è costituita dalla muscolatura liscia non sfinterica delle pareti del tubo digerente, in cui gli effetti alfa sono inibitori, in sinergismo con quelli beta anch'essi presenti e, come di consueto, inibitori. In un certo numero di effettori adrenergici, tra cui molti vasi sanguigni, esistono recettori sia α sia β. Nel caso dei vasi sanguigni, le catecolammine hanno azione costrittrice o dilatatrice a seconda sia della predominanza in un determinato distretto vascolare dei recettori α o di quelli β, sia in base alla diversa sensibilità di questi recettori ad adrenalina, noradrenalina e isoprenalina. L'isoprenalina, ad esempio, poiché attiva essenzialmente i recettori β (che hanno in tutti i vasi azione inibitoria), produce generalmente vasodilatazione. L'adrenalina, in concentrazioni fisiologiche (cioè quelle prodotte dall'attività della midollare surrenale), produce vasodilatazione nei vasi del muscolo scheletrico, del cuore e del fegato, mentre causa vasocostrizione nella milza e nei vasi splancnici e renali. Questa differenza è appunto attribuibile da un lato alla predominanza dei β-recettori nel primo gruppo di vasi e degli α-recettori nel secondo, dall'altro alla maggior efficacia dell'adrenalina sui recettori β. I vasi della cute hanno solo recettori α e l'adrenalina ha naturalmente su di essi azione vasocostrittrice. A causa dell'azione combinata di vasocostrizione e vasodilatazione, la somministrazione di adrenalina non aumenta (e anzi in genere leggermente riduce) la resistenza perilenca totale del circolo sistemico. La noradrenalina, infine, ha azione vasocostrittrice su tutti i vasi (con la possibile eccezione dei vasi coronarici) poiché essa è più efficace sui recettori α (ad azione eccitatoria). Per tale maggiore efficacia la noradrenalina induce vasocostrizione anche nei vasi in cui predominano i recettori β, come i vasi del muscolo scheletrico, con azione dunque opposta a quella dell'adrenalina. Per la sua azione di vasocostrizione generalizzata, la noradrenalina aumenta la resistenza periferica totale e a tale scopo può essere usata in medicina.
c) Natura dei recettori α e β e del meccanismo d'azione del trasmettitore
Molte prove indicano che il recettore β è strettamente associato con l'enzima adenilciclasi. Tale enzima è presente quasi esclusivamente nella membrana cellulare e la sua attivazione determina la trasformazione dell'adenosintrifosfato (ATP) in adenosin-3′,5′-monofosfato ciclico (AMP ciclico) (v. Sutherland e Rall, 1960). L'AMP ciclico costituisce in generale il ‛secondo messaggero', che traduce un messaggio extracellulare ('primo messaggero') in una risposta intracellulare. Il primo messaggero può essere un ormone, oppure, come nel caso delle catecolammine, un mediatore chimico. L'AMP ciclico a sua volta attiva delle proteinachinasi, la diversità delle quali determina il carattere specifico dell'effetto dell'AMP ciclico in tessuti diversi. La proteinachinasi catalizza la fosforilazione di proteine di membrana, la cui forma fosforilata a sua volta determina, o attraverso un effetto metabolico o attraverso una variazione del potenziale di membrana, la risposta specifica della cellula bersaglio. Questa catena di eventi viene controllata nella sua durata da una fosfodiesterasi che idrolizza l'AMP ciclico e da una fosfoproteinafosfatasi che riporta la proteina alla sua forma non fosforilata inattiva. Gli effetti prodotti dall'attivazione dei recettori β da parte delle catecolammine, quali ad esempio l'effetto glicogenolitico sul fegato, l'effetto motropo e cronotropo positivo sul cuore, l'effetto lipolitico sul tessuto adiposo, sono dunque mediati dall'AMP ciclico.
Molto poco è conosciuto circa la natura del recettore α, tranne che esso non è in relazione con l'adenilciclasi e l'AMP ciclico. L'attivazione da parte delle catecolammine dei recettori α porta in generale a modificazioni della conduttanza di membrana a vari ioni (potassio, sodio, cloro e cala seconda del tipo di azione, eccitatoria o inibitoria, e del tipo di tessuto.
d) Frequenza di stimolazione e suo effetto; tono parasimpatico e simpatico
La frequenza di stimolazione necessaria per essere efficace è in genere alta nei muscoli scheletrici, mentre è piuttosto bassa nel sistema autonomo: qui l'effetto massimale è raggiunto, infatti, a una frequenza di circa 10 impulsi per secondo (v. Folkow, 1952), mentre nei nervi motori scheletrici richiede 100-250 impulsi per secondo. Normalmente i nervi del sistema autonomo mantengono continuamente un certo grado di attività attraverso l'attivazione riflessa e non si trovano mai completamente a riposo; persino una frequenza di uno stimolo ogni pochi secondi è sufficiente a mantenere gli effetti parasimpatici o simpatici in condizione di riposo. Da questa frequenza pigra il ritmo può essere rapidamente aumentato in caso di necessità.
L'attività a bassa frequenza è spesso chiamata tono simpatico o parasimpatico, e può essere prontamente dimostrata interrompendo la conduzione nei nervi autonomi postgangliari; ciò causa la cessazione del flusso di impulsi e alterazioni dell'attività dell'organo innervato. Questo effetto è particolarmente evidente nell'innervazione simpatica del letto vascolare, che è sempre sottoposto a un certo grado di contrazione. Da questo livello i vasi possono essere o ulteriormente contratti oppure dilatati come conseguenza di un cambiamento nel flusso degli impulsi. Nell'uomo in posizione eretta le fibre adrenergiche che vanno agli arti inferiori sono costantemente attive e quindi mantengono un certo grado di costrizione, particolarmente nelle vene, che è la condizione indispensabile a salvaguardare la normale pressione arteriosa. L'abolizione dell'attività simpatica causa una caduta della pressione arteriosa e anemia cerebrale seguita da vertigine o perdita di coscienza. In condizioni di riposo la midollare del surrene contribuisce molto poco all'attività generale degli organi innervati dai nervi simpatici, come si può notare dopo rimozione dell'organo. La liberazione improvvisa, ‛esplosiva', di ormoni attivi è un fenomeno riservato alle situazioni di emergenza.
e) Ipersensibilità da denervazione
Sezionando un nervo autonomo postgangliare o interrompendo in qualche maniera il flusso di impulsi l'effetto immediato è la cessazione completa dell'attività che è normalmente prodotta dal corrispondente neurotrasmettitore, o perdita di ‛tono'. I vasi sanguigni, per esempio, si dilatano al massimo. Tuttavia, dopo un po' di tempo, il tono ritorna; tale fenomeno è stato chiamato ‛tono muscolare intrinseco'. In seguito a sezione dei nervi parasimpatici o simpatici di un organo si osserva, dopo circa una settimana, che la sensibilità dell'organo al corrispondente neurotrasmettitore è aumentata. Per questa ragione perfino la noradrenalina circolante o il trasmettitore che diffonde dal tessuto innervato adiacente possono causare notevoli effetti.
L'ipersensibilità da denervazione degli organi innervati dal simpatico è dovuta principalmente al fatto che, con la degenerazione delle fibre e terminazioni simpatiche determinata dalla sezione assonale, viene a mancare uno dei meccanismi più importanti di inattivazione del mediatore adrenergico: la sua captazione da parte delle terminazioni nervose. Va notato a questo proposito che tale meccanismo è peculiare dei sistemi adrenergici ed è completamente diverso da quello alla base degli analoghi fenomeni nei sistemi colinergici. Nel muscolo scheletrico, ad esempio, l'ipersensibilità al mediatore chimico (l'acetilcolina) che consegue alla denervazione è dovuta allo sviluppo di nuovi recettori per l'acetilcolina in tutta l'area extrasinaptica delle fibre muscolari denervate, dove sono altrimenti assenti (per ulteriori informazioni, v. Lømo e Westgaard, 1976).
6. Effetti specifici dei nervi autonomi sui vari organi
a) Sistema cardiovascolare
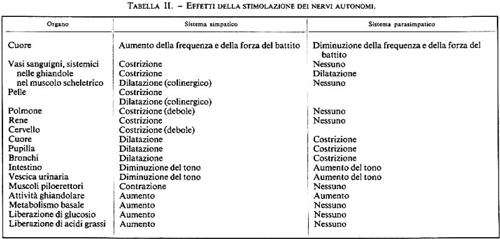
Nell'organismo i nervi autonomi influenzano l'attività del sistema nervoso centrale e la maggior parte degli organi. La tab. II mostra alcuni degli effetti dei nervi autonomi su varie funzioni fisiologiche.
La pressione arteriosa è mantenuta a un livello costante tramite un meccanismo riflesso a partenza dalla biforcazione dell'arteria carotide nel collo e dall'arco aortico. Un aumento della pressione arteriosa stimola i recettori da stiramento (barocettori) nella parete del seno carotideo, dal quale impulsi nervosi sono inviati attraverso il nono nervo encefalico ai centri del midollo allungato. Questi attivano le fibre efferenti vagali che vanno al cuore, riducendo in tal modo l'azione cardiaca e abbassando la pressione arteriosa (riflesso omeostatico). Contemporaneamente si determina una inibizione del tono vasale simpatico e i vasi si dilatano, contribuendo alla caduta della pressione arteriosa. Se la pressione invece è sotto il livello normale, il sistema simpatico, attivato dallo stesso tipo di riflesso, determina un aumento della forza dei battiti cardiaci e la costrizione dei vasi sanguigni che elevano la pressione sanguigna. Il potenziamento dell'attività simpatica in conseguenza dell'abbassamento della pressione sanguigna è spiegato da una diminuzione dell'inibizione normalmente esercitata dal riflesso barocettivo. L'aumento dell'attività simpatica nel cuore e nei vasi può essere anche provocato, in via riflessa, dalla mancanza di ossigeno e da una maggiore tensione di anidride carbonica del sangue: tali eventi agiscono sui chemocettori dei corpi carotidei e aortici. L'importanza dei riflessi simpatici nel letto vascolare è dimostrata dagli effetti di farmaci che impediscono il traffico degli impulsi, ad esempio i bloccanti dei gangli. Questi farmaci rendono difficile mantenere la posizione eretta, poiché il sangue si accumula nelle parti inferiori delle estremità, e conseguentemente se ne determinerà un ridotto afflusso al cervello. Il lavoro muscolare causa vasodilatazione nei muscoli, che è compensata da vasocostrizione in altre regioni; se quest'ultima è bloccata si avranno come conseguenza caduta della pressione sanguigna e segni di anemia cerebrale. Anche la posizione eretta in un ambiente ad alta temperatura può causare sintomi simili come risultato di una dilatazione riflessa dei vasi della pelle.
In genere il sistema simpatico agisce sul sistema vascolare nel suo insieme, mentre i nervi parasimpatici innervano organi specifici, come le ghiandole e gli organi della sfera genitale. Da un punto di vista funzionale è interessante notare che i vasi coronarici del cuore sono dilatati dai nervi simpatici, al contrario di tutti gli altri vasi. In questo modo il cuore riceve una maggiore quantità di sangue in concomitanza con gli stimoli che causano un'aumentata attività.
b) Occhio
L'illuminazione dell'occhio provoca un riflesso che causa costrizione della pupilla mediante attivazione dei nervi parasimpatici che vanno alle fibre muscolari circolari. Durante gli stati di eccitazione e di rabbia, vengono attivate le fibre simpatiche e la pupilla si allarga mediante contrazione delle fibre radiali.
c) Sistema gastrointestinale
Questo sistema è governato solo in parte da fibre autonome simpatiche e parasimpatiche in senso stretto. In generale, la stimolazione simpatica fa diminuire il tono intestinale a eccezione delle valvole e dei segmenti ristretti che separano le differenti sezioni (esofago, stomaco, piccolo intestino, grosso intestino, retto); la stimolazione parasimpatica ha effetto opposto. Tuttavia, l'intestino è ancora capace di movimenti peristaltici e di altro tipo dopo esclusione dei nervi simpatici e parasimpatici, per esempio dopo somministrazione di agenti di blocco come la fentolammina e l'atropina. Questa attività indipendente è stata attribuita alla presenza di un sistema specifico (sistema enterico) che ha un plesso nervoso nella parete intestinale (plesso di Auerbach e Müller).
d) Polmoni.
La regolazione della circolazione polmonare è controllata principalmente da meccanismi indipendenti dai nervi autonomi. Il flusso di sangue attraverso i polmoni può essere aumentato più di 5 volte senza aumento del gradiente di pressione, semplicemente mediante distensione delle sottili pareti vascolari. La circolazione attraverso i polmoni è regolata anche dalla pressione di ossigeno e di anidride carbonica del sangue che passa lungo i vasi dei polmoni. La stessa situazione si verifica anche nel caso del cordone ombelicale e della placenta, che sono privi di nervi del sistema autonomo.
7. Valutazione dell'attività dei nervi del sistema autonomo
In certe condizioni è utile sapere se l'attività del sistema nervoso autonomo è normale o se è alterata in una direzione o nell'altra. Ciò è valido per ambedue i sistemi, anche se per valutare il grado di attività del sistema parasimpatico si devono in generale usare metodi indiretti. È possibile ottenere informazioni sull'attività del sistema simpatico misurando l'escrezione di noradrenalina o dei suoi metaboliti nell'urina. Nell'uomo il metabolita principale delle catacolammine è l'acido vanilmandelico che pertanto è stato usato a questo scopo. Questo metabolita è formato sia dalla noradrenalina sia dall'adrenalina e perciò non ci permette di discriminare tra il trasmettitore simpatico e l'adrenalina che proviene dalla midollare del surrene. In alcuni casi la normetanefrina ci permette di valutare correttamente la secrezione di noradrenalina da ambedue le sorgenti. La noradrenalina e l'adrenalina libere eliminate nelle urine rappresentano solo una piccola percentuale del totale liberato, ma possono fornire egualmente informazioni utili sul grado di attività. Alcune volte viene impiegata noradrenalina radioattiva per determinare la velocità di turnover.
Un'aumentata escrezione di noradrenalina, che indica una più intensa attività simpatica, si osserva durante la posizione eretta ed è provocata dai riflessi omeostatici pressori. Durante il lavoro muscolare, particolarmente durante l'esercizio fisico intenso, l'escrezione di noradrenalina aumenta notevolmente. L'escrezione di noradrenalina aumenta anche in certe condizioni di superlavoro mentale o di esposizione a basse temperature.
In alcuni stati patologici si osserva che la noradrenalina viene escreta in quantità più alte del normale. Ciò si verifica in certe forme di ipertensione e può in tal caso indicare che la vasocostrizione è dovuta almeno in parte all'iperattività del sistema simpatico e può essere contrastata da farmaci appropriati. Certi farmaci, come la nicotina, alcuni agenti bloccanti adrenergici e veleni come il tallio, causano aumento dell'escrezione di noradrenalina. Negli ustionati si osserva un grande aumento dell'escrezione di noradrenalina nell'urina, e anche i valori dell'adrenalina possono essere elevati.
Anche la determinazione della concentrazione di noradrenalina nel plasma sanguigno può essere usata come misura dell'attività simpatica.
In condizioni di riposo c'è una costante, ma bassa escrezione di noradrenalina nelle urine, circa 10 ng per minuto. Questo valore può aumentare a 50 ng/minuto nella posizione eretta e ad alcune centinaia di ng/minuto durante il lavoro pesante.
Una diminuita attività del sistema simpatico si osserva nella sindrome da ipotensione posturale, che è associata con una deficienza funzionale di questo sistema. In questa condizione i pazienti presentano segni di anemia cerebrale durante la posizione eretta. Alcuni farmaci inibiscono la sintesi o la liberazione del neurotrasmettitore simpatico e producono sintomi simili (v. cap. 10).
8. Midollare del surrene e cellule cromaffini
Nell'uomo e in molti animali le ghiandole surrenali, che sono situate vicino ai poli superiori dei reni, sono costituite da una porzione centrale di cellule midollari, avvolte da una capsula di cellule corticali che rappresentano di norma la parte più cospicua della ghiandola. Le cellule midollari prendono origine dall'ectoderma (cresta neurale: v. cap. 11, § b) e migrano verso la loro sede di destinazione durante un precoce stadio della vita embrionale. Alcune cellule cromaffini sono localizzate lungo l'aorta e formano i cosiddetti paragangli, il più grande dei quali è l'organo di Zuckerkandl. Dopo la nascita quest'organo regredisce, mentre le ghiandole surrenali crescono con rapidità, probabilmente a causa della presenza delle cellule corticali. In alcune lucertole e uccelli le cellule cromaffini si trovano sparse a gruppi all'interno del tessuto corticale. Cellule contenenti catecolammine sono state trovate negli Insetti, e perfino nel lombrico. Le cellule cromaffini sono cosi chiamate perchè reagiscono col dicromato assumendo una colorazione bruna. È stato trovato che esse contengono le catecolammine adrenalina, noradrenalina o dopammina, che formano composti rossi con lo iodio e composti verdi con i sali ferrici.
Le cellule che contengono adrenalina e noradrenalina possono essere distinte su basi immunoistochimiche (v. cap. 2, § c). L'adrenalina e la noradrenalina sono presenti in proporzioni differenti nella midollare del surrene di animali diversi, per cui, mentre nella balena la noradrenalina può rappresentare fino al 90% delle ammine, nel coniglio è quasi del tutto assente. Nell'uomo l'adrenalina forma l'85% delle ammine.
La tab. III mostra la proporzione di noradrenalina nelle ghiandole surrenali di alcune specie.
Le cellule cromaffini contengono grandi quantità di particelle subcellulari nelle quali sono immagazzinate le ammine. L'aspetto di queste particelle varia a seconda del tipo di catecolammina che contengono. Esse si colorano di nero col cloruro di osmio e hanno un diametro che varia tra 0,1 e 0,4 μm. In alcune delle particelle si possono vedere sottostrutture di 0,02 μm di diametro. Da un punto di vista chimico i granuli contengono, oltre alle ammine, adenosin-5′-trifosfato (ATP), fosfolipidi e una proteina specifica, la cromogranina A. Dal momento che il rapporto di concentrazione molare delle ammine e dell'ATP è vicino a 4, che corrisponde al rapporto delle rispettive cariche (una positiva delle ammine e 4 negative dell'ATP), si ritiene che esse si combinino chimicamente, probabilmente in un complesso con la proteina specifica. Nei granuli le ammine sono immagazzinate in una forma protetta, insensibile all'ossidazione. Tuttavia acidi e composti attivi sulla membrana rompono la membrana dei granuli e dissociano il complesso, cosa che avviene anche nella lisi iposmotica o per via meccanica mediante trattamento con ultrasuoni. A bassa temperatura i granuli di ormoni sono stabili, ma a temperatura corporea essi perdono l'ammina assieme ai nucleotidi e alle proteine. Nei granuli si può avere uno scambio di ammine, ma dopo svuotamento essi non possono captarne di nuove. Per questa ragione è necessaria una settimana o più prima che le ghiandole surrenali riacquistino il loro contenuto normale di ormoni dopo deplezione, apparentemente dopo la formazione di nuove particelle di deposito.
a) Ormoni della midollare del surrene
1. Chimica. - Dopo che era stato scoperto (v. Oliver e Schäfer, 1895) che gli estratti di ghiandola surrenale provocano un aumento notevole della pressione sanguigna, fu isolata una sostanza attiva (v. Takamine, 1901) che fu chiamata adrenalina. Essa fu sintetizzata nel 1904. L'analogo non metilato, la noradrenalina, fu trovato nelle ghiandole surrenali solo nel 1944 (v. Holtz e altri, 1947) e la dopammina fu scoperta ancora più tardi.
Chimicamente l'adrenalina è 3,4-diidrossifenil-N-metilamminoetanolo e ha peso molecolare 183,2. Il composto naturale è levogiro, ma la sua configurazione chimica corrisponde a un composto della serie D e dovrebbe essere indicata come D(−)-adrenalina. La noradrenalina è l'ammina primaria corrispondente non metilata, e la dopammina, che è otticamente inattiva, è priva del gruppo idrossilico nella catena laterale.
2. Biosintesi. - Gli ormoni della midollare sono sintetizzati nelle cellule cromaffini dall'amminoacido tirosina, che è normalmente presente nei liquidi del corpo. La tirosina viene idrossilata nei granuli a diidrossifenilalanina (dopa) dall'enzima tirosinaidrossilasi. La dopa è decarbossilata dalla L-dopadecarbossilasi a dopammina (DA), che a sua volta è β-idrossilata a noradrenalina tramite l'enzima arilammina-β-idrossilasi. Quest'ultima reazione richiede la presenza dei granuli che contengono l'enzima. La noradrenalina è trasformata in adrenalina dall'enzima catecol-N-metiltransferasi.
L'idrossilazione della tirosina è la reazione più lenta della catena della biosintesi e perciò è quella che ne limita la velocità. Apparentemente la regolazione fisiologica della sintesi agisce a questo stadio.
3. Inattivazione. - L'inattivazione degli ormoni della midollare del surrene segue in generale il corso schematizzato per il trasmettitore dei nervi autonomi, a eccezione del fatto che tutti gli ormoni della midollare passano attraverso il sistema circolatorio e raggiungono le cellule effettrici dopo che sono stati captati dal liquido extracellulare. È pure ovvio che gli ormoni non sono diretti specificamente a un'area recettrice post-giunzionale, come per le cellule innervate, ma raggiungeranno tutte le zone della cellula. Dal momento che la catecol-O-metiltransferasi (COMT) è ubiquitaria come ormone inattivante, la maggior parte dell'adrenalina secreta dal surrene verrà trasformata in metanefrina, che è escreta nelle urine in forma libera o coniugata e anche deamminata. Nell'uomo, dopo somministrazione di adrenalina radioattiva si trova che circa il 90% della quantità totale è metilata dalla COMT, e di questa circa una metà è deamminata. Quando con i cibi si ingeriscono quantità relativamente elevate di adrenalina (per esempio, le ghiandole surrenali possono essere usate nella preparazione delle salsicce) una grande parte di questa sarà escreta nelle urine sotto forma di composti coniugati. Il tempo di dimezzamento dell'adrenalina nel plasma sanguigno è di circa 30 secondi, e ciò indica che l'inattivazione per captazione e degradazione enzimatica è moderatamente lenta.
b) Funzione degli ormoni della midollare del surrene
Dato che nella maggior parte degli animali, a eccezione degli organismi molto primitivi, sono presenti cellule che producono catecolammine e perfino un organo speciale per la loro produzione, si deve dedurre che esse hanno un ruolo importante nel mantenimento di una vita organizzata nell'ambiente predominante. D'altra parte la midollare del surrene non è di per sé indispensabile per la vita, come si può rilevare rimuovendo questa parte della ghiandola. Nei suoi studi classici sulla funzione della midollare del surrene Cannon (v., 1915) ha considerato l'adrenalina come un ormone di emergenza, che aiuta l'organismo in certe condizioni di stress come fame, paura e dolore. Per mezzo delle sue azioni essa prepara l'organismo alla paura e alla rabbia, determinando o potenziando le attitudini alla fuga e all'aggressività. Queste categorie emozionali in alcune condizioni della vita animale possono perfino dare la salvezza, come nel caso in cui un animale attaccato fugge rapidamente o combatte per la sopravvivenza. Nella vita civilizzata dell'uomo, tuttavia, raramente si presentano situazioni simili; si è osservato che la rimozione chirurgica delle ghiandole surrenali per scopi terapeutici, compensata dalla somministrazione di ormoni corticali, determina come unico cambiamento apparente un'attitudine più tranquilla e pacifica.
L'adrenalina, oltre ai cambiamenti comportamentali riproducibili se questo ormone viene iniettato, esplica nell'organismo diversi tipi di azioni che sembrano tutte convergere verso una migliore attività fisica. Queste azioni funzionali coinvolgono il sistema cardiovascolare, la respirazione, la forza muscolare, la visione e molte altre attività.
1. Cuore e circolazione del sangue. - Anche piccole quantità di adrenalina innalzano la frequenza cardiaca e aumentano la forza del battito, accrescendo pertanto la gettata cardiaca. Nello stesso tempo il letto vascolare nei diversi organi viene influenzato in tal modo che la corrente sanguigna è redistribuita nel corpo, provvedendo così a fornire le migliori condizioni per l'attività fisica. Alcune aree vascolari vengono contratte, come nella pelle (pallore) e nel tratto gastrointestinale, mentre il flusso del sangue attraverso i muscoli, il cuore e il fegato viene aumentato. Il sangue è così deviato a quelle parti che richiedono un rifornimento maggiore durante la lotta e la fuga. Attraverso questa redistribuzione del sangue la resistenza totale del letto vascolare è moderatamente abbassata, e perciò l'aumento del flusso ematico totale non richiede un aumento della pressione ematica media. Inoltre, il flusso sanguigno relativamente basso nella pelle riduce il rischio di una perdita di sangue nel caso di lesioni superficiali. L'erezione dei peli negli animali rivestiti di pelliccia può anche essere d'aiuto nell'atto difensivo, in quanto incute paura all'attaccante.
2. Muscolatura liscia. - In generale, si può dire che l'adrenalina fa contrarre o rilasciare il muscolo liscio, a seconda del tipo di recettore presente nelle cellule bersaglio. Sotto questo aspetto l'adrenalina differisce dalla noradrenalina, la quale agisce soprattutto sui recettori α vascolari, mentre l'adrenalina ha un effetto stimolante anche sui recettori β. Ne segue che le azioni dell'adrenalina non possono essere fedelmente riprodotte dalla noradrenalina liberata dai nervi adrenergici, ma possono alterare lo schema di risposta della muscolatura liscia per gli speciali scopi ricordati sopra.
Il più grande sistema organico a muscolatura liscia è il sistema gastrointestinale. L'adrenalina ha un effetto rilassante generale su questo sistema, la cui richiesta di sangue è quindi ridotta a beneficio dei muscoli scheletrici. Altri organi a muscolatura liscia reagiscono in diversi modi: così la membrana nittitante e il muscolo dilatatore della pupilla vengono contratti, creando migliori condizioni per una buona visione; i muscoli bronchiali vengono rilassati e il flusso d'aria ai polmoni è così facilitato; la milza viene contratta facendo fuoriuscire il sangue di riserva che diviene così disponibile per la circolazione generale.
3. Azioni metaboliche. - Sono state descritte svariate azioni metaboliche che coadiuvano efficacemente gli effetti meccanici dell'adrenalina. Il cosiddetto effetto calorigeno dell'adrenalina, per esempio, dipende in parte dalla sua capacità di mobilizzare gli acidi grassi dai vari depositi; in questo modo il rifornimento d'energia per la combustione viene aumentato. Un'azione di questo tipo può essere particolarmente utile durante l'esposizione a basse temperature, quando è necessario un aumentato metabolismo per il mantenimento della temperatura corporea. La funzione di alcuni organi, come il sistema nervoso, dipende da un adeguato apporto di glucosio, mentre la mancanza di cibo determina il rischio dell'esaurimento di tale rifornimento. Come fu osservato poco dopo la sua scoperta, l'adrenalina mobilizza lo zucchero dai depositi di glicogeno nei muscoli e nel fegato e salvaguarda così le funzioni cerebrali.
4. Azioni nervose. - Come ricordato sopra, l'adrenalina evoca alcuni sintomi emotivi mediante un'azione sul sistema nervoso che non è ancora stata spiegata. Questi effetti sono stati descritti come apprensione, senso di disagio e di difficoltà, e persino ansietà. Questo tipo di azione è ancor più interessante per il fatto che la quantità di ammina che può passare dal sangue al tessuto cerebrale è molto limitata, in conseguenza dell'ostacolo rappresentato dalla barriera ematoencefalica. Tuttavia, lo stesso cervello contiene piccole quantità di adrenalina che possono essere liberate e agire localmente. Se si somministrano piccole quantità di adrenalina mediante delle micropipette nel cervello, è possibile osservare che alcuni neuroni sono attivati dall'ormone, mentre altri sono inibiti. Tuttavia, il ruolo funzionale di questi effetti è compreso solo parzialmente.
Benché l'adrenalina sia l'ormone della midollare del surrene quantitativamente più rilevante, nella maggior parte dei Mammiferi, anche la noradrenalina è secreta dalla midollare, e questo sembra vero anche per la dopammina, sebbene questa rappresenti una piccola percentuale della quantità totale di ammine. Siccome la noradrenalina serve anche come trasmettitore nervoso adrenergico, non è necessario ricapitolare qui le sue azioni. Probabilmente la sua rapida liberazione in quantità piuttosto grandi rinforza le azioni dell'attività nervosa adrenergica. Si è ritenuto che la secrezione di noradrenalina possa essere particolarmente utile in quegli animali che attaccano le loro prede come fanno i felini, il che è corroborato dalla scoperta di quantità relativamente alte di noradrenalina nelle ghiandole surrenali di animali come il gatto e il leone.
Il ruolo della dopammina nella midollare del surrene o in altri gruppi cellulari è ancora sconosciuto. Sotto molti aspetti essa ha effetti simili a quelli dell'adrenalina, ma è circa 50 volte meno attiva sul sistema cardiovascolare. Essa appartiene alle ammine che hanno un'azione diretta sulle cellule effettrici e anche un'azione indiretta con la quale possono liberare adrenalina o noradrenalina dai siti di legame nei depositi, sia nelle particelle subcellulari sia altrove. Neuroni dopamminergici sono presenti anche nel sistema nervoso centrale (v. cap. 9, § b).
Da quanto è stato detto sembra che sia l'adrenalina, sia il suo analogo non metilato provochino una molteplicità di effetti, per cui il loro meccanismo d'azione è diventato un problema di primario interesse. La scoperta che queste ammine aumentano la formazione di adenosin-3′-5′-fosfato ciclico (cAMP) ha fornito sotto questo aspetto l'indicazione più importante (v. Sutherland e Rall, 1960). L'adrenalina, come molti altri ormoni, attiva l'enzima adenilciclasi che forma cAMP da ATP. Il cAMP interagisce con altri enzimi, così da facilitare le azioni della fosforilasi e della lipasi, innalzando quindi l'attività metabolica.
c) Secrezione della midollare del surrene
La secrezione di ormoni dalla midollare del surrene è stata studiata negli animali in varie condizioni sperimentali, misurando il contenuto di ormoni nel sangue venoso del surrene. Nell'uomo questo è stato fatto in alcuni casi raccogliendo il sangue per mezzo di un catetere inserito attraverso la vena cava nell'orifizio della vena del surrene.
In molti casi è possibile avere un'idea della secrezione ormonale misurando l'escrezione di adrenalina nell'urina. Le ammine libere costituiscono solo una piccola percentuale della quantità totale eliminata, ma questa proporzione sembra essere abbastanza costante e si presta perciò per misurazioni relative. Dall'analisi dell'urina è stato ricavato un gran numero di dati. Osservazioni fatte su pazienti a cui erano state asportate le ghiandole surrenali mostrano che l'adrenalina presente nell'urina è per la maggior parte secreta dalla midollare.
L'adrenalina può essere secreta dalla midollare del surrene in seguito a stimolazione dei suoi nervi secretori, che decorrono nei nervi splancnici; questi sono nervi pregangliari colinergici e passano attraverso il ganglio celiaco senza formarvi sinapsi. Le fibre si connettono direttamente con le cellule cromaffini e trasmettono i loro impulsi liberando acetilcolina. La nicotina e i composti nicotino-simili, come la dimetilfenilpiperazina (DMPP), hanno un'azione simile. È stato notato che la nicotina libera adrenalina in quantità maggiori rispetto alla stimolazione nervosa.
La sintesi di adrenalina può apparentemente continuare ad alta velocità anche se i depositi sono svuotati. Il contenuto in ormone non fornisce perciò una misura della capacità di sintesi e di liberazione. La ghiandola denervata, pur mostrando attività secretoria ridotta, continua a formare gli ormoni e a immagazzinarli.
Come abbiamo ricordato, i diversi ormoni midollari sono prodotti e depositati in cellule differenti, per cui la secrezione può essere differenziata dall'attivazione di differenti fibre nervose. Esperimenti di stimolazione localizzata di vari siti dell'ipotalamo e dell'area preottica hanno mostrato che alcune localizzazioni favoriscono la secrezione di noradrenalina, mentre altre liberano principalmente adrenalina. La stimolazione di certe aree nella regione orbitale causa inibizione della secrezione di catecolammine, fatto che indica che la secrezione è controllata a livello sopraipotalamico. Sembra verosimile che, a seconda se l'azione è di tipo centrale o riflessa, sia favorita la secrezione dell'uno o dell'altro ormone, per esempio in situazioni che comportano la fuga o l'aggressione. I cambiamenti posturali che alterano notevolmente la liberazione del trasmettitore adrenergico, la noradrenalina, dai nervi cardiaci e vasomotori hanno in genere un'azione modesta sulla secrezione di adrenalina.
In condizioni di riposo e in assenza di stress la secrezione è molto bassa, come si deduce dalle quantità riscontrate nell'urina durante il riposo e il sonno. Le quantità secrete in condizioni di riposo non sono state misurate direttamente nell'uomo, ma possono stimarsi di circa i ng per kg al minuto, valore che corrisponde a un'escrezione nell'urina di circa 1-2 ng per minuto in un adulto di taglia media.
Nell'uomo la stimolazione centrale che porta alla secrezione di adrenalina si osserva durante lo stress, ma è anche provocata dall'elettroshock e dalla pneumoencefalografia (iniezione di aria nei ventricoli cerebrali per scopi diagnostici). Una stimolazione riflessa della secrezione è provocata da stimolazione dei nervi afferenti in esperimenti su animali e probabilmente è presente, in connessione col dolore, in condizioni fisiopatologiche.
L'ipoglicemia causa un notevole aumento nella secrezione di adrenalina dalla midollare del surrene: tale meccanismo ha una grande importanza fisiologica, poiché salvaguarda automaticamente il bisogno che il sistema nervoso ha di glucosio, che è mobilizzato dall'adrenalina. Sotto questo aspetto l'adrenalina è considerevolmente più efficace della noradrenalina. Una dose di insulina sufficiente ad abbassare il glucosio ematico causa un marcato aumento dell'escrezione di adrenalina nell'urina. L'insulina a dosi più alte può provocare una grave deplezione dei depositi di adrenalina senza inibirne la sintesi e la liberazione. Anche il desossiglucosio, che sostituisce il glucosio nei centri ipotalamici, causa una forte secrezione di adrenalina che, d'altra parte, è abbassata dalla somministrazione di glucosio o di saccarosio.
Esponendo animali al freddo è stato possibile mostrare che sia l'adrenalina sia la noradrenalina sono secrete in quantità maggiori; l'aumento della secrezione di adrenalina è meno marcato di quello della noradrenalina e, durante esposizioni prolungate, raggiunge un picco alla fine della prima settimana. Un'aumentata escrezione di adrenalina nelle urine si riscontra anche nell'uomo esposto al freddo.
Anche l'emorragia, l'ipercapnia e l'ipossia determinano un aumento della secrezione di adrenalina dalla midollare, fino a raggiungere, qualche volta, valori molto alti. Nel feto l'organo di Zuckerkandl risponde all'asfissia con un'alta secrezione di noradrenalina; ciò sembra avere un'azione protettiva sul sistema nervoso centrale.
Durante il lavoro muscolare, se l'esercizio fisico è sufficientemente intenso, si ha un aumento della secrezione di adrenalina dalla midollare del surrene. Così a un consumo di ossigeno di 2 litri al minuto o più, l'escrezione di adrenalina nell'urina aumenta notevolmente, anche se in misura minore di quella di noradrenalina.
Durante lo stress mentale ed emotivo la secrezione di adrenalina è stata osservata in diverse condizioni (v. tab. IV). Perfino uno stato di moderata apprensione, come quella che può sperimentare un passeggero durante un viaggio in aereo, provoca nella maggior parte dei soggetti un aumento della produzione di adrenalina. Si sono notati aumenti simili e più grandi nell'escrezione di adrenalina durante le rotazioni in una centrifuga per uomo, in connessione con i lanci con paracadute e durante i voli spaziali suborbitali. È interessante il fatto che l'escrezione urinaria di adrenalina, ma non di noradrenalina, aumenta perfino prima che si verifichi l'evento. Questa tensione ‛da anticipazione' è riscontrabile negli esempi sopra riportati. Da questi studi risulta anche che c'è un adattamento, e quindi valori di escrezione più bassi, se le rotazioni nella centrifuga vengono ripetute; questo non è vero per i lanci con paracadute. Apparentemente non c'è adattamento quando l'evento è connesso con un rischio reale.
Altri studi hanno mostrato che l'escrezione di adrenalina aumenta spesso notevolmente prima e durante gli esami. Si è notata una tendenza a valori di escrezione minori nelle donne che negli uomini.
Lo stress connesso con le attività industriali, il rumore, il lavorare avendo poco tempo a disposizione, sono anche queste condizioni associate con un'aumentata escrezione di adrenalina. La quantità di adrenalina nell'urina è stata proposta e usata come misura del grado di tensione nelle varie situazioni. È anche stata notata una correlazione tra l'aumentata escrezione di catecolammine nell'urina e alcuni disturbi cardiaci, e ciò suggerisce che la tensione giuochi un ruolo nello sviluppo di questi disturbi.
Oltre alla nicotina e ai farmaci nicotino-simili, vi è un certo numero di altri composti che influenzano la secrezione di catecolammine dalla midollare del surrene. La reserpina previene la captazione nei granuli delle cellule cromaffini e in questo modo provoca un progressivo esaurimento dei depositi. La guanetidina, la fenossibenzammina, la prenilammina e gli inibitori della sintesi, come il decaborano, causano liberazione che alcune volte porta a svuotamento dei depositi. Alcune tossine, inoltre, impediscono il legame con i granuli e causano deplezione.
Diversi ormoni influenzano la secrezione di adrenalina, come detto sopra nel caso dell'insulina. L'iniezione endoarteriosa di piccole dosi di angiotensina II aumenta la secrezione di adrenalina. Infine l'istamina stimola direttamente le cellule cromaffini e provoca liberazione dei loro ormoni.
d) Meccanismo di liberazione
Gli stimoli nervosi che provocano secrezione di catecolammine dalle cellule cromaffini agiscono liberando acetilcolina dalle terminazioni nervose pregangliari e provocando la depolarizzazione delle cellule accompagnata anche dall'aumento della scarica di potenziali d'azione (v. Brandt e altri, 1976). Per la secrezione degli ormoni ottenuta mediante stimolazione nervosa, è fondamentale la presenza di ioni calcio. Tuttavia, ammine che agiscono indirettamente, come la tirammina o la feniletilammina, liberano gli ormoni mediante una reazione a scambio anche in assenza di ioni calcio. L'acetilcolina non provoca liberazione di ormoni dai granuli di deposito isolati, ma questi rispondono agli ioni calcio con una liberazione aumentata se è presente fosfato. Recenti osservazioni indicano che le ammine sono secrete dalle cellule cromaffini insieme ai nucleotidi (metaboliti dell'ATP), proteine, dopammina-β-idrossilasi e cromogranina A. Questi dati hanno suggerito che i granuli di deposito si fondano con la membrana cellulare e scarichino nel liquido extracellulare il loro contenuto, che, dopo aver passato la parete capillare, viene trasportato dalla corrente sanguigna alle altre parti del corpo. Dopo che si sono scaricati, i granuli ‛fantasmi' sono incapaci di captare e immagazzinare nuove ammine. Questa modalità di liberazione può spiegare la scarica iniziale, spesso ‛esplosiva', degli ormoni midollari.
Se i granuli di deposito isolati sono incubati in saccarosio o tampone fosfato, le ammine vengono gradualmente liberate a una velocità che dipende dalla temperatura e dal pH del mezzo, insieme con i nucleotidi e le proteine. È possibile che la liberazione di ormoni avvenga in vivo anche in questo modo. L'aggiunta di ATP e Mg2+ al mezzo inibisce la liberazione ormonale dai granuli isolati, che però aumenta in presenza di ioni cloruro.
Una caratteristica generale dell'azione di liberazione causata dall'acetilcolina e dalla nicotina in vivo è che l'effetto è forte all'inizio, ma si attenua in alcuni secondi a causa di un blocco secondario. Questo sembra essere un effetto di freno fisiologico che previene la liberazione continuata di grandi quantità di ormoni, che possono causare effetti indesiderabili.
I granuli di dopammina sembrano liberare il loro contenuto a una velocità più alta che non i granuli che contengono adrenalina e noradrenalina.
9. Funzioni centrali del sistema autonomo
a) Funzioni autonome dei centri dell'ipotalamo e di altre parti del cervello
Varie funzioni del sistema autonomo sono controllate da nuclei cerebrali e da aree nervose localizzate nella sostanza reticolare del ponte, del mesencefalo e del bulbo. Anche da alcune parti del cervello arrivano segnali nervosi che influenzano l'azione autonoma. Tuttavia, l'area più importante è l'ipotalamo, che si può considerare come il quartier generale di tutte le più importanti funzioni vegetative del corpo, come l'ingestione di cibo e acqua, la pressione del sangue, la regolazione della temperatura ecc.
Dopo sezione del tronco dell'encefalo a livello mesencefalico (decerebrazione) la pressione del sangue è mantenuta vicina a livelli normali e la respirazione continua. Tuttavia, se la sezione è fatta al di sotto del bulbo, la pressione del sangue cade immediatamente a circa metà del valore normale e la respirazione cessa (spinalizzazione). Stimoli che alterano la pressione del sangue e l'attività cardiaca possono essere evocati da varie aree dell'ipotalamo, ma anche da regioni corticali.
Il controllo della temperatura è localizzato nell'ipotalamo anteriore. Un aumento della temperatura del sangue che scorre verso quest'area attiva i sistemi neuronali che causano vasodilatazione e sudorazione, mentre un abbassamento provoca vasocostrizione e brividi. In certi animali il respirare affannosamente riduce la temperatura del corpo. Alcuni animali se esposti al freddo aumentano la liberazione di noradrenalina dai nervi adrenergici che vanno al tessuto adiposo, e in tal modo si liberano acidi grassi che servono come materiale di combustione.
Un aumento del metabolismo e della produzione di calore si può ottenere anche con una maggiore secrezione degli ormoni tiroidei.
Un'altra importante funzione è la regolazione dei liquidi del corpo, sia che si tratti della loro composizione che della loro quantità totale. La normale concentrazione di liquidi nel corpo è controllata dall'ormone antidiuretico, che è liberato nel lobo posteriore dell'ipofisi dalle terminazioni assoniche (neurosecrezione) di neuroni situati nell'ipotalamo. È qui, nei nuclei paraventricolare e sopraottico, che avviene sia la produzione che la regolazione della liberazione dell'ormone. Ad esempio, una maggiore concentrazione di sali nel plasma sanguigno, attraverso recettori (osmocettori) situati in queste aree, determina un aumento della scarica di impulsi nei neuroni ipotalamici in questione e quindi una maggiore liberazione ipofisaria dell'ormone antidiuretico, che riduce l'eliminazione di acqua con le urine, ristabilendo così l'equilibrio idrico. In modo corrispondente, una diluizione dei liquidi del corpo inibisce la secrezione dell'ormone e una maggior quantità d'acqua viene secreta dai reni, come si vede dopo ingestione d'acqua. Questo meccanismo regolatore è affiancato da uno speciale centro della sete localizzato nel nucleo ventromediale, che viene attivato da un aumento locale della concentrazione di sale.
La quantità totale di liquido corporeo è regolata in parte da un sistema che agisce attraverso segnali nervosi che provengono dal sistema a bassa pressione degli atri e delle grandi vene nel torace. Un aumento della quantità totale di liquido corporeo distende i vasi a pareti sottili e attiva i recettori da stiramento, che mandano impulsi ai centri ipotalamici provocando una diminuita immissione in circolo di ormone antidiuretico. Il controllo principale del volume del liquido extracellulare è tuttavia dovuto a meccanismi non nervosi che coinvolgono la renina e l'aldosterone.
Anche l'ingestione di cibo è regolata dai nuclei di quest'area. La mancanza di glucosio nel plasma sanguigno agisce come stimolante su certi recettori ipotalamici che provocano secrezione di adrenalina e mobilitazione di glucosio. Tale mancanza porta alla fame mediante l'attivazione di recettori specifici localizzati nell'area ipotalamica laterale, la cui distruzione fa scomparire l'appetito e determina una progressiva perdita di peso corporeo. La stimolazione di un centro della sazietà nel nucleo ventromediale provoca indifferenza per il cibo; se si distrugge tale centro non esistono più limiti nell'ingestione di cibo, il che può portare ad alti gradi di obesità.
Stimolando certe aree ipotalamiche della regione del nucleo perifornicale si rendono manifesti alcuni sintomi caratteristici della stimolazione della funzione del sistema autonomo, particolarmente del sistema simpatico; tali sintomi, che rientrano tutti nella manifestazione di rabbia e costituiscono un tipo di comportamento integrato, comprendono pupille dilatate, piloerezione e aumento della pressione arteriosa.
Si può ottenere secrezione degli ormoni della midollare del surrene, adrenalina e noradrenalina, stimolando varie aree ipotalamiche, il ponte, il bulbo e perfino le regioni preottiche. Nella maggior parte dei casi l'effetto della stimolazione elettrica consiste in un aumento della secrezione, ma talvolta questa viene inibita: in questo modo l'attività normale può essere modulata in ambedue le direzioni.
Infine, l'ipotalamo controlla la secrezione di un certo numero di ormoni secreti dall'ipofisi anteriore, alcuni dei quali interagiscono in vari modi con il sistema autonomo, come gli ormoni della corteccia surrenale e l'ormone tiroideo.
b) Funzioni centrali dei neuroni monoamminergici
L'avvento della tecnica della istofluorescenza ha portato alla scoperta nel sistema nervoso centrale di numerosi sistemi di neuroni contenenti catecolammine e serotonina (v. Dahlstrom e Fuxe, 1964). La fluorescenza da catecolammine si distingue da quella da serotonina per il colore verde intenso delle prime rispetto al giallo pallido della seconda. Tuttavia, l'istofluorescenza non consente di distinguere il tipo di catecolammina prodotto da un certo sistema di neuroni, cioè se dopammina, noradrenalina o adrenalina. Tale distinzione è divenuta possibile con l'uso di altre tecniche, tra cui quella della immunoistochimica, già descritta nel cap. 2, § c. Essa permette di distinguere i neuroni adrenergici e noradrenergici da quelli dopamminergici per il fatto che solo i primi contengono l'enzima DBH. La distinzione tra i neuroni adrenergici e quelli noradrenergici, poi, viene eseguita in base al fatto che solo i primi contengono l'enzima PNMT (v. Hökfelt e altri, 1974). Sono stati così distinti tre sistemi di neuroni catecolamminergici nel SNC: neuroni dopamminergici, noradrenergici e adrenergici. I relativi assoni partono da una serie di corpi cellulari situati nel tronco encefalico. Relativamente meglio note nelle loro funzioni sono le vie dopamminergiche e particolarmente il sistema nigro-striatale, al quale limiteremo la nostra descrizione. Il gruppo cellulare da cui questo si forma è situato nella sostanza nera. I suoi assoni formano un importante fascio che, dirigendosi rostralmente, attraversa il globo pallido per terminare nel corpo striato, cioè nel nucleo caudato e nel putamen. Se questo sistema, che è implicato nell'inizio e nell'esecuzione dei movimenti, cessa di funzionare, si determina come conseguenza il morbo di Parkinson, che ha tra i sintomi più caratteristici l'acinesia e la rigidità. La dopammina viene normalmente sintetizzata nei neuroni della sostanza nera, trasportata attraverso i loro assoni al corpo striato e qui liberata alle terminazioni quale neurotrasmettitore. Nel morbo di Parkinson la sostanza nera è danneggiata, con depressione della sintesi e del trasporto della dopammina. Queste conclusioni sono state raggiunte attraverso una serie di importanti scoperte.
Dapprima è stato trovato che la reserpina, alcaloide della Rauwolfia già noto come tranquillante e anti-ipertensivo, produce deplezione di serotonina, noradrenalina e adrenalina nel sistema nervoso sia periferico sia centrale (v. Brodie e altri, 1956; v. Carlsson e Hillarp, 1956). Inoltre era già noto che la reserpina produceva come inatteso effetto collaterale una rigidità di tipo parkinsoniano in pazienti cui veniva somministrata quale anti-ipertensivo. Similmente il trattamento di animali con reserpina produceva sintomi di tipo parkinsoniano. Sono state poi trovate concentrazioni straordinariamente elevate di dopammina nello striato di animali normali, mentre il trattamento con reserpina ne produceva la deplezione, in analogia con gli effetti sulle altre catecolammine e sulla serotonina. Inoltre l'esame autoptico di pazienti parkinsoniani ha rivelato che il corpo striato e la sostanza nera contengono una scarsa quantità di dopammina. Infine è stato mostrato che la somministrazione di L-dopa produce un notevole miglioramento dei sintomi del morbo di Parkinson, tanto che attualmente ne costituisce il trattamento più efficace. La L-dopa attraversa facilmente la barriera ematoencefalica ed è il precursore della dopammina, che da essa si forma per decarbossilazione a opera dell'enzima dopa-decarbossilasi.
10. Farmacologia del sistema autonomo
a) Sistema parasimpatico
1. Farmaci colinergici. - Il neurotrasmettitore naturale del sistema colinergico, l'acetilcolina, è circa mille volte biologicamente più attivo della colina. È stato sintetizzato un gran numero di esteri della colina, la maggior parte dei quali è meno attiva dell'acetilcolina. Le azioni dell'acetilcolina sono state divise in due gruppi, a seconda del tipo di recettore coinvolto. Nel caso dei nervi colinergici postgangliari, il trasmettitore liberato agisce in modo simile alla muscarina, per esempio nel far contrarre la pupilla. Tale effetto è abolito da basse concentrazioni di atropina, fatto che permette l'identificazione di questo gruppo di recettori. Un secondo tipo di effetto è definito nicotino-simile e si manifesta, per esempio, nell'eccitazione di un neurone secondario del sistema nervoso centrale o del sistema nervoso autonomo periferico o nell'attivazione della placca motrice del muscolo scheletrico. Tale effetto non è bloccato dall'atropina a bassa concentrazione, ma è inibito da bloccanti gangliari come l'esametonio o il decametonio. Non vi è un limite netto tra questi due tipi di azione, e in molti casi l'azione degli esteri della colina può essere, a seconda della dose, muscarino-simile o nicotino-simile; se si abolisce l'azione del primo tipo con atropina, si può osservare quella del secondo tipo usando il farmaco a dosi maggiori.
Mentre il neurotrasmettitore naturale, l'acetilcolina, è idrolizzato rapidamente dall'acetilcolinesterasi, che è caratteristicamente localizzata nei luoghi di liberazione dell'acetilcolina, altri esteri della colina, come il carbacolo, non sono attaccati e possono quindi esercitare un'azione prolungata. Alcuni di questi esteri sono usati in terapia come vasodilatatori.
2. Farmaci bloccanti del sistema colinergico. - Si sapeva da tempo che gli alcaloidi di Atropa belladonna inibiscono l'effetto della stimolazione dei nervi parasimpatici e della colina, nonché dei suoi esteri attivi. I più conosciuti sono l'atropina (dl-iosciammina) e la scopolammina (l-ioscina), che esercitano un'azione di blocco sui recettori parasimpatici postgangliari. I loro effetti sono chiamati talvolta antimuscarinici, dal momento che l'alcaloide muscarina, che si ricava dal fungo velenoso Amanita muscaria, riproduce tipicamente l'effetto di stimolazione dei nervi parasimpatici. Le azioni tipiche dell'atropina e della scopolammina sono l'inibizione della secrezione delle ghiandole salivari, lacrimali e sudorifere, la dilatazione della pupilla e la paralisi dell'accomodazione dell'occhio. I movimenti gastrointestinali sono depressi e la frequenza cardiaca è aumentata. A più alte dosi tali farmaci possono anche inibire la trasmissione colinergica a livello delle sinapsi gangliari: tali azioni sono antinicotiniche.
L'atropina non impedisce la liberazione di acetilcolina nelle terminazioni dei nervi, ma compete con il trasmettitore (o con l'acetilcolina sperimentalmente applicata) per i siti del recettore. Mentre il complesso recettore-acetilcolina attiva la cellula effettrice, il complesso recettore-atropina non ha tale azione. L'atropina ha un'azione di blocco reversibile, ma si dissocia solo lentamente dal recettore, per cui la sua azione è di lunga durata.
L'atropina esercita sulle ghiandole sudorifere un'azione di blocco sulla sudorazione termica ed emotiva. Nelle ghiandole salivari l'atropina blocca l'effetto secretorio della stimolazione della corda del timpano, ma non impedisce la vasodilatazione che è causata da un polipeptide (v. anche cap. 2, § c). Inoltre la ioscina previene efficacemente la risposta del bere nei ratti. Un'azione periferica dell'atropina consiste nell'inibire la secrezione dei succhi gastrici, come pure quella del succo pancreatico, evocata da stimolazione vagale. In chirurgia si usa l'atropina per impedire la secrezione nasale, bronchiale e salivare causata dall'anestesia con etere.
L'effetto stimolante dell'attivazione parasimpatica e dei farmaci colinergici sulla muscolatura liscia può essere impedito dall'atropina, per esempio nell'intestino e nei bronchi. Tuttavia l'effetto dell'atropina sulla motilità intestinale e sulla risposta dell'intestino alla stimolazione parasimpatica e ai farmaci colinergici è di natura complessa poiché dipende in parte da una inibizione della stimolazione nicotino-simile dei gangli.
L'applicazione locale di atropina nel sacco congiuntivale provoca dilatazione della pupilla inibendo il muscolo circolare che fa restringere la pupilla.
Clinicamente, l'atropina o la scopolammina vengono usate nello spasmo bronchiale, nello spasmo gastrointestinale e nell'ipersecrezione gastrica, sebbene gli effetti siano variabili. Molti derivati dell'atropina e altri farmaci colinergici sono stati provati con vario successo allo scopo di ridurre gli effetti collaterali.
Nel sistema cardiovascolare l'atropina provoca accelerazione cardiaca bloccando l'azione inibitoria del tono vagale continuo. Essa migliora anche la conduzione atrioventricolare, che è rallentata dalla stimolazione vagale. Contrariamente all'atropina, la scopolammina diminuisce la frequenza cardiaca, probabilmente a causa di una più forte azione centrale. Nell'uomo l'atropina non ha grande influenza sulla pressione del sangue; ciò dimostra che il sistema vascolare periferico è controllato soltanto in grado minimo da nervi vasomotori colinergici.
Si sono notati vari effetti centrali dell'atropina, alcuni dei quali sono dovuti a un'azione diretta sulle strutture nervose, mentre altri dipendono dall'effetto di blocco sui recettori colinergici. L'effetto sul bulbo e sui suoi centri nervosi è generalmente di modesta entità.
Nell'ipotalamo, che è il principale centro di regolazione autonoma, si è osservato che l'atropina ha alcuni effetti depressivi. È probabile che questi siano principalmente di natura antinicotinica.
I centri superiori sembrano reagire in modo diverso all'atropina e alla scopolammina. Così l'atropina in piccole dosi ha solo un effetto modesto, mentre la scopolammina ha un'azione ipnotica, che è anche usata clinicamente. Ad alte dosi si è visto che l'atropina è efficace nel controbilanciare l'azione di alcuni anticolinesterasici che impediscono la normale inattivazione dell'acetilcolina.
3. Inibitori della colinesterasi. - Un'azione anticolinesterasica era nota e anche utilizzata molto tempo prima che l'acetilcolina venisse scoperta. Infatti erano note da secoli le proprietà della fava del Calabar, che contiene fisostigmina (eserina).
L'eserina appartiene al gruppo degli inibitori reversibili della colinesterasi (ChE). Lo sviluppo delle conoscenze sugli inibitori irreversibili della ChE appartenenti al gruppo degli organofosfori è intimamente connesso con gli studi che hanno portato alla produzione dei cosiddetti gas nervini, usati sia a scopo bellico sia nella preparazione di insetticidi. Data la loro capacità di aumentare efficacemente l'attività dell'intero sistema parasimpatico inibendo la distruzione del trasmettitore, è forse sorprendente che tali farmaci abbiano trovato scarso uso in terapia.
Come precedentemente affermato, nell'organismo si trovano due tipi di colinesterasi, l'acetilcolinesterasi (AChE) specifica, e un secondo tipo, generalmente chiamato butirricolinesterasi (BuChE) perché è molto attivo nello scindere la butirrilcolina.
L'inibizione reversibile può essere competitiva o non competitiva. Tale reazione avviene o nel sito anionico o in quello estereo, oppure in entrambi. Nell'inibizione irreversibile, soprattutto con gli agenti organofosforici, l'atomo di fosforo si lega strettamente all'enzima. Gli enzimi fosforilati sono riattivati lentamente per idrolisi, spontaneamente, ma questa reazione può essere accelerata da alcuni composti di adeguata costituzione chimica, come lo iodometilato di piridina-2-aldossima.
Le colinesterasi di entrambi i tipi sono largamente distribuite nel sistema nervoso autonomo. I neuroni pregangliari colinergici centrali, che sono in connessione con le fibre autonome, hanno attività di AChE da moderata ad alta. L'enzima si trova nelle terminazioni nervose di alcune fibre pregangliari, che spesso sono divise in tre classi a seconda del loro contenuto di AChE. Le fibre colinergiche postgangliari sono, tuttavia, uniformemente ricche in AChE. Le cellule di Schwann che circondano le porzioni terminali delle fibre autonome sono ricche di BuChE. AChE si trova in piccole quantità anche nelle fibre nervose adrenergiche.
Mentre l'AChE è presente in tutti gli organi che contengono nervi pregangliari o fibre colinergiche postgangliari, il secondo tipo di enzima, BuChE, si trova nel tessuto non nervoso sparso in tutto il corpo.
L'eserina appartiene ai composti azotati terziari, mentre la neostigmina, la prostigmina e l'edrofonio sono quaternari. L'ambenonio è considerato particolarmente specifico nei confronti dell'AChE. È anche interessante il fatto che la tremorina, che è uno stimolante centrale colinomimetico, possieda una debole azione anti-ChE.
Numerosi anti-ChE irreversibili sono stati sintetizzati e studiati con particolare attenzione alla loro azione come insetticidi (v. pesticidi) e potenziali gas nervini. Tra i più potenti inibitori vi sono i composti quaternari organofosforici. È stata riscontrata una certa differenziazione in relazione all'effetto inibitorio sull'AChE e sulla BuChE: composti come il diisopropilfiuorofosfato (DFP) o fluoruro di di-iso-propossifosforile e l'analogo mipafox sembrano abbastanza specifici per la BuChE.
Gli anticolinesterasici sono stati trovati molto utili nell'analisi delle funzioni del sistema autonomo, particolarmente per quanto concerne la sua parte parasimpatica o colinergica. Il potenziamento di una reazione fisiologica dopo somministrazione di un anti-ChE è una valida prova di un meccanismo colinergico. In questo modo è stato possibile mettere in luce meccanismi di questo tipo nel midollo spinale e in altre parti del sistema nervoso centrale e la loro presenza è stata convalidata dal rinvenimento di vescicole sinaptiche e di potenziali in miniatura in tali aree.
L'ormone antidiuretico è liberato dall'ACh o da un anti-ChE iniettato per via endovenosa o locale. La nicotina ha lo stesso effetto. Anche in altri casi queste sono indicazioni che nelle funzioni centrali sono implicati meccanismi colinergici. D'altra parte la modesta produzione di ACh nel sistema nervoso centrale e la presenza di un piccolo numero di cellule colinocettive suggeriscono che le sinapsi colinergiche centrali sono presenti solo in misura limitata.
Effetti anti-ChE nelle parti periferiche del sistema autonomo sono stati descritti per diversi tipi di tessuti e organi. Un aumento di secrezione salivare è causato dagli anti-ChE con stimolazione sia simpatica sia parasimpatica. Similmente questi farmaci causano lacrimazione e aumentano la sudorazione e la secrezione di succhi gastrici e intestinali.
La muscolatura bronchiale come pure quella intestinale, particolarmente la circolare, sono contratte dagli anti-ChE. Nell'occhio gli anti-ChE provocano contrazione della pupilla e spasmo dell'accomodazione. La frequenza cardiaca viene diminuita e si produce vasodilatazione in alcune aree senza alterare significativamente la pressione del sangue.
Negli organi innervati dal simpatico, come la membrana nittitante e il canale deferente, dopo somministrazione di anti-ChE si osserva un effetto di contrazione probabilmente dovuto alla presenza in essi di fibre colinergiche. Nel ratto il modesto effetto vasocostrittore della stimolazione a basse frequenze dei nervi mesenterici viene aumentato dagli anti-ChE. L'analisi del supposto legame colinergico degli organi innervati dal sistema adrenergico è complicata dal fatto che l'acetilcolina in modeste concentrazioni inibisce l'effetto della stimolazione nervosa adrenergica, ma lo aumenta quando le concentrazioni sono molto basse.
b) Sistema simpatico
1. Farmaci simpaticomimetici. - Un gran numero di farmaci agisce su diversi tipi di organi e di processi biochimici producendo effetti simili a quelli della noradrenalina e della adrenalina; essi sono stati perciò chiamati farmaci simpaticomimetici.
Esaminando gli effetti di tali farmaci si è osservato che alcuni di essi cessano di agire in assenza di nervi simpatici. Si è dunque concluso che essi agiscono liberando il trasmettitore dai nervi adrenergici. Farmaci di tal genere vengono denominati generalmente ammine ad azione indiretta. Altri farmaci esercitano la loro azione, simile a quella dell'adrenalina e della noradrenalina, anche in assenza di nervi (ammine ad azione diretta). Non si può stabilire una netta linea di demarcazione fra questi gruppi, anche perché alcuni farmaci esercitano un'azione mista. L'effetto dipende anche dal tipo di organo usato per l'esame. Nella tab. V sono state sistemate nei corrispondenti gruppi un certo numero di ammine simpaticomimetiche.
Mentre tutte le ammine ad azione indiretta esercitano lo stesso tipo di azione, cioè liberano noradrenalina, l'effetto di quelle ad azione diretta può variare, a seconda che esse abbiano proprietà di stimolazione α o β. Esempi caratteristici di ammine che stimolano i recettori α, oltre al trasmettitore naturale, la noradrenalina, sono la dopammina e l'α-metilnoradrenalina, mentre l'isopropilnoradrenalina (isoprenalina) ha tipiche proprietà β-stimolanti. Dunque la noradrenalina fa contrarre la maggior parte dei vasi e, per esempio, il dilatatore della pupilla, mentre l'isopropilnoradrenalina non ha effetto vasocostrittore, ma fa aumentare la frequenza cardiaca e rilassare la muscolatura bronchiale.
Alcune ammine simpaticomimetiche hanno anche altri effetti. Così l'efedrina e l'amfetammina, che sono ambedue ammine ad azione indiretta, inibiscono la monoamminossidasi e possono in tal modo potenziare l'azione dei nervi simpatici, per esempio dopo reserpina.
Nella maggior parte dei casi le ammine simpaticomimetiche non penetrano nel cervello o vi entrano solo in concentrazioni molto basse a causa della barriera ematoencefalica. L'amfetammina presenta un più alto grado di solubilità nei lipidi e pertanto attraversa questa barriera più facilmente, determinando così una marcata eccitazione centrale, in parte dovuta a liberazione di noradrenalina nel sistema nervoso centrale.
Anche la dopa, precursore del trasmettitore, entra nel sistema nervoso centrale dove viene decarbossilata a dopammina che è o captata nei neuroni dopamminergici o ulteriormente traformata in noradrenalina.
In aggiunta alla noradrenalina e all'adrenalina, molti farmaci simpaticomimetici hanno trovato impiego terapeutico. Le azioni più utilizzate sono quelle che hanno effetto stimolante sul cuore e che aumentano la pressione del sangue per vasocostrizione.
Diversi farmaci sono stati usati per produrre broncodilatazione in condizioni allergiche, tra cui l'asma. Alcuni di questi farmaci sono preferiti alla noradrenalina (per gli effetti α) e all'adrenalina (per effetti misti α e β), poiché sono meno prontamente inattivati nell'organismo dalla monoamminossidasi (MAO) o dalla catecol-O-metiltransferasi (COMT). Così i derivati α-metilici non sono attaccati dalla MAO, e i composti non idrossilati nell'anello benzenico non sono inattivati dalla COMT. Tali composti hanno dunque un'azione più duratura (metaraminolo, efedrina) e possono essere attivi anche per assunzione orale.
2. Inibitori della sintesi. - La produzione del neurotrasmettitore adrenergico può essere ridotta o impedita da un certo numero di composti che agiscono come inibitori degli enzimi che partecipano alla biosintesi della noradrenalina. Alcuni di questi vengono impiegati in terapia per limitare l'attività del sistema adrenergico.
La trasformazione della tirosina in dopa, per opera dell'enzima tirosinaidrossilasi, è quella che limita la velocità ed è pertanto in grado di inibire efficacemente la sintesi. Tra i composti che agiscono come inibitori di questa trasformazione si possono ricordare la dopacetammide e l'a-metil-p-tirosina col suo estere dimetilico. Queste ultime sostanze possono far insorgere sintomi di grave deficienza di noradrenalina. Inoltre l'inibizione di tale stadio della biosintesi è provocata normalmente dai prodotti della sintesi (dopammina e noradrenalina), con un meccanismo dunque di regolazione a feedback (inibizione da prodotto).
La dopadecarbossilasi può essere inibita da certi derivati idrazinici, quali la N-metil-N-(3-idrossibenzil)idrazina. Un inibitore efficace è il decaborano, un idruro del boro (B10H14) che agisce inattivando il cofattore enzimatico piridossal-5′-fosfato. Dopo somministrazione di decaborano, il contenuto in noradrenalina della maggior parte degli organi scende a valori bassi per 24-48 ore, con conseguente deficienza funzionale dei nervi adrenergici.
La dopammina-β-idrossilasi è inibita dall'idrossibenzilossiammina e dal disulfiram, che agisce da inibitore dell'enzima dopo formazione del dietilditiocarbammato in presenza di acido ascorbico.
3. Farmaci che bloccano l'inattivazione. - Il trasmettitore adrenergico è metabolizzato principalmente dalla monoamminossidasi (MAO) e dalla catecol-O-metiltransferasi (COMT). Si conoscono diversi composti che inibiscono l'azione di questi enzimi. Probabilmente a causa dell'esistenza di altri sistemi di inattivazione, l'azione di tali composti nell'organismo non è particolarmente efficace, salvo alcuni effetti sul sistema nervoso centrale. L'effetto antidepressivo dell'inibitore della MAO iproniazide ha portato all'uso di tale farmaco in terapia, ma siccome è stato in seguito provato che esso ha effetti epatotossici, sono stati utilizzati altri inibitori della MAO.
Alcune ammine simpaticomimetiche hanno effetti stimolanti sul sistema nervoso centrale, che vengono utilizzati in terapia. L'adrenalina o la noradrenalina non possono essere direttamente utilizzate a questo scopo, poiché non attraversano la barriera ematoencefalica. Alcuni dei più potenti inibitori della MAO (fenelzina, feniprazina e tranilcipromina) sono strutturalmente correlati con le ammine simpatiche e agiscono prevalentemente sul sistema nervoso centrale, mentre le loro azioni simpaticomimetiche periferiche sono relativamente deboli.
Le ammine simpaticomimetiche amfetammina ed efedrina agiscono sulla MAO in vitro, ma non sembrano esercitare tale azione in vivo. La loro azione è in parte diretta, particolarmente nel caso dell'amfetammina, ma esse inibiscono anche la ricaptazione del trasmettitore e quindi potenziano la sua azione. Non vi è stretta correlazione tra la presenza di noradrenalina e di MAO nel sistema nervoso centrale.
4. Agenti di blocco adrenergico. - Come descritto precedentemente (v. cap. 5, § b), il tipo di azione che i farmaci simpaticomimetici hanno su differenti tessuti, organi e cellule ha portato al concetto di recettori specifici, generalmente chiamati recettori α e β. I recettori adrenergici α mediano l'eccitazione della muscolatura liscia vascolare e delle cellule ghiandolari e causano, dopo stimolazione, rilassamento di alcune parti dell'intestino, mentre i recettori β sono responsabili dell'inibizione del tono dei muscoli lisci, compresi quelli dell'intestino, e provocano stimolazione del miocardio. I farmaci inibitori dei recettori sono di regola più attivi sugli effetti delle ammine simpaticomimetiche aggiunte che su quelli della stimolazione dei nervi adrenergici. È interessante notare che quasi tutti gli agenti simpaticomimetici agiscono su entrambi i tipi di recettori, sebbene in gradi diversi, mentre la specificità degli agenti di blocco sembra essere assai più grande.
Farmaci che bloccano i recettori α. Ricerche farmaceutiche hanno portato alla scoperta di un certo numero di agenti di questo tipo che hanno suscitato un notevole interesse, poiché è spesso utile ridurre gli effetti biologici dell'attività dei nervi adrenergici. Le aloalchilammine, delle quali è un esempio tipico la dibenammina, producono un effetto più completo e duraturo degli altri α-bloccanti e di norma hanno un'alta specificità. La frazione β-aloalchilica è fortemente reattiva. Di solito l'azione è lenta all'inizio, forse in dipendenza dal tempo richiesto per la formazione di intermediari della reazione. Durante la prima fase dell'azione una catecolammina può diminuire il blocco per competizione al sito del recettore, ma dopo che il blocco si è sviluppato cpmpletamente, le catecolammine non hanno azione competitiva. Il blocco ha lunga durata, con un tempo di dimezzamento di circa 24 ore. Le aloalchilammine sono altamente solubili nei lipidi, ma scarsamente in acqua.
Inibendo la ricaptazione del trasmettitore, le aloalchilammine possono esercitare un iniziale effetto simpaticomimetico.
Sebbene gli alcaloidi della segale cornuta siano i più attivi di tutti gli α-bloccanti, non sono così specifici nella loro azione. Tra gli effetti collaterali possono essere ricordate la stimolazione della muscolatura liscia e l'azione centrale. I dudroderivati (Hydergina) mostrano un accresciuto potere di blocco adrenergico, mentre esercitano un'azione più debole sulla muscolatura liscia.
Fra i derivati della imidazolina, la tolazolina e la fentolammina hanno effetti relativamente deboli e di breve durata. Questi composti hanno generalmente una bassa specificità e producono una serie di effetti collaterali, particolarmente rilevanti nel caso della tolazolina.
Le benzodiazepine come l'azapetina sono relativamente efficaci come α-bloccanti in quanto causano blocco competitivo. Sono stati descritti alcuni effetti riferibili ad azioni centrali, ma non sappiamo se questi siano dovuti a blocco dei recettori adrenergici centrali α.
Diversi altri composti esercitano attività di blocco a-adrenergico (benzodiossano, iohimbina, clorpromazina), ma determinano anche molti altri effetti.
Gli effetti periferici degli agenti α-bloccanti adrenergici dipendono in maniera rilevante dal grado di tono simpatico e dal tipo di organo esaminato. L'effetto sul cuore è piccolo, ma può essere talvolta forte sul letto vascolare, per esempio nella posizione eretta. L'inversione dell'effetto vascolare dell'adrenalina sulla pressione del sangue mediante un α-bloccante adrenergico dipende dal duplice effetto dell'adrenalina sui recettori α-vasocostrittori e su quelli fi-vasodilatatori. Quando si bloccano solo i primi, prevale la vasodilatazione e la pressione arteriosa cade.
L'effetto vasocostrittore dovuto ai recettori a è stato osservato nelle aree renale, cutanea (ma non per ciò che riguarda l'arrossire), splancnica e dei vasi scheletrici; tale effetto è perciò inibito da agenti α-bloccanti adrenergici. Si sono notati effetti di scarsa entità sui vasi cerebrali, polmonari e coronarici.
Per quanto riguarda il sistema nervoso centrale, che contiene una trama di fibre adrenergiche e probabilmente recettori, non è stato possibile dimostrare con assoluta certezza effetti di agenti di blocco adrenergico che possano attribuirsi all'azione sui recettori α.
Negli organi a muscolatura liscia e nelle ghiandole gli agenti α-bloccanti provocano inibizione di quella parte dell'azione simpatica che è dovuta ai recettori α. Sugli organi a doppia innervazione un effetto di questo tipo può causare solo una lieve alterazione funzionale.
Farmaci che bloccano i recettori β. La dimostrazione di un'attività β-bloccante è di data relativamente recente: il primo bloccante specifico, il dicloroisoproterenolo, è stato introdotto solo nel 1958. Da allora sono stati sintetizzati e usati terapeuticamente diversi efficaci β-bloccanti, alcuni dei quali, oltre all'azione di blocco, hanno effetti diretti. I β-bloccanti meglio conosciuti sono il pronetalolo, il propranololo, l'alprenololo, i composti MJ 1998 e 1999, e l'Inpea. L'azione di blocco sembra essere specifica, come si può vedere per esempio nel cuore. Pertanto le risposte inotrope e cronotrope positive agli stimoli adrenergici scompaiono, mentre gli α-bloccanti adrenergici non modificano tali effetti.
L'effetto dei β-bloccanti adrenergici sui vasi coronarici e polmonari è piccolo, e ciò significa che il ruolo dei β-recettori in questi letti vascolari è modesto. Molti organi, come l'utero e l'intestino, contengono recettori sia α sia β. Nell'utero l'azione inibitoria dell'adrenalina e dell'isoproterenolo è soppressa dai β-bloccanti, il che dimostra che il rilassamento del miometrio è dovuto all'attivazione dei β-recettori.
L'azione dei β-bloccanti sugli effetti metabolici degli stimoli adrenergici è variabile, ma si può dimostrare anche un effetto inibitorio per la glicogenolisi indotta dall'adrenalina. Lo stesso vale per l'effetto lipolitico e per l'effetto attivante sulla formazione di AMP ciclico.
In terapia i β-bloccanti sono usati primariamente come inibitori dell'eccessiva attività adrenergica nel cuore.
5. Agenti di blocco neuronale. - Si è notato che alcuni farmaci interferiscono con la liberazione del trasmettitore provocando il blocco del neurone. Farmaci di questo tipo sono il bretilio, la guanetidina, la xilocolina e la betanidina. La somministrazione di questi farmaci blocca gli effetti della stimolazione nervosa adrenergica, e pertanto essi sono specifici per tale genere di nervi autonomi; tuttavia le cellule effettrici rispondono nel modo usuale.
Gli agenti di blocco neuronale inibiscono la conduzione degli impulsi nervosi nelle terminazioni del nervo, ma non nei tronchi. La loro azione è stata associata a un effetto anestetico locale, limitato alle porzioni terminali dell'assone. Il blocco della liberazione di trasmettitore causa un certo aumento delle riserve, per cui, dopo somministrazione di bretilio, si trovano maggiori quantità di noradrenalina negli organi.
Poiché i farmaci di tale genere prevengono la liberazione del trasmettitore, vengono largamente impiegati in alcune malattie, come certi tipi di ipertensione, i cui sintomi si ritiene che siano almeno in parte sostenuti da un'eccessiva azione simpatica.
Questi farmaci causano un moderato rialzo della pressione arteriosa, dovuto probabilmente a una liberazione di noradrenalina dalle riserve e a un'inibizione della ricaptazione. Tale effetto è accresciuto dalla reserpina.
6. Inibitori della captazione. - Nel gatto, stimolando i nervi adrenergici che vanno alla milza perfusa, è possibile riscontrare la presenza del trasmettitore nel liquido di perfusione. A basse frequenze di stimolazione, la quantità di noradrenalina che compare nel sangue venoso che fuoriesce dall'organo è piccola, ma dopo somministrazione di agenti α-bloccanti adrenergici, quali fentolammina, fenossibenzammina (FBA) o Hydergina, essa aumenta in maniera rilevante, fino a raggiungere una quantità 5 volte maggiore. Questo effetto viene spiegato come conseguenza dell'inibizione della ricaptazione del trasmettitore liberato. Tale captazione, riscontrabile sia nelle terminazioni dei nervi adrenergici sia in altre cellule, è considerata un importante meccanismo per l'inattivazione fisiologica del trasmettitore liberato: concetto questo che è validamente sostenuto dalla scoperta che la captazione è molto ridotta negli organi sottoposti a denervazione simpatica.
In base ad altri esperimenti sulla milza perfusa di gatto si è concluso che il meccanismo più importante per il mantenimento di un livello costante di noradrenalina nel neurone, durante un'aumentata attività nervosa, è una ricaptazione quasi quantitativa della noradrenalina liberata dai neuroni, cosa che può essere prevenuta da fenossibenzammina. D'altra parte la fenossibenzammina aggiunta al liquido di perfusione riduce fortemente o abolisce completamente l'iperflusso di risposta alla tirammina, probabilmente prevenendo la sua captazione.
Si sono ottenuti simili risultati usando altri bloccanti della captazione, come la cocaina, la demetilimiprammina (DMI) e altri, che agiscono sulla membrana dell'assone e impediscono il passaggio o l'entrata del trasmettitore. È degno di nota il fatto che gli α-bloccanti adrenergici sono particolarmente efficaci sotto questo aspetto; non si dovrebbe trascurare la possibilità di interazione con i siti del recettore.
Gli studi sulla captazione della noradrenalina hanno dimostrato che, somministrando l'ammina in più alte concentrazioni, l'inibizione della captazione seguiva uno schema diverso da quello osservato con basse concentrazioni. Il primo tipo di captazione menzionato è stato denominato captazione II al fine di distinguerlo dal secondo tipo, che è stato denominato captazione I. Sembra che la captazione I corrisponda primariamente all'assorbimento nei depositi specifici, e che la captazione II sia invece largamente aspecifica e temporanea.
La somministrazione dei bloccanti della captazione fa aumentare la concentrazione del neurotrasmettitore a livello dei recettori, causando una maggiore attività. Lo stesso fenomeno è stato dimostrato con l'aggiunta di noradrenalina.
La captazione II è fortemente inibita dalla normetanefrina. La risposta vascolare della milza perfusa di gatto a treni di 200 stimoli, applicati alla frequenza di 10 Hz nei nervi splenici, inizialmente è aumentata di più dalla combinazione di normetanefrina e cocaina che dalla cocaina sola: ciò indica un momentaneo processo di captazione II in aggiunta alla captazione I. Similmente l'iperflusso di noradrenalina è inizialmente aumentato di più dalla combinazione dei due farmaci che dalla cocaina sola. Si è concluso che la cocaina inibisce la captazione I e che in queste condizioni una certa quantità del trasmettitore liberato è rimossa dalla captazione II. Il blocco di ambedue i processi di captazione provoca un accresciuto iperflusso, equivalente a 3-4 volte l'originale.
È ancora incerto se la forte azione della FBA sia associata con qualche effetto diverso dall'inibizione della captazione al livello della membrana dell'assone o delle particelle di deposito. Si può prendere in considerazione quest'ultima possibilità, dal momento che la FBA è una sostanza che provoca una potente deplezione, in contrasto con altri inibitori della captazione. A una frequenza di stimolazione di 25/s né la DMI né la FBA aumentano l'iperflusso: ciò indica che i processi di ricaptazione non operano a questa frequenza. È stato osservato che la quantità di noradrenalina liberata per ogni impulso aumenta da 0,56 ng/g a 5/s fino a 1,53 ng/g a 25/s.
Da esperimenti effettuati con stimolazione nervosa sul cuore di coniglio perfuso, si è concluso che la cocaina e la desiprammina aumentano l'iperflusso di noradrenalina principalmente inibendo la ricaptazione, mentre la FBA e la protriptilina aumentano ulteriormente la quantità di noradrenalina liberata dai nervi, probabilmente contrastando alcuni meccanismi frenanti, di cui potrebbero essere responsabili le prostaglandine, che normalmente limitano la liberazione di noradrenalina in risposta alla stimolazione nervosa.
Sebbene esistano prove convincenti che i farmaci esaminati in questa sezione agiscono inibendo il passaggio di noradrenalina attraverso la membrana dell'assone, dovrebbe esser considerata anche la possibilità che questi farmaci interferiscano specificamente con la captazione nei granuli di deposito. Tutti i farmaci menzionati (α-bloccanti adrenergici, cocaina, DMI, protriptilina e i loro affini) inibiscono la captazione e la liberazione di noradrenalina negli specifici granuli di deposito. D'altra parte la capacità di captazione specifica è relativamente piccola e i dati disponibili suggeriscono l'ipotesi che la maggior parte delle ammine normalmente ricaptate venga metabolizzata nelle terminazioni dell'assone e dispersa per diffusione. Se si inibisce la captazione, per esempio con FBA, l'escrezione di noradrenalina libera nell'urina aumenta notevolmente. Si è osservato nei ratti che, anche dopo somministrazione di cocaina, l'escrezione di noradrenalina nell'urina aumenta.
Gli unici composti finora trovati che facilitano la captazione del trasmettitore adrenergico nei granuli nervosi di deposito sono alcuni nucleotidi. Mentre l'ATP è a questo proposito il più attivo, la citidina, l'inosina e l'uridintrifosfato aumentano pure la captazione netta e la ricaptazione della noradrenalina. L'assorbimento dipendente da ATP nei granuli di deposito è inibito dagli α-bloccanti, dalla reserpina, dalla prenilammina, e da alcuni inibitori metabolici che agiscono in differenti punti nella catena di trasporto di elettroni e sulla fosforilazione ossidativa (rotenone, antimicina A, oligomicina, dinitrofenolo, pentaclorofenolo).
7. Reserpina. - È stato trovato che alcuni alcaloidi della pianta indiana Rauwolfia, come la reserpina, svuotano il sistema nervoso centrale degli animali del suo contenuto di 5-idrossitriptammina. Si è visto più tardi che questo era vero anche per la noradrenalina e altre ammine simpaticomimetiche. Oltre a ciò si è osservato che la reserpina causa una perdita del neurotrasmettitore adrenergico in ogni parte del corpo, e anche di adrenalina nelle ghiandole surrenali. Dapprima si era ritenuto che la reserpina causasse una liberazione diretta delle ammine, ma osservazioni su particelle di deposito isolate da nervi adrenergici hanno dimostrato che la deplezione era dovuta all'incapacità di queste particelle di captare e legare il trasmettitore. Questo era il caso specialmente della captazione facilitata dall'ATP. La diretta liberazione del trasmettitore dalle particelle di deposito aumenta solo ad alte concentrazioni di reserpina e questo è probabilmente un processo non specifico. A basse concentrazioni che prevengono la captazione del trasmettitore, la reserpina ritarda la liberazione e annulla quasi completamente il turnover del trasmettitore nei granuli.
L'effetto di svuotamento della reserpina in organi a innervazione simpatica dipende dalla dose e dall'attività di impulsi nei nervi. Se l'attività degli impulsi è intensa, come può essere, per esempio, quella nel cuore, la deplezione avviene rapidamente, cosicché il tempo di dimezzamento della noradrenalina endogena nel cuore di coniglio è di soli 20 minuti, dopo una dose di reserpina di 0,25 mg/kg. Dopo denervazione acuta o decentralizzazione simpatica (procedimenti che aboliscono l'attività di impulsi), lo svuotamento avviene a velocità minore.
Dopo somministrazione di reserpina e susseguente svuotamento dei depositi del trasmettitore, l'effetto della stimolazione nervosa decresce gradualmente, sebbene la sintesi del trasmettitore possa continuare e produrre una risposta debole. Tuttavia è stato dimostrato che anche subito dopo somministrazione di reserpina, ben prima che i depositi siano stati svuotati, la risposta alla stimolazione del nervo può essere diminuita. Questo dato è stato interpretato come una deplezione della piccola quantità di trasmettitore che è immediatamente disponibile per la liberazione e che è continuamente rimpiazzata sia dai depositi granulari, sia dal trasmettitore di nuova sintesi. Dopo reserpina sembra che il riempimento di questo deposito secondario disponibile sia meno efficace, il che conduce a cessazione o diminuzione della liberazione, specialmente se la frequenza degli impulsi del nervo è alta. Anche a una concentrazione di 0,1 μg/ml la reserpina fa diminuire rapidamente la risposta di organi isolati alla stimolazione del nervo. Questo effetto della reserpina, che avviene mentre tutte le riserve sono ancora in gran parte intatte, può essere dovuto a liberazione ritardata dai depositi principali del trasmettitore o a insufficiente captazione e liberazione dai piccoli depositi secondari. È probabile che le conseguenze terapeutiche nell'uomo, osservate con dosi dell'ordine di 0,1-1 mg al giorno, siano dovute a un effetto di questo tipo, piuttosto che a deplezione delle principali riserve. È tipico il fatto che la reserpina usata per il trattamento dell'ipertensione richieda un considerevole tempo di induzione, talvolta settimane, prima che abbia l'effetto desiderato. Dato che tale alcaloide si lega strettamente alle strutture cellulari, inclusi i granuli di riserva, è chiaro che quantità così piccole richiedono un lungo periodo di tempo per raggiungere una concentrazione abbastanza elevata da interferire con la liberazione di trasmettitore dalle terminazioni nervose.
Uno degli effetti centrali più ovvi della reserpina è la sua azione sedativa, che si osserva sia nell'uomo sia negli animali. Essa è dovuta apparentemente all'inibizione della liberazione di noradrenalina nel sistema nervoso centrale. Simili effetti sono riscontrati negli animali dopo somministrazione di inibitori della sintesi della noradrenalina, come il decaborano.
Mentre la reserpina inibisce efficacemente la captazione specifica di noradrenalina, dipendente dall'ATP, non previene la captazione non specifica nei tessuti. Tuttavia l'ammina captata in questo modo è rapidamente perduta di nuovo o metabolizzata dalla monoamminossidasi nelle terminazioni nervose. Studi di istochimica hanno rivelato che la noradrenalina captata in un tessuto trattato con reserpina è distribuita in modo non specifico.
Ci sono prove convincenti che la nuova sintesi del trasmettitore continui a una velocità moderatamente ridotta dopo trattamento con reserpina, sebbene la maggior parte di questa sia normalmente inattivata dalla monoamminossidasi. Se l'attività di questo enzima è inibita da farmaci come l'iproniazide o la nialammide, la noradrenalina formata viene protetta e il contenuto negli organi aumenta. Questo normalmente dovrebbe inibire la sintesi, ma si osserva invece che il trasmettitore è liberato e la sintesi continua. Come conseguenza della somministrazione combinata di reserpina e di un inibitore della monoamminossidasi, si determina una forte azione simpatica, che è causa di aumento della pressione sanguigna e della frequenza cardiaca; questo indica che vi è una incontrollata liberazione di trasmettitore. Se a un animale dopo reserpina viene somministrato l'analogo poco attivo della nicotina, il bromuro di iso-monometilnicotinio, anche la sua azione aumenta in maniera notevole, provocando una maggiore liberazione del trasmettitore.
L'effetto plurivalente della reserpina sulla neurotrasmissione adrenergica complica il suo impiego terapeutico, particolarmente quando essa è usata in combinazione con altri farmaci. Tuttavia le sue azioni principali sono la prevenzione del legame specifico con le particelle di deposito e la ritardata liberazione del trasmettitore; in questo modo essa riduce l'attività dei nervi simpatici. Tuttavia, questo effetto può essere invertito in presenza di altri farmaci.
c) Farmaci nicotinici
Le prime osservazioni che la nicotina in alte concentrazioni impediva agli impulsi nervosi di passare dai neuroni pregangliari a quelli postgangliari nel sistema nervoso autonomo diressero l'attenzione verso questo potente farmaco. A basse concentrazioni, la nicotina agisce come stimolante gangliare. Essa esercita pure un'azione stimolante sulle terminazioni nervose, determinando in tal modo la liberazione del trasmettitore, e inoltre agisce direttamente sui recettori nicotinici nelle cellule effettrici. La nicotina è un potente stimolante delle cellule cromaffini della midollare del surrene e provoca secrezione intensa, ma di breve durata, degli ormoni della midollare. La breve azione è dovuta al rapido svilupparsi di una autoinibizione, che si riscontra pure per l'acetilcolina e per altri farmaci che hanno azione nicotinosimile, come la dimetilfenilpiperazina (DMPP). Si ritiene che l'azione inibitoria sugli effetti della stimolazione dei nervi sia dovuta a un blocco da persistente depolarizzazione.
I più semplici composti ad azione nicotino-simile sono la piperidina e la pirrolidina, che si formano nel corpo e si trovano costantemente come prodotti di escrezione della nicotina nell'urina. Questi composti sono presenti anche nel sistema nervoso centrale e possono esercitare alcuni speciali tipi d'azione nicotino-simile.
Gli analoghi quaternari della nicotina, come il bromuro di iso-monometilnicotinio, hanno solo una modesta azione biologica, perché non penetrano nella membrana dell'assone. Tuttavia, dopo somministrazione di composti come la reserpina, che alterano la permeabilità della membrana, i composti quaternari esercitano azioni simili alla nicotina terziaria.
L'alta tossicità della nicotina è dovuta al suo generale effetto paralizzante sulla trasmissione gangliare. A basse concentrazioni prevalgono le azioni stimolanti sulle funzioni autonome.
11. Controllo dello sviluppo del sistema autonomo
a) Introduzione
Il problema dello sviluppo del sistema autonomo è parte del più generale problema della formazione, durante l'ontogenesi, di quella rete di neuroni estremamente complessa che costituisce il sistema nervoso centrale e periferico. Di fatto, il sistema nervoso autonomo offre un modello relativamente semplice per lo studio del suo sviluppo, essendo costituito alla periferia da due soli neuroni in contatto sinaptico tra di loro: il neurone pregangliare e quello postgangliare. Contribuisce in modo determinante alla semplicità del modello il fatto che i neuroni autonomi sono ben identificati dal punto di vista del trasmettitore chimico: è colinergico, infatti, il neurone pregangliare e adrenergico (simpatico) o colinergico (parasimpatico) quello postgangliare.
Nei gangli simpatici, quali l'intensamente studiato ganglio cervicale superiore (GCS), esistono caratteristiche biochimiche molto utili per gli studi di ontogenesi. La colinoacetilasi (ChAc), l'enzima che catalizza la sintesi di acetilcolina, è contenuta in elevata concentrazione nelle terminazioni simpatiche pregangliari ed è un buon indice dello sviluppo dei neuroni colinergici pregangliari. Lo sviluppo dei neuroni postgangliari adrenergici può invece essere seguito attraverso la sequenza degli enzimi che sintetizzano le catecolammine: la tirosinaidrossilasi (TH), che catalizza il primo passaggio da tirosina a L-dopa; la dopadecarbossilasi (DDC), che converte la L-dopa in dopammina; la dopammina-β-idrossilasi (DBH), che trasforma la dopammina in noradrenalina (NA). Inoltre le tecniche di istofluorescenza da formaldeide di Falck e Hillarp (v. Falck, 1962) e quelle di immunoistochimica consentono la dimostrazione morfologica dei neuroni adrenergici.
Benché lo sviluppo del sistema nervoso autonomo, come quello degli altri componenti dell'organismo, avvenga per la più gran parte durante la vita embrionale, esso si completa solamente durante i primi periodi della vita extrauterina.
b) Sviluppo embrionale
1. Neuroni postgangliari. - I neuroni autonomi prendono origine da una struttura embrionale transitoria chiamata cresta neurale, situata dorsalmente al tubo neurale. Benché le possibilità differenziative delle cellule della cresta siano ormai molto limitate, esse possono ancora dar luogo a vari tipi cellulari, oltre ai neuroni autonomi: i neuroni dei gangli sensitivi, le cellule cromaffini della midollare surrenale, le cellule ‛C' della tiroide, produttrici di calcitonina, i melanociti e le cellule mesenchimali che formeranno i tessuti ossei e connettivali della testa. Le cellule della cresta neurale, inizialmente omogenee, vanno incontro a differenziazione durante e dopo la loro migrazione (un fondamentale processo embrionale) lungo direzioni ben definite per ogni livello del corpo. L'ambiente cellulare in cui le cellule migrano svolge un ruolo essenziale nel determinare sia il quadro dei movimenti migratori sia la differenziazione. Per quanto riguarda i neuroni autonomi, essi derivano da quella popolazione di cellule della cresta neurale che migra ventralmente, da ambo i lati, nel mesenchima somitico. La crescita e la differenziazione dei neuroni autonomi dipendono dall'interazione tra l'informazione genetica contenuta nel neurone primitivo e l'ambiente, appunto, del mesenchima somitico.
Una tappa cruciale nello sviluppo dei neuroni autonomi è la scelta del mediatore chimico colinergico o adrenergico. L'ambiente in cui migrano i simpatoblasti primitivi ha grande importanza nel determinare questa scelta, come è illustrato da esperimenti di trapianto di cellule della cresta neurale di quaglia in embrioni di pollo o viceversa (v. LeDouarin e Teillet, 1974). Le cellule di quaglia si distinguono facilmente da quelle di pollo per le caratteristiche morfologiche del nucleo. Normalmente la regione del ‛tronco' della cresta neurale dà origine ai neuroni gangliari simpatici adrenergici e alle cellule della midollare surrenale, mentre la regione ‛vagale' (così chiamata perché da essa si formano anche i neuroni postgangliari del parasimpatico vagale) dà origine ai neuroni colinergici dei gangli enterici. Quando la cresta del ‛tronco' di quaglia viene trapiantata nella regione ‛vagale' dell'embrione di pollo, le cellule di quaglia vanno a popolare i gangli enterici del pulcino. Le cellule del tronco di quaglia che hanno migrato in queste sedi per esse anormali non mostrano fluorescenza come avrebbero normalmente fatto ed esibiscono invece le proprietà dei neuroni colinergici. Similmente l'esperimento inverso mostra che se si trapiantano cellule della cresta neurale di quaglia della regione ‛vagale' (normalmente a destino colinergico) nella regione del ‛tronco' del pulcino, la midollare surrenale di quest'ultimo mostra numerose cellule di quaglia con la fluorescenza caratteristica delle cellule adrenergiche. Si può quindi concludere: 1) che strade migratorie specifiche sono connesse a ciascun livello della cresta neurale; 2) che l'espressione del fenotipo colinergico o adrenergico viene regolata dall'ambiente incontrato lungo la strada e nella sede definitiva di migrazione.
Si possono fare due ipotesi circa il meccanismo d'azione dei fattori ambientali. La prima ipotesi è che l'ambiente si limiti a selezionare cellule già irreversibilmente determinate a divenire colinergiche o adrenergiche. La seconda ipotesi è che i fattori ambientali siano invece in grado di indurre un nuovo o diverso mediatore chimico in cellule pluripotenti o in cellule in cui la scelta dell'uno o dell'altro mediatore sia ancora reversibile. Eleganti esperimenti di coltura in vitro di neuroni autonomi mostrano che nella realtà si verifica la seconda ipotesi, rendendo quindi altamente probabile l'assunto che l'azione del microambiente embrionale sia induttiva e non selettiva.
Rispetto agli studi in vivo, la coltura in vitro ha il vantaggio di poter tenere sotto controllo la composizione dell'ambiente in cui i neuroni si sviluppano, ambiente costituito sia dal liquido di coltura sia da altri elementi cellulari eventualmente coltivati assieme ai neuroni. Possono così essere più facilmente studiati i fattori ambientali che inducono o controllano particolari funzioni cellulari, quale appunto la scelta del trasmettitore chimico. Molti di questi esperimenti sono stati eseguiti, su neuroni immaturi ottenuti da gangli simpatici di ratti neonati, da un gruppo di ricercatori della Facoltà di Medicina di Harvard.
Condizione indispensabile per la crescita in vitro dei neuroni autonomi è la presenza del fattore di accrescimento nervoso NGF (Nerve Growth Factor) in analogia con quanto mostrato, per lo sviluppo dei medesimi neuroni nell'animale intatto, da Rita Levi-Montalcini (v. § d; v. neurogenesi). I neuroni in coltura sviluppano estesi prolungamenti, si ingrandiscono e acquisiscono molte caratteristiche normali, quali la capacità di generare impulsi nervosi e la presenza alla loro superficie di recettori per l'acetilcolina (il mediatore chimico liberato dai neuroni centrali che normalmente li innervano, cioè i neuroni pregangliari colinergici). A differenza di queste proprietà, il tipo di mediatore chimico elaborato, acetilcolina (ACh) o noradrenalina (NA), dipende dalla presenza o assenza nella coltura di cellule non neuronali.
Quando i neuroni gangliari simpatici vengono coltivati da soli, cioè in assenza di cellule non neuronali, essi si differenziano in senso noradrenergico, comportandosi in tal modo non diversamente da come avrebbero fatto nello sviluppo in vivo. Così essi sintetizzano e immagazzinano NA partendo dall'amminoacido precursore tirosina (v. Mains e Patterson, 1973). La loro natura adrenergica è anche mostrata dai caratteri delle sinapsi che essi formano tra di loro (e solo tra di loro, dato che mancano altre cellule bersaglio). Tali sinapsi sono chiaramente evidenziabili morfologicamente, alla microscopia elettronica, e appaiono caratterizzate dalla presenza delle piccole vescicole a nucleo denso tipiche delle terminazioni adrenergiche, ove costituiscono il luogo di deposito della NA. Funzionalmente, invece, tali sinapsi non sono evidenziabili, a causa della discrepanza tra il mediatore chimico liberato (noradrenalina) e i recettori postsinaptici del soma neuronale che sono invece colinergici, come più sopra esposto. È questo un fenomeno di per sè interessante, in quanto costituisce uno dei rari casi finora documentati di sinapsi elettricamente silenti.
Quando invece i neuroni simpatici sono coltivati assieme ad altre cellule non neuronali, quali i miotubi scheletrici o i miociti cardiaci, essi si differenziano in senso colinergico (v. O'Lague e altri, 1974). Formano infatti sinapsi colinergiche tra di loro, non più elettricamente silenti, ma a carattere eccitatorio e, come ci si attenderebbe, di tipo nicotinico (vengono infatti bloccate dall'esametonio e dal curaro). I neuroni simpatici formano inoltre sinapsi eccitatorie di tipo nicotinico con i miotubi scheletrici, e sinapsi inibitorie di tipo muscarinico (bloccate dall'atropina) con i miociti cardiaci. La microscopia elettronica a livello di tutte queste sinapsi mostra le vescicole a contenuto chiaro tipiche delle terminazioni colinergiche, ove costituiscono il probabile luogo di deposito dell'ACh. Non è necessario il contatto diretto con le cellule non neuronali affinché si abbiano queste modificazioni colinergiche: esse infatti si producono anche quando manchino nella coltura cellule non neuronali ma si utilizzi un liquido di coltura precedentemente ‛condizionato' mediante incubazione separata con cellule non neuronali. Infatti, le sinapsi che si formano in tal caso tra i neuroni sono funzionali e di tipo colinergico. È così aperta la strada per l'isolamento e la caratterizzazione chimica del fattore ‛colinergico', il fattore chimico, cioè, che indirizza la scelta adrenergico-colinergica dei neuroni autonomi verso l'ACh.
Poiché ancora prima della nascita i neuroni dei gangli simpatici sintetizzano, sia pure a livello ridotto, noradrenalina, l'effetto del mezzo condizionato (MC) da cellule non neuronali appare quello di modificare in senso colinergico un ‛impegno' già preso in senso adrenergico.
Che si tratti effettivamente di un fenomeno di plasticità a livello del singolo neurone, piuttosto che di selezione a opera del MC di una popolazione di neuroni colinergici con soppressione di quella normale adrenergica, è mostrato da varie prove tra cui quelle basate su ‛microcolture' (v. Furshpan e altri, 1976; v. Potter e altri 1980). La microcoltura utilizzata è formata da un piccolissimo disco di collageno (circa 0,5 mm di diametro) al quale aderisce uno strato di miociti cardiaci che fanno da supporto a un singolo neurone. Se è vero che tale neurone è inizialmente (cioè nei primi giorni dopo l'espianto) adrenergico e poi si trasforma in colinergico a causa della presenza delle cellule non neuronali (miociti cardiaci, in questo caso), potrà esistere una fase di transizione in cui il neurone libera entrambi i trasmettitori, NA e ACh. In questo esperimento i miociti cardiaci, che pulsano spontaneamente e ritmicamente in coltura, servono anche come rivelatori del mediatore chimico liberato dal neurone, purché siano da esso innervati, in quanto possiedono sia recettori colinergici sia adrenergici. Il neurone e una cellula cardiaca adiacente vengono ciascuno penetrati con un microelettrodo; il neurone viene quindi stimolato e se esso libera ACh determina una riduzione di frequenza o l'arresto del battito del miocita (effetto bloccato dall'atropina), mentre se libera NA determina un aumento di frequenza (effetto bloccato dal propranololo). Oltre a neuroni con caratteristiche solo adrenergiche o solo colinergiche, sono stati trovati anche neuroni che liberano entrambi i mediatori, poiché la loro attivazione produce effetti misti su un dato miocita cardiaco, consistenti in inibizione seguita da eccitazione (v. fig. 23, D, E, F e G). La fig. 23 mostra inoltre che il neurone fa anche sinapsi con se stesso (autapsi) e che la sinapsi è colinergica eccitatoria (v. fig. 23A) e di tipo nicotinico in quanto viene bloccata dall'esametonio (v. fig. 23B).
Si può notare qui incidentalmente che la dimostrazione dell'esistenza di neuroni simpatici a doppio trasmettitore potrebbe apparire come una conferma dell'ipotesi di Burn e Rand (v., 1965): secondo tale ipotesi, i neuroni simpatici adrenergici adulti secernerebbero normalmente ACh oltre a NA e l'ACh agirebbe presinapticamente su recettori nicotinici della stessa terminazione che l'ha liberata, determinando il rilascio di NA. Secondo questa ipotesi, dunque, la liberazione di NA è sempre conseguente alla liberazione di ACh. Tuttavia i dati mostrati nella fig. 23 indicano che il neurone della microcoltura continua a secernere NA e così ad accelerare il miocita cardiaco (v. fig. 23E), anche in presenza di blocco nicotinico da esametonio di entità tale da abolire l'effetto eccitatorio autaptico (v. fig. 23B).
La prova definitiva che il medesimo neurone autonomo in coltura si trasforma da adrenergico in colinergico sotto l'azione del ‛fattore colinergico' delle cellule non neuronali è stata ottenuta in recenti esperimenti con microcolture (v. Potter e altri, 1980). Lo stesso neurone di una microcoltura è stato ripetutamente penetrato con un microelettrodo, lungo un arco di tempo di sei settimane. Si è potuta così osservare la transizione attraverso i seguenti stadi: 1) uno stadio iniziale adrenergico puro, caratterizzato da accelerazione dei miociti cardiaci a seguito della stimolazione del neurone (il propranololo blocca l'eccitazione dei miociti, senza smascherare un'azione inibitoria); 2) uno stadio intermedio, caratterizzato dalla liberazione di entrambi i trasmettitori (situazione analoga a quella del neurone illustrato in fig. 23); 3) uno stadio finale colinergico puro, nel quale la stimolazione del neurone produce inibizione del battito dei miociti cardiaci (l'atropina blocca l'inibizione senza smascherare un'azione eccitatoria).
È interessante notare che, almeno in questi esperimenti in vitro, l'NGF sembra avere un'azione permissiva invece che istruttiva riguardo alla produzione del trasmettitore: esso stimola l'accrescimento e la differenziazione di neuroni simpatici immaturi sia lungo la via adrenergica, sia lungo quella colinergica, ma non sembra avere effetto sulla scelta della via che viene imboccata.
Appare chiaro che le ricerche esposte sopra rappresentano appena l'inizio del cammino per la comprensione della differenziazione dei neuroni autonomi in senso adrenergico o colinergico. Molte domande si affacciano, alcune per ora senza risposta, altre alle quali si possono dare risposte plausibili perché basate su qualche dato sperimentale. Tra questi, uno assai interessante riguarda il ruolo svolto dall'attività di impulsi nervosi dei neuroni autonomi nei confronti della scelta del trasmettitore. Se i neuroni simpatici in coltura vengono stimolati elettricamente per vari giorni (oppure vengono mantenuti in stato di depolarizzazione aumentando la concentrazione di potassio nel mezzo), essi si sviluppano in senso adrenergico anche in presenza di mezzo condizionato da cellule non neuronali (che normalmente fa invece differenziare i neuroni in senso colinergico). Questa osservazione potrebbe spiegare perché nei gangli simpatici intatti la grande maggioranza dei neuroni rimane nella condizione prenatale adrenergica, e anzi si sviluppa vieppiù in questa direzione, pur essendo in stretto contatto con le cellule non neuronali dei gangli stessi. Tali cellule, come è noto dagli esperimenti di colture, dovrebbero invece trasformare i neuroni in senso colinergico. Questo avviene tuttavia solo per una ristretta minoranza dei neuroni dei gangli simpatici, quelli che innervano certi vasi sanguigni e le ghiandole sudoripare. La spiegazione potrebbe risiedere nell'attività di impulsi dei neuroni gangliari che inizia nella prima settimana di vita a causa dell'azione sinaptica eccitatoria esercitata dai neuroni pregangliari. In accordo con questa ipotesi, la minoranza dei neuroni gangliari che diviene colinergica acquisterebbe l'innervazione e la guida eccitatoria dai neuroni pregangliari più tardivamente, cioè dopo essere stata già influenzata dalle cellule non neuronali a scegliere l'ACh quale trasmettitore chimico.
2. Neuroni pregangliari. - Le fibre colinergiche pregangliari che innervano i gangli autonomi provengono da somi cellulari situati nella colonna intermediolaterale (CIL) e intermediomediale del midollo spinale. Queste cellule originano dal tubo neurale e non dalla cresta neurale, come è il caso dei neuroni postgangliari. La prima parte dello sviluppo dei simpatoblasti pregangliari e della crescita delle loro fibre nervose avviene anche in assenza della cresta neurale, e quindi in assenza dei neuroni bersaglio postsinaptici. Tuttavia il successivo sviluppo è regolato dai neuroni postgangliari, che determinano sia la sopravvivenza sia la differenziazione dei neuroni pregangliari (v. È c).
c) Sviluppo postnatale
La grande maggioranza delle connessioni sinaptiche dei neuroni tra di loro e con le loro cellule bersaglio periferiche avviene e matura nell'ultimo periodo fetale e nella primissima parte di vita postnatale. Orbene, importanti azioni vengono esercitate da ciascun neurone sugli altri neuroni o sulle cellule non neuronali con cui esso si mette in rapporto sinaptico, in particolare per quanto riguarda il loro sviluppo. La direzione dell'azione può essere sia dal neurone presinaptico a quello postsinaptico, nel qual caso si parla di regolazione ‛trans-sinaptica anterograda', sia da quello postsinaptico a quello presinaptico, nel qual caso si parla di regolazione ‛trans-sinaptica retrograda'. In generale, benché la regolazione trans-sinaptica sia presente anche nell'adulto, essa è assai più marcata durante lo sviluppo.
Lo sviluppo dei neuroni del sistema autonomo dipende anch'esso in modo determinante da queste azioni transsinaptiche, come può essere facilmente mostrato mediante lesioni, eseguite su animali sperimentali durante i primi giorni di vita, o delle vie discendenti midollari dirette ai corpi cellulari dei neuroni pregangliari situati nella CIL, o dei neuroni pregangliari stessi, oppure di quelli postgangliari, o infine delle cellule innervate alla periferia da questi ultimi.
Un approccio molto usato per studiare la regolazione trans-sinaptica anterograda consiste nella sezione, in topi o ratti neonati, del tronco del simpatico cervicale, che contiene gli assoni pregangliari colinergici diretti ai neuroni del ganglio cervicale superiore (GCS). Come conseguenza, i neuroni postgangliari presentano dimensioni più piccole, sviluppano un minor numero di terminazioni assoniche a livello degli organi bersaglio (ad es. nell'iride) e soprattutto hanno un contenuto assai ridotto di tirosinaidrossilasi (TH), dato che manca il normale aumento postnatale dell'enzima che può arrivare fino a circa dieci volte. Similmente la denervazione della midollare surrenale alla nascita impedisce il normale sviluppo di TH e DBH, portando conseguentemente a un ridotto contenuto in catecolammine. Quando si seziona il midollo spinale, interrompendo così le vie discendenti dirette ai neuroni pregangliari della colonna intermedio-laterale, questi rallentano la loro differenziazione, com'è testimoniato da un minore contenuto di ChAc (enzima essenziale in questi neuroni colinergici per la sintesi di ACh) e da un diminuito sviluppo dell'innervazione dei neuroni postgangliari. La sezione del midollo spinale porta inoltre ad alterazioni dei neuroni postgangliari, simili a quelle conseguenti a interruzione delle fibre pregangliari: in questo caso l'effetto si manifesta attraverso due sinapsi, prendendo il nome di azione trans-sinaptica anterograda secondaria.
Il meccanismo delle alterazioni trans-sinaptiche anterograde è ancora incerto. Si sa però che non è necessario per produrle che si abbia denervazione e degenerazione neuronale: infatti gli effetti inibitori sull'aumento postnatale di TH postgangliare si producono anche solamente bloccando la trasmissione sinaptica con clorisondammina (che compete con l'acetilcolina per i recettori postgangliari nicotinici; v. Black e Geen, 1974). Questo è dimostrato anche dal fatto che si possono avere alterazioni anterograde secondarie, come detto sopra. Si sa inoltre che, per quanto riguarda i neuroni adrenergici postgangliari, l'NGF (che agisce potentemente su questi neuroni: v. È d) non è coinvolto nella regolazione anterograda, poiché non è in grado di impedire o di far regredire le alterazioni gangliari da denervazione pregangliare. Non è improbabile che le alterazioni transsinaptiche anterograde siano dovute essenzialmente al venir meno dell'attività di impulsi nervosi, in analogia con quanto accade per le alterazioni del muscolo scheletrico dopo denervazione (v. Lømo e Westgaard, 1976), benché l'assenza di ancora ignote ‛sostanze trofiche' possa anche giocare un ruolo.
Come già esposto all'inizio, esiste anche una regolazione trans-sinaptica retrograda, attraverso la quale i neuroni postsinaptici controllano la maturazione di quelli presinaptici. Ad esempio, la distruzione selettiva dei neuroni postgangliari adrenergici nel topo neonato, mediante 6-idrossidopammina (6-OHDA) o guanetidina o siero anti-NGF, impedisce il normale sviluppo dei neuroni colinergici pregangliari nei quali l'attività ChAc rimane ai bassi livelli neonatali. Questo è in parte dovuto alla mancata sopravvivenza di una quota di neuroni pregangliari. All'opposto, uno sviluppo abnorme dei gangli simpatici ottenuto con NGF produce un aumento della ChAc pregangliare al di sopra della norma, aumento dovuto a una sopravvivenza maggiore del normale dei neuroni pregangliari. Infatti la morte di un certo numero di neuroni è parte del normale sviluppo di varie zone del sistema nervoso dei Vertebrati. La morte cellulare avviene già nel feto, quando i neuroni iniziano a stabilire le connessioni con le cellule bersaglio, e colpisce quei neuroni che non riescono appunto a stabilire sinapsi con il bersaglio stesso. Come è ovvio, la distruzione sperimentale delle cellule bersaglio potenzia il normale fenomeno della morte neuronale. Per quanto riguarda il sistema autonomo, non solo la sopravvivenza dei neuroni pregangliari dipende da quelli postgangliari, ma anche la sopravvivenza di questi ultimi dipende dalle cellule effettrici periferiche, muscolari o ghiandolari. Così, la rimozione delle ghiandole salivari o dell'iride, innervate da neuroni del GCS, determina una maggiore diminuzione nel numero dei neuroni del GCS stesso.
Il meccanismo della regolazione trans-sinaptica retrograda è, come quello anterogrado, ancora incerto. Tuttavia esso è di natura diversa da quello anterogrado. Per produrre le alterazioni retrograde non basta il blocco della trasmissione sinaptica (sufficiente invece per gli effetti anterogradi), ma è necessaria una grave lesione degli elementi postsinaptici. È probabile che fattori chimici vengano normalmente trasportati all'indietro dagli elementi postsinaptici a quelli presinaptici e che la loro soppressione sia la causa delle alterazioni retrograde. Per quanto riguarda il caso particolare dei rapporti tra effettori periferici e neuroni adrenergici gangliari, è probabile che tale fattore sia un fattore proteico già ben noto, l'NGF, come è descritto dettagliatamente nel successivo paragrafo.
d) Nerve Growth Factor (NGF)
L'esistenza di un fattore che stimola potentemente l'accrescimento dei gangli simpatici e sensitivi è stata scoperta casualmente in seguito all'osservazione che un sarcoma del topo trapiantato in embrioni di pollo stimola la crescita di neuroni sensitivi e simpatici. È stato poi mostrato che si tratta di un fattore proteico isolabile da tumori mesenchimali, dal veleno di serpenti e dalle ghiandole salivari di topo adulto. A questo fattore R. Levi-Montalcini ha dato il nome di Nerve Growth Factor (NGF; per una rassegna sull'argomento, v. Levi-Montalcini e Angeletti, 1968, e Thoenen e Barde, 1980). L'NGF salivare ha un peso molecolare 140.000; da esso si possono dissociare tre subunità, α, β e γ, delle quali solo l'unità β, con peso molecolare 30.000, possiede gli effetti della molecola intera.
L'NGF determina l'aumento di volume dei gangli simpatici e sensitivi e una profusa crescita di fibre nervose, sia in vivo (nell'embrione e nel neonato) che in vitro. I neuroni si ingrandiscono, vi è stimolazione della sintesi proteica, lipidica e di RNA e accelerazione della loro differenziazione con aumento dell'attività TH, DDC e DBH nei neuroni adrenergici. L'aumento di volume dei gangli degli animali neonati è anche dovuto a un aumento numerico dei neuroni, a sua volta attribuibile a una diminuita incidenza del normale fenomeno di morte cellulare. Gli effetti dell'NGF sui neuroni simpatici persistono nell'adulto, mentre quelli sui neuroni sensitivi sono presenti solo nell'embrione. L'NGF agisce anche sulla midollare surrenale e sui neuroni amminergici centrali, ma non su altri neuroni.
La miglior prova che l'NGF svolge un'importante azione fisiologica durante lo sviluppo è costituita dal fatto che in animali neonati l'iniezione di anticorpi preparati contro l'NGF (siero anti-NGF) produce la distruzione selettiva e quasi completa dei gangli simpatici. Questo effetto viene chiamato ‛immunosimpatectomia'.
La somministrazione di siero anti-NGF nell'animale adulto produce effetti assai meno marcati, poiché non si ha morte dei neuroni adrenergici ma solo riduzione delle loro dimensioni, la deplezione in catecolammine e alcuni effetti simili a quelli che si osservano dopo assotomia.
L'NGF è presente nel siero del sangue di tutti i Mammiferi ed è secreto da una grande varietà di tessuti. È probabile che l'NGF venga normalmente captato a livello dei tessuti periferici dalle terminazioni dei neuroni postgangliari adrenergici e trasportato in via retrograda ai loro corpi cellulari esercitandovi la sua azione di stimolo all'accrescimento e alla differenziazione, nel neonato, e di mantenimento nell'adulto. I fatti in favore di questa possibilità sono i seguenti.
1) NGF esogeno marcato viene captato selettivamente dalle terminazioni adrenergiche e trasportato in via retrograda ai somi cellulari. Questo trasporto viene bloccato dalla colchicina, sostanza che blocca il trasporto assonico anterogrado e retrogrado.
2) La rimozione delle cellule bersaglio periferiche incrementa il fenomeno di morte cellulare dei neuroni adrenergici (come già detto sopra), ma questo può essere impedito mettendo, al posto dei bersagli rimossi, della cellulosa contenente NGF.
3) Il trattamento di ratti neonati con 6-OHDA produce una simpatectomia chimica, essendo seguito, come il trattamento con siero anti-NGF, da distruzione dei neuroni dei gangli simpatici. La 6-OHDA viene captata selettivamente dalle terminazioni adrenergiche ove svolge la sua azione lesiva: le conseguenze dannose sui somi cellulari vengono impedite dal trattamento con NGF. Gli effetti della 6-OHDA nel neonato appaiono simili a quelli dell'assotomia, che ugualmente porta nel neonato alla morte del neurone. Nell'adulto, invece, sia l'assotomia postgangliare sia il trattamento con 6-OHDA producono alterazioni meno gravi e transitorie nei corpi cellulari dei neuroni adrenergici, realizzando il quadro della degenerazione retrograda: anche questi effetti vengono contrastati dal trattamento con NGF.
(Il paragrafo c del capitolo 2, i paragrafi b e c del capitolo 5, il paragrafo b del capitolo 9 e l'intero capitolo 11 sono stati scritti dal prof. Alberto Cangiano, al quale si deve anche l'aggiornamento delle parti scritte dal prof. Ulf S. von Euler).
bibliografia
Acheson, G. H. (a cura di), Second symposium on cathecolamines, Milan, July 4-9, 1965, in ‟Pharmacological reviews", 1966, XVIII, pp. 1-803.
Aloe, L., Levi-Montalcini, R., Nerve growth factor-induced transformation of immature chromaffin cells in vivo into sympathetic neurons: effect of antiserum to nerve growth factor, in ‟Proceedings of the National Academy of Sciences", 1979, LXXVI, pp. 1246-1250.
Axelrod, J., The metabolism, storage and release of cathecolamines, in Recent progress in hormone research (a cura di G. Pincus), vol. XXI, New York 1965, pp. 597-619.
Bell, C., Fine structural localizationh of acetylcholinesterase at a cholinergic vasodilator nerve-arterial smooth muscle synapse, in ‟Circulation research", 1969, XXIV, pp. 61-70.
Black, I. B., Geen, S. C., Inhibition of the biochemical and morphological maturation of adrenergic neurons by nicotinic receptor blockade, in ‟Journal of neurochemistry", 1974, XXII, pp. 301-306.
Blaschko, H., The activity of L(−)-dopa decarboxylase, in ‟Journal of physiology", 1942, CI, pp. 337-349.
Blaschko, H., Muscholl, E. (a cura di), Catecholamines, Berlin-Heidelberg-New York 1972.
Brandt, B. ., Hagiwara, S., Kidokoro, Y., Miyazaki, S., Action potentials in the rat chromaffin cell and effects of acetylcholine, in ‟Journal of physiology", 1976, CCLXIII, pp. 417-439.
Brodie, B. B., Shore, P. A., Pletscher, A., Serotonin-releasing activity limited to rauwolfia alkaloids with tranquillizing action, in ‟Science", 1956, CXXIII, pp. 992-993.
Brooks, C. McC., Koizumi, K., Sato, A., Integrative functions of the autonomic nervous system, Amsterdam 1979.
Bülbring, E., Brading, A. F., Jones, A. W., Tomita, T., Smooth muscle: an assesment of current knowledge, London 1981.
Burn, J. H., Rand, M. J., Acetylcholine in adrenergic transmission, in ‟Annual review of pharmacology", 1965, V, pp. 163-182.
Burnstock, G., Purinergic nerves, in ‟Pharmacological reviews", 1972, XXIV, pp. 509-581.
Burnstock, G., Costa, M., Adrenergic neurons: their organisation, function and development in the peripheral nervous system, London 1975.
Cannon, W. B., Bodily changes in pain, hunger, fear and rage, New York 1915.
Carlsson, A., The occurrence, distribution and physiological role of catecholamines in the nervous system, in ‟Pharmacological reviews", 1959, XI, pp. 490-493.
Carlsson, A., Hillar, N.-A., Release of adrenaline from the adrenal medulla of rabbits produced by reserpine, in ‟Kungliga fysiografiska sällskapets i Lund förhandlingar", 1956, XXVI, 8.
Cooper, J. R., Bloom, F. E., Roth, R. H., The biochemical basis of neuropharmacology, London 1970.
Dahlstrom, A., Fuxe, K., Evidence for the existence of monoamine containing neurons in the central nervous system, in ‟Acta physiologica scandinavica", 1964, LXII, suppl. 232.
Dale, H. H., The occurrence in ergot and action of acetylcholine, in ‟Journal of physiology", 1914, XLVIII, pp. iii-iv.
Dale, H. H., Chemical transmission of the effects of nerve impulses, in ‟British medical journal", 1934, pp. 1-20.
Ehrenpreis, D., Fleisch, J. H., Mittag, T. W., Approaches to the molecular nature of pharmacological receptors, in ‟Pharmacological reviews", 1969, xXI, pp. 131-181.
Eränkö, O., Cell types of the adrenal medulla, in Ciba Foundation symposium on adrenergic mechanisms (a cura di J. R. Vane, G. E. Wolstenholme e M. O'Connor), Boston 1960, pp. 103-108.
Euler, U. S. von, A specific sympathomimetic ergone in adrenergic nerve fibres (Sympathin) and its relations to adrenaline and noradrenaline, in ‟Acta physiologica scandinavica", 1946, XII, pp. 73-97.
Euler, U. S. von, Noradrenaline, Springfield, Ill., 1956.
Euler, U. S. von, Adrenergic neurohormones, in Comparative endocrinology (a cura di U. S. von Euler e H. Heller), vol. II, New York 1963, pp. 209-238.
Falck, B., Observations on the possibilities of the cellular localization of monoamines by a fluorescence method, in ‟Acta physiologica scandinavica", 1962, LVI, supp. 197.
Folkow, B., Impulse frequency in sympathetic vasomotor fibres correlated to the release and elimination of the transmitter, in ‟Acta physiologica scandinavica", 1952, XXV, pp. 49-76.
Furchgott, R. F., The receptors for epinephrine and norepinephrine (adrenergic receptors), in ‟Pharmacological reviews", 1959, XI, pp. 429-441.
Furshpan, E. J., MacLeish, P. R., O'Lague, P. H., Potter, D. D., Chemical transmission between rat sympathetic neurons and cardiac myocites developing in microcultures: evidence for cholinergic, adrenergic and dual-function neurons, in ‟Proceedings of the National Academy of Sciences", 1976, LXXIII, pp. 4225-4229.
Geffen, L.B., Jarrott, B., Cellular aspects of cathecholaminergic neurons, in Handbook of physiology, section 1, The nervous system, vol. I, part I (a cura di J.M. Brookhart e V. B. Mountcastle), Bethesda 1977.
Greengard, P., Possible role for cyclic nucleotides and phosphorilated membrane proteins in post-synaptic actions of neurotransmitters, in ‟Nature", 1976, CCLX, pp. 101-108.
Hillarp, N.-A., Structure of the synapse and the peripheral innervation apparatus of the autonomic nervous system, in ‟Acta anatomica", 1946, II, suppl. 4.
Höckfelt, T., Fuxe, K., Goldstein, M., Johansson, O., Immunohistochemical evidence for the existence of adrenaline neurons in the rat brain, in ‟Brain research", 1974, LXVI, pp. 235-251.
Hökfelt, T., Johansson, O., Ljungdahl, A., Lundberg, J.-M., Schultzberg, M., Ppetidergic neurones, in ‟Nature", 1980, CCLXXXIV, pp. 515-521.
Hökfelt, T., Johansson, O., Ljungdahl, A., Lundberg, J.-M., Schultzberg, M., steinbush, H., Verhofstad, A., Goldstein, M., Histochemical characterization of neuron populations: immunocytochemical studies on transmitter related substances, in Nerve cells, transmitters and behaviour (a cura di R. Levi-Montalcini), Roma 1980, pp. 293-314.
Holtz, P., Credner, K., Kronenberg, G., Über das sympathicomimeitsche pressorische Prinzip des Harns (Urosympathin'), in ‟Naunyn-Schmiedebergs Archiv für Pharmakologie und experimentelle Pathologie", 1947, CCIV, pp. 228-243.
Iversen, L. L., The uptake and storage of noradrenaline in sympathetic nerves, London 1967.
Jan, Y. N., Jan, L. Y., Kuffler, S. W., Further evidence for peptidergic transmission in sympathetic ganglia, in ‟Proceedings of the National Academy of Sciences", 1980, LXXVII, pp. 5008-5012.
Kopin, I. J., Storage and metabolism of catecholamines: the role of monoamine oxidase, in ‟Pharmacological reviews", 1964, XVI, pp. 179-191.
LeDouarin, N. M., Teillet, M. A., Experimental analysis of the migration and differentiation of neuroblasts of the autonomic nervous system and of neuroectodermal mesenchymal derivatives, using a biological cell marking technique, in ‟Developmental biology", 1974, XLI, pp. 162-184.
Levi-Montalcini, R., Aloe, L., Menesini Chen, M. G., Chen, J. S., New features of the Nerve Growth Factor-target cells interaction, in Nerve cells, transmitters and behaviour (a cura di R. Levi-Montalcini), Roma 1980, pp. 11-40.
Levi-Montalcini, R., Angeletti, P. U., Nerve Growth Factor, in ‟Physiological reviews", 1968, XLVIII, pp. 534-569.
Loewi, O., Über humorale Übertragbarkeit der Herznervenwirkung, in ‟Pflügers Archiv", 1921, CLXXXIX, pp. 239-242.
Lomo, T., Westgaard, R. H., Control of ACh sensitivity in rat muscle fibers, in ‟Cold Spring Harbor Symposia on quantitative biology", 1976, XL, pp. 263-274.
Mains, R.E., Patterson, P. H., Primary cultures of dissociated sympathetic neurons. I. Establishment of long-term growth in culture and studies of differentiated properties, in ‟Journal of cell biology", 1973, LIX, pp. 329-345.
Moore, K. L., The developing human, Philadelphia 1973 (tr. it.: Lo sviluppo dell'uomo, Bologna 1980).
Nachmansohn, D., Machado, A. L., The formation of acetylcholine. A new enzyme: choline acetylase', in ‟Journal of neurophysiology", 1943, VI, pp. 397-401.
O'Lague, P. H., Obata, K., Claude, P., Furshpan, E. J., Potter, D. D., Evidence for cholinergic synapses between dissociated rat symnpathetic neurons in cell culture, in ‟Proceedings of the National Academy of Sciences", 1974, LXXI, pp. 3602-3606.
Oliver, G., Schäfer, E. A., The physiological effects of extracts of the suprarenal capsules, in ‟Journal of physiology", 1895, XVIII, pp. 230-276.
Potter, D. D., Landis, S. C., Furshpan, E. J., Adrenergic-cholinergic dual function in cultured sympathetic neurones of the rat, in Ciba Foundation symposium on the development of the autonomic nervous system, London 1980, pp. 123-138.
Robertis, E. de, Molecular biology of synaptic receptors, in ‟Science", 1971, CLXXI, pp. 963-971.
Skök, V. I., Physiology of autonomic ganglia, Tokyo 1973.
Sutherland, E. W., Rall, T. W., The relation of adenosine-3′,5′-phosphate and phosphorylase to the actions of catecholamines and other hormones, in ‟Pharmacological reviews", 1960, XII, pp. 265-299.
Takamine, J., Adrenaline, the active principle of the suprarenal glands and its mode of preparation, in ‟American journal of pharmacology", 1901, LXXIII, pp. 523 ss.
Thoenen, H., Barde, Y. A., Physiology of nerve growth factor, in ‟Physiological review", 1980, LX, pp. 1284-1335.
Triggle, D. J., Chemical aspects of the autonomic nervous system, New York 1965.
Vane, J. R., Wolstenholme, G. E., O'Connor, M. (a cura di), Ciba Foundation symposium on adrenergic mechanisms, Boston 1960.