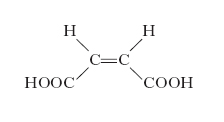
maleico, acido
Acido bicarbossilico insaturo, avente
Si tratta dell’acido cis- 1,2-etilendicarbossilico. In presenza di luce o di tracce di bromo, iodio o acido nitroso si trasforma nel più stabile isomero trans (acido fumarico). L’isomerizzazione è più rapida e completa per blando riscaldamento in presenza di acido cloridrico. Al contrario dell’acido fumarico, l’acido m. non si rinviene in natura. È l’acido bicarbossilico più forte. Si presenta in prismi incolori, di sapore acido sgradevole, solubili in alcol, etere ed acqua, che fondono a 130 °C; ha importanza come tale e sotto forma di derivati, in varie sintesi organiche, nell’industria tessile come colorante per il cotone, la lana e la seta, nella fabbricazione di resine sintetiche, nell’industria degli oli siccativi come ritardante dell’irrancidimento.
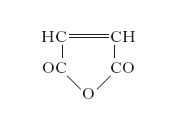
Analoghi, ma più larghi impieghi dell’acido ha l’anidride maleica, che ha
Si ottiene dall’acido corrispondente per perdita di acqua. Industrialmente si ottiene ossidando il benzene in fase vapore (con anidride vanadica come catalizzatore) secondo la reazione
2C6H6 + 9O2 ⇄ 2C4H2O3 + 4H2O + 4CO2,
raffreddando i vapori e purificando il prodotto grezzo ottenuto o per distillazione o per sublimazione. Si può ottenere anidride maleica in minor quantità anche ossidando naftalina, butene, butadiene, toluene ecc., con catalizzatori a base di ossidi di molibdeno, vanadio, fosforo. Forma cristalli aghiformi, incolori, solubili in diossano, in alcol.