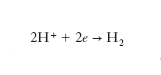elettrocatalisi
Enciclopedia on line
Variazione della velocità di una reazione elettrochimica in seguito al cambiamento del substrato di cui è costituito l’elettrodo, a parità di sovrapotenziale. L’esempio più chiaro di e. è offerto dalla reazione dell’evoluzione dell’idrogeno:
dove e indica un elettrone, la cui velocità dipende in modo significativo dalla natura del metallo di cui è costituito l’elettrodo. Altri esempi interessanti riguardano l’ossidazione degli idrocarburi insaturi su elettrodi di metalli nobili e la riduzione catodica dell’ossigeno nelle celle a combustibile.