retinolo
In biochimica, la vitamina A1, precursore inattivo del retinale, che è la forma biologicamente attiva della vitamina A. Ha formula C20H30O e possiede una catena idrocarburica insatura, con 4 doppi legami, legata a un anello β-iononico che presenta un gruppo alcolico terminale sull’atomo di carbonio C20. Si origina dalla degradazione enzimatica del β-carotene, che avviene nell’intestino tenue, dando origine a due molecole di r., che si ritrovano comunemente nella loro forma isomerica trans-. Successivamente, il r. viene enzimaticamente ossidato e isomerizzato a retinale a livello epatico. Anche se il r. come tale non possiede attività biologica, può essere però immagazzinato per diversi mesi nel fegato dopo esterificazione con acidi grassi a lunga catena carboniosa (come l’acido palmitico).
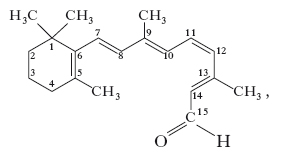
Il retinale deriva dal r. per ossidazione del gruppo alcolico terminale in gruppo aldeidico e successiva isomerizzazione del doppio legame fra il C11 e il C12, operate a livello epatico da enzimi specifici (rispettivamente, retinolodeidrogenasi e retinoloisomerasi). Ha formula C20H28O; nella sua conformazione di 11-cis retinale, la cui formula di struttura è
,
si lega alla proteina opsina, presente nei bastoncelli della retina, formando la rodopsina, direttamente coinvolta nei meccanismi biochimici della visione. Il trasporto del retinale dal fegato alla retina avviene mediante il legame con la proteina RBP. Prodotto di ossidazione del retinale è l’acido retinoico, che appartiene al gruppo delle sostanze dotate di attività vitaminica A, anche se molto limitata.