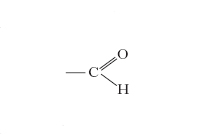
aldeidi
Composti chimici, detti anche alcoli deidrogenati, caratterizzati dalla presenza del gruppo funzionale
unito a un radicale alchilico o arilico. Il nome delle singole a. deriva in genere da quello dell’acido di ugual numero di atomi di carbonio (per es., a. acetica dall’acido acetico); la nomenclatura IUPAC prescrive di assegnare la desinenza -ale al nome dell’idrocarburo da cui l’a. si può far derivare.
Nella serie alifatica i termini inferiori sono liquidi (salvo il primo che è gassoso), tanto più solubili in acqua quanto più basso è il loro numero di atomi di carbonio. Le a. della serie aromatica sono liquidi poco solubili dotati di odore penetrante. Fra i numerosi metodi generali di preparazione figurano l’ossidazione moderata degli alcoli primari, la riduzione dei cloruri degli acidi e la reazione di ossosintesi nella quale un alchene viene riscaldato sotto pressione con ossido di carbonio e idrogeno, in presenza di un sale di cobalto quale catalizzatore. Le a. aromatiche si possono preparare per ossidazione di un gruppo metilico legato a un anello aromatico per ossidazione con anidride cromica in presenza di anidride acetica. Molte a. hanno un odore gradevole (di frutta o di fiori), hanno reazione neutra o debolmente acida. A causa della presenza del doppio legame nel gruppo funzionale, le a. hanno una grande reattività: danno facilmente reazioni di addizione (con acqua, idrogeno, bisolfiti, acido cianidrico), di polimerizzazione, di condensazione ecc., ampiamente utilizzate nelle sintesi industriali. Tra le più importanti, la formaldeide, l'acetaldeide, la benzaldeide.
Biochimica
Le a. hanno una notevolissima importanza biochimica in quanto la maggior parte dell’energia utilizzata nei sistemi biologici ha origine dall’ossidazione enzimatica della funzione aldeidica dei monosaccaridi a gruppo carbossilico. Negli organismi superiori i meccanismi biochimici mediante i quali si ha produzione di energia in seguito a dissimilazione dei monosaccaridi sono due:
a) ossidazione diretta del gruppo aldeidico a gruppo carbossilico, previa fosforilazione del gruppo alcolico all’altra estremità della molecola, con formazione di glicosio-6-fosfato (ciclo dei pentosi);
b) trasformazione dei monosaccaridi in esosi-difosfati e scissione della catena carboniosa con formazione di due triosi-fosfati isomeri, il fosfodiossiacetone e l’aldeide-3-fosfoglicerica, da cui si origina l’acido piruvico (glicolisi). L’energia sviluppata in tali processi ossidativi viene accumulata sotto forma di legami fosforici ricchi di energia e usata per le reazioni di sintesi del metabolismo cellulare.