Cardiopatie
Cardiopatie
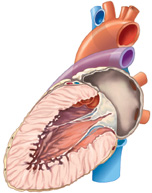
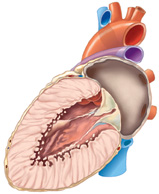
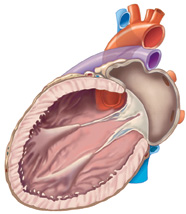
Lo scompenso cardiaco (fig. 1, 2, 3) è una sindrome clinica caratterizzata da un'anomala funzione contrattile del muscolo cardiaco, che risulta incapace di pompare una quantità di sangue adeguata alle richieste metaboliche dell'organismo. Esso costituisce una sindrome di frequente riscontro e un problema sanitario mondiale di dimensioni sempre crescenti, soprattutto nel mondo occidentale, divenendo la principale malattia in ambito cardiovascolare. L'aumento dell'età media, la riduzione della mortalità per eventi cardiaci acuti, come l'infarto del miocardio, i progressi nel trattamento delle patologie cardiovascolari croniche, come la cardiopatia ischemica, l'ipertensione arteriosa o il diabete mellito, sembrano, infatti, posporre l'insorgenza della malattia piuttosto che prevenirla.
Viene stimato, attualmente, che circa 5 milioni di Americani siano affetti da scompenso cardiaco e che ogni anno vengano diagnosticati oltre mezzo milione di nuovi casi, con una richiesta annuale di quasi 900.000 ospedalizzazioni. In Europa, la prevalenza nella popolazione generale varia dallo 0,4 al 2% e in Italia almeno mezzo milione di persone ne è colpito. L'incidenza della malattia, ossia il numero di nuovi casi annui, cresce notevolmente con l'aumentare dell'età, costituendo la causa più frequente di ospedalizzazione nella popolazione maggiore di sessantacinque anni. La prognosi della malattia è uniformemente infausta, se non si riesce a intervenire sulla causa sottostante. La mortalità media tra i pazienti affetti da tale sindrome è di circa il 50% a cinque anni, arrivando, nei casi più gravi di scompenso, addirittura a una mortalità del 50% a un anno. In circa il 40% dei casi il decesso avviene improvvisamente, probabilmente per la comparsa di un'aritmia fatale. Anche sotto il profilo economico lo scompenso cardiaco costituisce un problema sanitario di estrema rilevanza poiché, in termini di risorse, rappresenta in Europa e negli Stati Uniti d'America l'1÷2% della spesa sanitaria totale.
Numerose ed eterogenee condizioni cliniche possono essere alla base dell'insufficienza cardiaca. L'eziologia deve essere, pertanto, ricercata accuratamente, in quanto la conoscenza delle cause spesso permette di rallentarne il decorso e migliorare la prognosi attraverso la scelta di una terapia mirata. La cardiopatia ischemica, secondo le casistiche più recenti, risulta essere, oggi, la causa maggiormente responsabile dell'insufficienza cardiaca. In passato, invece, l'ipertensione arteriosa era l'eziologia più frequente di scompenso, ma negli ultimi venti anni la maggiore disponibilità terapeutica ne ha notevolmente ridotto l'incidenza quale fattore causale. Seppure in una percentuale inferiore di casi, lo scompenso cardiaco può essere secondario a malattie delle valvole cardiache, ad alterazioni del pericardio o a patologie del muscolo cardiaco (cardiomiopatie primitive).
La malattia reumatica è, nel mondo occidentale, sempre meno responsabile di insufficienza cardiaca, mentre le cardiopatie congenite rappresentano una minima percentuale tra le cause di scompenso. Diverse condizioni patologiche non cardiache possono provocare, attraverso un interessamento diretto o indiretto del muscolo cardiaco, una disfunzione miocardica. Ricordiamo, tra queste, le alterazioni endocrino-metaboliche (patologie della tiroide, feocromocitoma, ecc.), alcuni farmaci o sostanze tossiche (intossicazione da metalli pesanti, farmaci antitumorali), le patologie infettive, infiammatorie (lupus eritematoso sistemico, artrite reumatoide, ecc.) e altre condizioni sistemiche, come le patologie polmonari croniche, che possono coinvolgere, con estensione variabile, il sistema cardiovascolare. Vi sono, inoltre, fattori che, attraverso differenti meccanismi, quali l'aumento delle richieste metaboliche dell'organismo, possono esacerbare i sintomi dello scompenso cardiaco o far aggravare la situazione clinica, come l'insorgenza di un evento aritmico, l'anemia, la gravidanza, una crisi ipertensiva o un evento infettivo.
Lo scompenso cardiaco
Lo scompenso cardiaco viene attualmente distinto, in base alla fisiopatologia, in 'sistolico' e 'diastolico'. Nel primo caso, si ha una riduzione della quantità di sangue che viene espulsa dal ventricolo durante ogni sistole (gittata sistolica), con un conseguente aumento della quantità di sangue residuo all'interno del ventricolo (volume telediastolico), cui segue una congestione del distretto venoso a monte. L'aumento del volume telediastolico causa un aumento pressorio all'interno della cavità ventricolare cui segue la successiva dilatazione del ventricolo sinistro, tipica delle fasi più avanzate di scompenso sistolico. Nelle forme di scompenso diastolico, invece, non si osserva una riduzione della funzione contrattile, ma una disfunzione della fase di rilasciamento, dovuta a una diminuzione della velocità o dell'entità del riempimento ventricolare con una successiva congestione del circolo venoso polmonare o del circolo venoso sistemico.
La classificazione in 'scompenso destro' e 'sinistro', in funzione delle sezioni cardiache maggiormente coinvolte, fa riferimento alla presenza di un predominante interessamento del ventricolo sinistro o destro, con rispettiva congestione venosa delle vene polmonari o delle vene sistemiche. La distinzione in 'cronico' e 'acuto', invece, è legata alla presentazione clinica della sintomatologia. La forma cronica è di gran lunga la più frequente ed è caratterizzata dalla presenza costante dei segni e dei sintomi propri dello scompenso cardiaco: la dispnea (disturbo della respirazione, caratterizzato da una penosa sensazione di mancanza d'aria, la cosidetta 'fame d'aria', e da un'alterazione del ritmo respiratorio, che si fa breve, superficiale, affannoso), che può insorgere in condizioni di sforzo o a riposo, gli edemi declivi e l'evidenza obiettiva di una riduzione della funzione cardiaca. La forma acuta, invece, può essere la fase di esacerbazione di una disfunzione cronica o rappresentare l'improvvisa manifestazione di un danno cardiaco importante, come quello conseguente a un infarto miocardico esteso.
Diversi sono i sintomi e i segni che caratterizzano il paziente affetto da scompenso cardiaco: molti sono riconducibili alla congestione del sistema venoso, alla riduzione del flusso ematico in periferia e ai meccanismi neuro-ormonali che vengono attivati come iniziale tentativo di compenso del sistema circolatorio, ma che poi sono anche i principali responsabili del peggioramento clinico (sistema nervoso adrenergico, sistema renina-angiotensina-aldosterone). La dispnea costituisce un sintomo cardine dello scompenso cardiaco. È dovuta alla congestione polmonare che conduce alla formazione di un edema interstiziale con conseguente riduzione della distensibilità polmonare. Non è un sintomo specifico dell'insufficienza cardiaca poiché si può riscontrare in molte altre condizioni morbose cardiache (vizi valvolari mitralici o aortici) e non cardiache (malattie respiratorie croniche). La difficoltà respiratoria, associata o meno alla presenza di tosse, può presentarsi sia in condizioni di sforzo fisico (dispnea da sforzo) sia in condizioni di riposo, obbligando il paziente a mantenere il torace in posizione eretta per evitarne l'insorgenza (ortopnea), o svegliandolo bruscamente una volta addormentato (dispnea parossistica notturna). La classificazione della New York Heart Association stabilisce la classe funzionale dei pazienti: valuta le attività fisiche che il soggetto è in grado di svolgere senza la comparsa di dispnea, includendo i pazienti in quattro classi di gravità crescente dalla I alla IV. Altri sintomi sono l'astenia (senso di affaticamento e debolezza), i disturbi gastrointestinali (anoressia, gonfiore, stipsi e dolenzia addominale), l'oliguria (riduzione della diuresi) e i sintomi cerebrali (ansietà, confusione, insonnia), tutti legati alla ridotta irrorazione periferica.
Dal punto di vista clinico, si osservano alterazioni della cute, quali l'ipotermia o la cianosi delle estremità, dovute all'attivazione del sistema nervoso adrenergico e alla ridotta irrorazione tissutale. L'esame cardiovascolare permette di rilevare reperti legati a eventuali patologie sottostanti che possono essere la causa dell'insufficienza stessa. La frequenza cardiaca è solitamente aumentata; all'auscultazione cardiaca può essere evidenziato un ritmo particolare (ritmo di galoppo) caratterizzato dalla comparsa di toni aggiunti o dal riscontro di altri reperti quali i soffi, segni di un'alterata funzionalità degli apparati valvolari. L'esame del torace può essere del tutto normale nelle forme lievi ma, quando la pressione nel sistema polmonare aumenta eccessivamente, provocando la trasudazione di liquidi nello spazio interstiziale, si auscultano rumori umidi in corrispondenza delle zone basali, fino ad averne, come nel caso dell'edema polmonare franco, l'estensione a tutti i campi polmonari con un'importante compromissione della funzione respiratoria. Nello scompenso cronico si può osservare anche la presenza di liquido che si accumula nello spazio pleurico (idrotorace). L'esame clinico dell'addome può documentare un aumento delle dimensioni del fegato (epatomegalia) o un versamento nella cavità peritoneale (ascite), successivo a un aumento, sostenuto e protratto nel tempo, della pressione all'interno delle vene epatiche. L'edema periferico è un'altra caratteristica clinica presente nei pazienti con scompenso cardiaco. Generalmente riscontrabile a livello pretibiale e malleolare, bilateralmente, nei pazienti che mantengono la stazione eretta, si localizza a livello presacrale in quelli costretti a letto. L'edema agli arti superiori o l'edema generalizzato (anasarca) è attualmente raro e riscontrabile solo nelle forme avanzate o non trattate. Nonostante sia fondamentale un accurato esame clinico, non si può prescindere da una valutazione strumentale per aumentare la sensibilità della diagnosi stessa e per meglio valutare l'entità della compromissione funzionale e quindi la gravità clinica.
La diagnosi
La valutazione dei pazienti con scompenso cardiaco ha l'obiettivo di accertare il tipo di disfunzione e il grado di compromissione cardiaca, evidenziare eventuali fattori causali reversibili, determinare la prognosi e guidare la terapia. Gli esami di laboratorio possono suggerire la diagnosi di scompenso ed escludere potenziali cause sistemiche o patologie concomitanti quali l'insufficienza renale, la tireotossicosi o il feocromocitoma. Inoltre, negli ultimi anni, sempre più rilievo è stato assunto dalla valutazione delle alterazioni neuro-ormonali che si osservano in corso di insufficienza cardiaca. I livelli sierici di noradrenalina, renina, angiotensina II, aldosterone e ancor di più dei peptidi natriuretici, atriale e ventricolare (ANP e BNP), sono stati correlati, in molti studi, con la progressione e con la prognosi della malattia. In particolare, ANP e BNP aumentano in circolo in corso di disfunzione miocardica, mediante meccanismi non del tutto definiti, ancor prima che si abbia una franca manifestazione clinica e hanno dimostrato di essere i più importanti indicatori umorali per la diagnosi e la valutazione della risposta alla terapia farmacologica.
L'elettrocardiogramma a dodici derivazioni raramente risulta normale nei pazienti con ridotta frazione d'eiezione e permette di evidenziare importanti alterazioni che possono indirizzare verso un'eziologia precisa come quella ischemica o ipertensiva. Inoltre documenta eventuali turbe del ritmo elettrico, quali le bradiaritmie o le tachiaritmie come il flutter o la fibrillazione atriale, che possono essere alla base di una destabilizzazione clinica dello scompenso. Anche l'esame elettrocardiografico sotto sforzo può essere d'ausilio per chiarire l'eventuale eziologia ischemica e valutare la tolleranza del paziente allo sforzo fisico. La radiografia del torace in duplice proiezione può mostrare un ingrandimento delle dimensioni cardiache, i segni legati a un'alterazione del flusso ematico polmonare, come la distensione dei vasi polmonari, o, in alcuni casi, determinare la presenza di versamento pleurico. Fondamentale per la valutazione dello scompenso, è l'esame ecocardiografico completo (mono- e bidimensionale e color-doppler), poiché guida la diagnosi eziologica e fornisce indicazioni sui meccanismi fisiopatologici, sulla gravità della disfunzione ventricolare e sulla prognosi, permettendo di valutare l'evoluzione temporale e la risposta alla terapia. Lo studio ecocardiografico offre informazioni sulle dimensioni, sulla geometria e sulla funzione sistolica e diastolica del ventricolo sinistro. Consente lo studio della morfologia e della funzionalità dell'apparato valvolare, grazie anche all'impiego della metodica doppler, che analizza la velocità dei flussi transvalvolari e rivela la presenza di stenosi o insufficienze.
Il cateterismo cardiaco non è generalmente necessario per la diagnosi ma può fornire informazioni utili sull'eziologia dello scompenso, poiché permette di misurare parametri quali la gittata cardiaca e le pressioni di riempimento. Inoltre, mediante l'angiografia coronarica, è possibile individuare cause ischemiche di dilatazione ventricolare che potrebbero beneficiare di un intervento di rivascolarizzazione, percutaneo, mediante angioplastica coronarica, o chirurgico, mediante by-pass aorto-coronarico. La biopsia endomiocardica si effettua quando la patologia del muscolo cardiaco non riconosce una causa valvolare, coronarica o legata all'ipertensione arteriosa e si associa a un forte sospetto di forme su base infiammatoria, come nelle miocarditi virali, infiltrativa, come la sarcoidosi o l'amiloidosi, o degenerativa, come la displasia aritmogena del ventricolo destro.
Le terapie
Il trattamento dello scompenso cardiaco impegna gran parte della ricerca scientifica in ambito cardiologico. Ciononostante individuare e rimuovere la causa, effettuando pertanto una terapia eziologica, è possibile solo in una percentuale esigua di casi. Nelle altre situazioni, l'obiettivo terapeutico è quello di ridurre i sintomi, aumentare l'autonomia funzionale del paziente, rallentare la progressione della malattia e prevenire le complicanze, ottenendo un aumento della sopravvivenza e un miglioramento della qualità della vita. Negli ultimi anni, le possibilità terapeutiche, nei pazienti con scompenso cardiaco, sono notevolmente aumentate e sempre più numerosi sono i campi verso cui la ricerca sta indirizzandosi. La terapia farmacologica, infatti, in molti casi non è sufficiente a controllare la malattia e spesso è necessario ricorrere all'associazione di più farmaci. Elementi cardine della terapia dello scompenso sono: i farmaci ad azione diuretica, quelli che migliorano la contrattilità ventricolare (azione inotropa positiva), quelli ad azione vasodilatatrice e i farmaci antagonisti dei sistemi neuro-ormonali. La terapia diuretica costituisce la più collaudata strategia per ridurre la ritenzione idrica e diminuire il lavoro cardiaco. Diversi trials clinici hanno dimostrato che l'uso dei diuretici riduce il rischio di morte e di progressione della malattia. L'utilizzo ottimale dei diuretici non può prescindere, tuttavia, da una riduzione dell'apporto idrosalino con la dieta e dal monitoraggio quotidiano del peso corporeo. Gli ACE-inibitori e gli antagonisti recettoriali dell'angiotensina II, molecole antagoniste del sistema renina-angiotensina, si sono rivelati, in numerosi studi clinici, farmaci cardine nella terapia dello scompenso. Agendo come vasodilatatori, riducono il lavoro cardiaco ma hanno anche un importante effetto nel contrastare la progressiva dilatazione e il deterioramento funzionale del ventricolo, migliorando, così, significativamente la sopravvivenza. Un effetto complementare, volto ad antagonizzare il sistema neuro-ormonale, attivato in corso di scompenso cardiaco, è determinato dai diuretici antialdosteronici, come lo spironolattone, la cui azione è indipendente dall'attività diuretica e di risparmiatore di potassio. Un'altra categoria farmacologica estremamente efficace nel ritardare la progressione della malattia e nel migliorare la sintomatologia è rappresentata dai betabloccanti. Questi farmaci contrastano l'attivazione nervosa simpatica e riducono la frequenza cardiaca, il consumo di ossigeno e quindi il lavoro cardiaco, aumentando il tempo di riempimento diastolico e determinando un miglioramento della meccanica ventricolare e un'importante azione anti-ischemica e antiaritmica.
I farmaci ad azione inotropa comprendono una serie di molecole eterogenee per struttura e meccanismo d'azione che vengono accomunate dalla proprietà di incrementare la funzione contrattile del cardiomiocita. Per molte di queste, l'impiego non si è ancora dimostrato efficace, per altre è limitato a condizioni acute o, comunque, temporaneo nelle fasi di destabilizzazione delle forme croniche (dopamina, dobutamina, amrinone, enoximone). La digitale, farmaco storico nella terapia dello scompenso, è l'unico composto ad azione inotropa positiva impiegato cronicamente. I suoi effetti sono riconducibili a un aumento dell'inotropismo cardiaco e a un contemporaneo effetto bradicardizzante, che risulta particolarmente utile nei pazienti con fibrillazione atriale. Alcuni sottogruppi di pazienti possono attualmente beneficiare di presidi non farmacologici, come il pacemaker e il defibrillatore impiantabile, che hanno contribuito notevolmente a migliorare la sincronia ventricolare e a ridurre il rischio di morte improvvisa per eventi aritmici. Il trapianto cardiaco viene indicato nelle forme avanzate, refrattarie alla terapia (medica, interventistica o chirurgica) e in caso di severa disfunzione ventricolare con frequente necessità di ricovero per deterioramento dello stato di compenso.
Le conoscenze sempre più approfondite delle alterazioni molecolari alla base dello scompenso cardiaco e il continuo progresso delle scienze biotecnologiche negli ultimi decenni indirizzano la ricerca verso nuovi e promettenti orizzonti terapeutici, come quelli prospettati dalla terapia genica e dall'utilizzo delle cellule staminali. Diversi vettori e molti target molecolari sono stati studiati per la manipolazione genetica del miocardio con risultati molto differenti. Questa tecnica prevede l'introduzione in un organo di una porzione di cDNA, attraverso vettori virali (adenovirus, lentivirus, retrovirus, herpes simplex virus) e non virali (liposomi cationici, plasmidi nudi), capaci di integrarsi nel tessuto dove vengono rilasciati per esprimere una determinata proteina e modificare l'attività cellulare. Il recupero della funzione, in condizioni di ridotta contrattilità, è oggetto di numerosi studi preclinici. Sebbene molti di questi abbiano dimostrato che la manipolazione di alcune proteine cellulari, coinvolte nella regolazione dei livelli citoplasmatici di calcio (SERCA 2a, fosfolambano), sia in grado di migliorare la funzione sistolica, numerose sono ancora le incognite sulla sicurezza e sull'efficacia di tale metodica. Anche per la terapia cellulare, i campi di ricerca sono molto differenti. Essendo le staminali cellule totipotenti (cellule embrionali) o multipotenti (staminali midollari, mioblasti scheletrici, cellule progenitrici endoteliali, cellule ematopoietiche e mesenchimali), esse potrebbero essere indotte a produrre cellule cardiache o endoteliali differenziate, reintegrando il tessuto miocardico danneggiato, per esempio, da un insulto ischemico. I risultati incoraggianti di numerosi esperimenti preclinici, hanno permesso di effettuare studi su un piccolo numero di pazienti, i cui risultati però devono essere ancora considerati preliminari. La ricerca, pertanto, dovrà chiarire, attraverso studi condotti su larga scala e incrementando le attuali conoscenze, l'efficacia delle varie popolazioni cellulari, gli effetti a breve e lungo termine, il tempo ottimale e la metodica più efficace per il trapianto.
Bibliografia
Braunwald 1976: Braunwald, Eugene - Ross, John jr - Sonnenblick, Edmund H., Mechanisms of contraction of the normal and failing heart, 2. ed., Boston, Little, Brown, 1976.
Cardarelli 1891: Cardarelli, Antonio, Le malattie nervose e funzionali del cuore, Napoli, Cesareo Domenico, 1891.
Condorelli 1937: Condorelli, Luigi, Le miocarditi croniche. Relazione, Fidenza, Mattioli, 1937.
Condorelli 2001: Condorelli, Mario, L'insufficienza cardiaca congestizia acuta, Roma, CAPI-AIM Group, 2001.
Davani 2005: Davani, Siamak e altri, Can stem cell mend a broken heart?, "Cardiovascular research", 65, 2005, pp. 305-316.
Melo 2004: Melo, Luis G. e altri, Gene and cell-based therapies for heart disease, "The FASEB journal", 18, 2004, pp. 648-663.
Peschle, Condorelli 2005: Peschle, Cesare - Condorelli, Gianluigi, Cardiac stem cells: state of the art and future perspectives, "Annals of the New York Academy of Sciences", 1047, 2005, pp. 376-385.
Remme, Swedberg 2001: Remme, Willem J. - Swedberg, Karl, The task force for the diagnosis and treatment of chronic heart failure. Guidelines for the diagnosis and treatment of chronic heart failure, European Society of Cardiology, "European heart journal", 22, 2001, pp. 1527-1560.
Ross 2003: Ross, John jr, From pump to molecules, "Circulation research", 92, 2003, pp. 480-481.
Teodori 2004: Teodori, Ugo, Trattato italiano di medicina interna, a cura di Pietro Cugini e Giuseppe Guarini, 7. ed., Roma, Universo, 2004.
Yan 2005: Yan, Andrew T. e altri, Narrative review: pharmacotherapy for chronic heart failure: evidence from recent clinical trials, "Annals of internal medicine", 142, 2005, pp. 132-145.
Zipes 2001: Braunwald's heart disease: a textbook of cardiovascular medicine, edited by Douglas P. Zipes e altri, 6. ed., Philadelphia, Saunders, 2001.