Metalli
Metalli
I metalli nativi, quali il rame, l'argento e l'oro, sono tra i più antichi materiali usati dall'uomo, ma solamente con l'inizio della produzione di metalli e di leghe a partire dai minerali, i materiali metallici raggiunsero una posizione predominante riflessa nelle denominazioni Età del bronzo (in Europa a partire ca. dal 1800 fino al 700 a.C.) ed Età del ferro (ca. dal 1100 a.C.) per designare le tradizionali periodizzazioni della preistoria. Al giorno d'oggi i metalli e le leghe offrono innumerevoli possibilità applicative. La ricerca attuale si propone, in sostanza, di comprendere e ottimizzare le proprietà dei materiali metallici, come pure di svilupparne nuove combinazioni, anche con materiali non metallici. Metodi e concetti della fisica dello stato solido vengono utilizzati in misura sempre maggiore.
Accanto allo splendore metallico (alto potere riflettente nel campo della luce visibile), i metalli possiedono un'alta conducibilità sia termica sia elettrica. Questa caratteristica è dovuta alla presenza di portatori di cariche libere (ca. 1023 elettroni/cm3). La conducibilità elettrica σe è data dal prodotto della densità di portatori di cariche n per la carica q e per la mobilità μ. Mentre nei semiconduttori tipici l'influsso della temperatura T si manifesta primariamente in un aumento di n al crescere di T, la conducibilità tipica dei metalli è caratterizzata da una diminuzione della mobilità al crescere della temperatura (diminuzione del cammino libero medio a causa di un aumento della diffusione di elettroni da parte dei fononi). Altra caratteristica dei metalli è la buona duttilità (deformabilità plastica). La deformabilità plastica dei metalli può essere intesa come una conseguenza del legame metallico. A causa del fatto che la direzionalità dei legami è scarsamente pronunciata, le strutture cristalline dei metalli tendono a un riempimento dello spazio quanto più possibile elevato, cioè a tipi di reticolo semplici. Nelle strutture compatte semplici i supporti della deformazione plastica, ossia le dislocazioni, sono facili da produrre e molto mobili, cosicché un impedimento alla deformazione plastica (quindi la resistenza meccanica) si realizza soprattutto attraverso l'impedimento reciproco delle dislocazioni (incrudimento) e attraverso la deviazione dalla struttura del reticolo perfetto (atomi estranei, difetti reticolari, inclusioni non metalliche, fasi estranee precipitate o disperse). Queste inomogeneità controllano molte proprietà macroscopiche, perciò nelle ricerche sui metalli si è sempre interessati a conoscere bene la microstruttura, ossia le proporzioni locali nell'ambito microscopico e submicroscopico, sia sotto l'aspetto strutturale sia sotto quello chimico. Infine, in alcuni casi, i metalli possiedono particolari proprietà magnetiche. Le proprietà illustrate, però, non sono sufficienti per una distinzione netta (per es. nei confronti dei semiconduttori, dei polimeri, e così via). L'interpretazione fisica del legame metallico fornisce una definizione più precisa: si definiscono metallici tutti quei materiali che possiedono (anche alla temperatura T=0 K), grazie alla conformazione delle loro bande di energia, cariche libere ossia bande parzialmente occupate. I metalli costituiscono oltre l'80% degli elementi chimici. Miscele (leghe) di metalli tra di loro forniscono una grande varietà di materiali, le cui proprietà possono venire ulteriormente modificate tramite trattamenti termici, meccanici, termomeccanici e delle superfici. La scienza dei materiali metallici si prefigge di interpretarne le proprietà macroscopiche a partire dalla relativa struttura microscopica (atomica ed elettronica).
sommario
1. Classificazione e usi dei materiali metallici. 2. Trasformazioni di fase. 3. Plasticità dei materiali metallici. 4. Materiali magnetici. 5. Sollecitazione e durata dei metalli. 6. Prospettive. □ Bibliografia.
Classificazione e usi dei materiali metallici
Attualmente, il metallo utilizzato in quantità maggiori è il ferro, soprattutto per la produzione dell'acciaio. Come materiali da costruzione sono importanti, ma in misura minore, le leghe dell'alluminio, del magnesio e del titanio (a causa della loro bassa densità) e le leghe del nichel con l'aggiunta o meno di ferro (a causa della loro resistenza meccanica alle alte temperature). In virtù della loro buona conducibilità elettrica e termica, il rame e l'alluminio vengono impiegati nei generatori, nei motori e nei cavi, negli scambiatori di calore (refrigeratori, impianti di condizionamento d'aria), e così via. Il miglior conduttore a temperatura ambiente è l'argento, che, però, a causa del suo alto prezzo, viene impiegato come materiale di contatto solo in casi particolari (attrezzi speciali, elettronica). Nella lavorazione artistica sono preferiti i metalli chimicamente stabili (come i metalli nobili: argento, oro, platino, rodio). Le leghe di ferro, nichel e cobalto forniscono importanti materiali magnetici mentre le leghe del niobio sono materiali di base della tecnologia della superconduttività. I metalli nobili, i metalli di transizione e le loro leghe trovano impiego nella catalisi eterogenea; lo stagno, lo zinco, il nichel, il cromo e altri metalli vengono impiegati per la protezione dell'acciaio dall'ossidazione e dalla corrosione. Alcune leghe mostrano nelle trasformazioni di fase una 'memoria' di una forma precedente, che si può utilizzare bene in casi particolari; le leghe del tungsteno vengono impiegate come spirali per lampade a incandescenza e sorgenti di elettroni, a causa del loro alto punto di fusione, mentre il mercurio è notoriamente usato nei termometri e nei barometri per il suo basso punto di fusione e per la sua alta densità.
A causa della loro preminente importanza, i materiali ferrosi si distinguono da tutti gli altri materiali (metalli non ferrosi). Ai primi appartengono, oltre ai materiali ferrosi 'puri', quelli che, accanto agli elementi che a essi si accompagnano in natura (silicio, manganese), contengono, come principale elemento di lega, solo il carbonio (per es., la ghisa che contiene il 2÷6% in peso di carbonio). Per meno del 2% in peso di carbonio si parla di acciaio semplice non legato (0,03÷2% in peso di carbonio), che si lascia forgiare e deformare a freddo. Gli acciai con meno dello 0,6% in peso di carbonio si chiamano anche acciai da costruzione, mentre quelli con contenuto di carbonio più alto acciai per utensili. Se un acciaio contiene più del 5% circa di altri metalli in lega, per esempio alluminio, silicio, manganese, niobio, cromo, molibdeno, nichel, si chiama acciaio altamente legato, al di sotto del valore indicato acciaio basso-legato. Per i metalli non ferrosi esistono principî di classificazione diversi a seconda della densità, del punto di fusione, della stabilità chimica, del colore, e così via.
I prodotti di partenza per la produzione controllata dei materiali metallici si ottengono, eventualmente dopo più fasi intermedie, o dal trattamento dei minerali oppure da una loro lavorazione non convenzionale o anche dal riciclaggio di rottami. Molti metalli possono essere miscelati gli uni con gli altri allo stato liquido senza grosse limitazioni, tanto che la maggior parte dei materiali metallici viene prodotta mediante colata di un'opportuna lega allo stato liquido. Normalmente i liquidi metallici solidificano in forma cristallina. A velocità di raffreddamento molto elevate (>106 K/s), raggiungibili soltanto in strati sottili a contatto con un substrato freddo, si ottengono leghe amorfe. Nel processo di solidificazione vengono decisamente influenzate già molte proprietà del materiale. Il trattamento termico e meccanico (allo stato solido) permette, particolarmente per le leghe, un'estesa gamma di variazioni delle proprietà. Questi interventi possono riguardare le proprietà massive o anche solamente la superficie dei pezzi finiti. Se un getto riceve già la forma definitiva, che mediante lavorazione successiva deve subire ancora solo dei mutamenti insignificanti, si parla di getto in forma. Per una lavorazione ulteriore viene prodotto un lingotto, che in seguito verrà convertito, mediante fucinatura, laminazione, stiratura, taglio, rispettivamente in semilavorato, in pezzi finiti e, alla fine, mediante unione (saldatura, brasatura, ecc.), in struttura finita. Spesso i diversi stadi intermedi sono legati a trattamenti termici energeticamente dispendiosi o a processi di sagomatura dai costi elevati. L'applicazione della metallurgia delle polveri consente di ottenere in un solo passo, attraverso la pressione e la sinterizzazione di polveri, l'aggregazione delle particelle di polvere in un materiale massiccio e la formatura finale o suscettibile di ulteriore lavorazione.
Per la formazione di una fase cristallina è necessario che venga superata una certa dimensione critica del nucleo di cristallizzazione, la quale diminuisce con l'aumentare del sottoraffreddamento. I nuclei possono formarsi omogeneamente, sulla base di fluttuazioni statistiche, ma in pratica prevalgono i nuclei formati eterogeneamente attorno a impurezze solide e sulle pareti. Partendo da nuclei della struttura cristallina stabile capaci di accrescersi si formano nel liquido piccoli cristalli, per lo più con velocità di crescita dipendente dall'orientazione, fino a quando i diversi cristalliti (grani) non vengono a contatto e, uniti lungo i loro bordi (bordi di grano), danno luogo a una struttura policristallina. Solo quando si riesce a lasciar crescere nel liquido un singolo nucleo si ottiene un corpo cristallino solido senza bordi di grano, ossia un monocristallo. Dato che i bordi di grano portano già un contributo importante alla resistenza meccanica di un materiale, il controllo della dimensione dei grani durante la solidificazione è un compito tecnicamente importante. Durante la solidificazione, la distribuzione della temperatura influisce inoltre sulla distribuzione dell'orientazione dei singoli cristalliti. Si indica con 'tessitura' ogni deviazione dalla distribuzione statistica casuale dell'orientazione dei cristalliti nell'aggregato policristallino.
Trasformazioni di fase
Accanto alla trasformazione solido ⇆ liquido, ha luogo, allo stato solido, una serie di trasformazioni che sono legate alle variazioni di concentrazione e quindi alla diffusione, dette trasformazioni di fase controllate dalla diffusione. Inoltre, si possono avere, nei metalli puri e nelle leghe, transizioni di fase che corrispondono a piccoli ma correlati cambiamenti di posizione degli atomi, senza che siano necessari ampi processi di diffusione. Poiché la velocità di queste trasformazioni dipende solo debolmente dalla temperatura, esse vengono definite atermiche.
Diagrammi di fase
Come per la solidificazione, anche per le trasformazioni di fase allo stato solido la diminuzione dell'entalpia libera di Gibbs è la forza motrice che provoca il loro decorso. Nuove interfacce − e talvolta tensioni di coerenza elastiche − si oppongono alla trasformazione. Le fasi solide stabili a una data temperatura e la loro composizione si trovano, nei sistemi binari, ricercando la tangente comune alle curve entalpia libera/concentrazione per le diverse fasi possibili. Le trasformazioni ordine/disordine appartengono alle più importanti reazioni allo stato solido. Attraverso la messa a punto di una nuova periodicità del reticolo, una lega con ordine a lunga distanza assomiglia molto di più a un metallo puro per quel che riguarda le proprietà elettroniche. Infatti, le onde elettroniche non percepiscono più gli atomi estranei come un disturbo della simmetria di traslazione, bensì, a causa dell'ingrandimento dei vettori della base del reticolo ordinato, sono soltanto influenzate da nuovi confini delle zone di Brillouin, per determinate lunghezze d'onda e direzioni di propagazione.
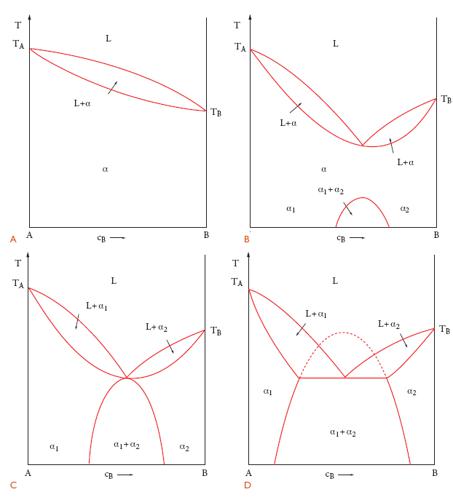
Allo stato solido può avvenire anche uno smescolamento, come illustra la serie di diagrammi di fase della fig. 2. Invece di un eutettico si rileva innanzitutto un abbassamento della temperatura di solidificazione e un campo di miscibilità completa allo stato solido, prima che appaia una lacuna di miscibilità per ulteriore raffreddamento.
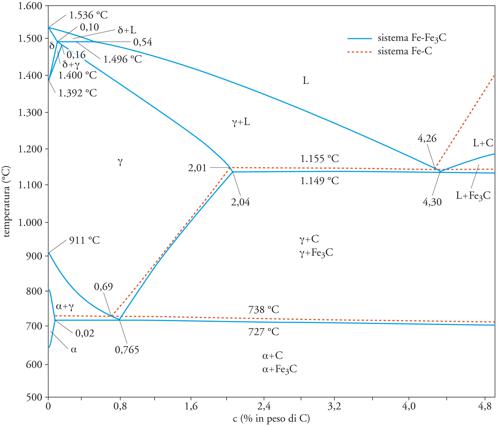
Ulteriori trasformazioni allo stato solido traggono origine da instabilità strutturali di una o più fasi interessate. Così, per esempio, il ferro puro solido si presenta in due forme allotropiche: a temperature tra 1536 °C e 1392 °C è stabile la fase δ cubica a facce centrate, che a 1392 °C si trasforma nella fase γ cubica a facce centrate (austenite), per riapparire a temperatura più bassa (come fase α, ferrite). In casi come questo si hanno diagrammi di fase più complicati, a causa delle diverse solubilità degli atomi di lega nelle due fasi. Nella pratica è molto importante il diagramma Fe-C, specialmente al di sotto di circa 6,7% in peso di C (≃ 25% atomi di C), composizione del carburo Fe3C, la fase all'equilibrio (metastabile) stechiometricamente più vicina. La fig. 3 mostra l'importante settore del diagramma binario Fe-C, in cui sono disegnate le linee di solubilità (leggermente spostate) dell'equilibrio (metastabile) con grafite.
Cinetica delle trasformazioni di fase
Le trasformazioni atermiche e le trasformazioni controllate dalla diffusione osservano leggi temporali diverse. Sebbene l'equilibrio stabile, per ogni composizione e per ogni temperatura, sia definito in modo univoco, fino alla sua instaurazione può intercorrere anche una serie di stati metastabili, la cui vita in molti casi dura così a lungo che in pratica essi forniscono materiali dalle proprietà utilizzabili. È proprio questa molteplicità delle strutture possibili che permette di impiegare materiali metallici in condizioni così diverse.
Nella formazione di nuove fasi nei solidi, accanto alla differenza nell'entalpia libera, sono di importanza decisiva le superfici limite tra fasi e le deformazioni elastiche (a causa del diverso volume atomico).
Nella teoria classica della nucleazione omogenea, la variazione dell'entalpia libera nella formazione di un nucleo della nuova fase è
[1] ΔG = VΔg + AγG + VΔgS,
dove V è il volume del nucleo, A la superficie del nucleo, Δg la differenza di energia libera specifica, γG l'energia specifica di superficie limite e ΔgS l'energia specifica di disadattamento (misfit energy).
La crescita di particelle di una nuova fase non può essere descritta in termini del tutto generali, anche nel caso di nucleazione omogenea. Per la crescita di particelle isolate è decisivo il rapporto della mobilità delle superfici limite col coefficiente di diffusione (quindi è decisiva la velocità dell'assemblaggio degli atomi diffondenti provenienti dalla superficie limite). In presenza di un'elevata mobilità delle superfici limite, la diffusione controlla la velocità e il raggio di una particella cresce secondo un processo di diffusione lineare
[2] R = (2Dαt)1/2
dove t è il tempo e α il parametro adimensionale determinato dalla soprasaturazione. Per basse soprasaturazioni la [2] è frequentemente verificata.
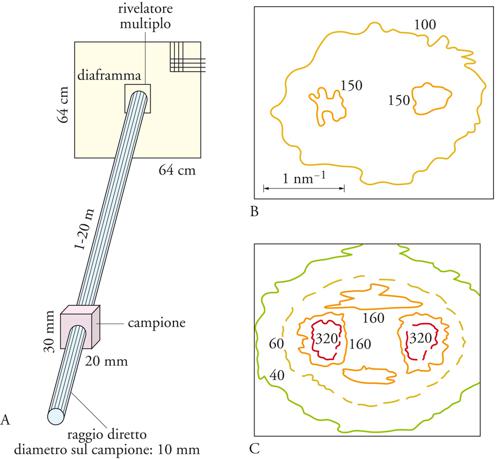
Bisogna però sottolineare come nucleazione, crescita, ridissoluzione per variazione delle dimensioni critiche del nucleo e riprecipitazione sono, in molti casi, frammiste l'una all'altra. Alcuni aspetti della nucleazione, della crescita e della ridissoluzione sono stati studiati in tempi recenti con diversi metodi ad alta risoluzione. La formazione di precipitati di diversa composizione può, per esempio, essere documentata con molta precisione con metodi di diffusione di raggi X o di neutroni, specialmente per mezzo della diffusione a basso angolo (fig. 4). La diffusione intorno al raggio primario ha una larghezza caratteristica, inversamente proporzionale alle dimensioni dei precipitati. Con i due tipi di radiazione si possono identificare bene particelle con diametri da circa 1 nm fino a parecchie centinaia di nm. I dettagli delle curve di intensità diffusa contengono anche informazioni sulla forma e sulla disposizione delle particelle diffondenti. Poiché i metalli assorbono i neutroni molto meno dei raggi X, con misurazioni mediante neutroni è possibile acquisire informazioni su campioni di maggior volume. Volumi tipici interessati dai neutroni sono dell'ordine di 0,1÷1 cm3, dai raggi X di circa 1 mm3 e dalla microscopia elettronica in trasmissione di 1 μm3 e anche meno. Attraverso la combinazione di microscopia elettronica, diffusione a basso angolo di neutroni e microscopia ionica a emissione di campo con sonda atomica (AP-FIM, Atom probe field ion microscopy) è stata studiata particolarmente a fondo, in tempi molto recenti, la formazione di particelle γ′ coerenti e ordinate (struttura L12) in leghe c.f.c. (cubiche a facce centrate) ricche in Ni.
Per trasformazioni discontinue si intendono reazioni di smescolamento nelle quali il fronte di reazione avanza in un campo monofasico instabile e lascia dietro di sé un campo bifasico. Tali reazioni sorgono in particolare nella solidificazione di liquidi eutettici e nella decomposizione eutettoidica, per esempio dell'austenite (Feγ-C) con lo 0,765% in peso di C, secondo γ → α+Fe3C.
Dietro il fronte di reazione costituito da superfici limite di fase sorgono due nuove fasi. In un'altra reazione di precipitazione discontinua ugualmente osservata, il bordo di grano diviene fronte di reazione e la struttura cristallina della matrice rimane invariata, per esempio secondo α → α′ + β, cambia solo la sua composizione. La nucleazione in queste reazioni allo stato solido avviene su un bordo di grano o su un'altra perturbazione e, in presenza di condizioni appropriate (rapporto delle energie interfacciali delle nuove fasi tra loro e con la fase finale, rapporto reciproco tra le quantità delle fasi, coefficienti di diffusione, ecc.), possono sorgere strutture di smescolamento lamellari. Come la velocità di nucleazione, anche la velocità di decomposizione per le reazioni eutettoidiche è bassa per un piccolo sottoraffreddamento, poi aumenta, per diminuire a un ulteriore sottoraffreddamento a causa della difficoltà della diffusione. La dipendenza dal tempo delle trasformazioni per una data temperatura viene spesso descritta per mezzo della crescita controllata da diffusione a numero di nuclei costante. Con ciò, a velocità di crescita costante, per la frazione trasformata di un campione (n>0, dipendente dalle particolarità della trasformazione) si ha in generale
[3] X(t) = 1 − exp(−t/τc)n
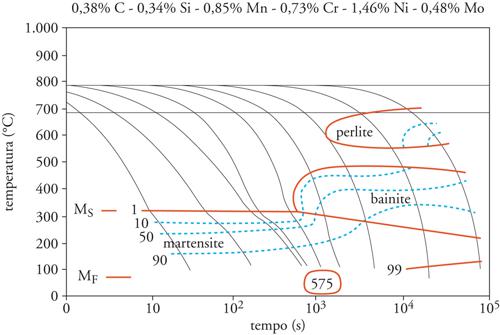
con un tempo caratteristico τc che, attraverso la densità dei nuclei (densità delle lamelle) e la velocità di crescita, dipende dalla temperatura. Questa relazione viene chiamata spesso equazione di Johnson-Mehl o anche equazione di Avrami. In un diagramma TTT (tempo-temperatura di trasformazione) si riportano, secondo queste rappresentazioni, curve di trasformazione che indicano l'inizio, gli stadi intermedi e la fine di una trasformazione. La fig. 5 mostra un esempio per un acciaio basso-legato con formazione di perlite tra circa 690 e 560 °C. Gli elementi di lega sostituzionali (in questo caso Ni, Mn, Cr, Si, Mo) ritardano la formazione della perlite, cosicché si può inquadrare più esattamente la microstruttura programmata. Tra circa 490 e 315 °C si ha un ulteriore campo di trasformazione, chiamato bainite. In esso si trova Fe3C finemente suddiviso e disperso, ma anche rilievi superficiali, che indicano una trasformazione per scorrimento, dunque componenti martensitici. Verosimilmente si separa prima Fe3C, per cui la temperatura MS sale nell'austenite. Se si raffredda abbastanza velocemente, per esempio secondo la curva di raffreddamento n. 575 della fig. 5, si giunge nel campo della formazione atermica della martensite. In questo caso, tra MS (temperatura iniziale della martensite) e MF (temperatura finale della martensite) una certa quantità di austenite si trasforma spontaneamente in martensite: la frazione di austenite trasformata dipende esclusivamente dalla temperatura.
Tramite la diminuzione di simmetria di una struttura altamente simmetrica, è possibile un gran numero di trasformazioni di fase atermiche che formano oggetto della ricerca attuale sullo stato solido. Per i materiali metallici, per esempio, appartiene a questa classe la trasformazione ω in leghe di titanio, zirconio e afnio. Invece della trasformazione, controllata dalla diffusione, della fase cubica a corpo centrato ad alte temperature nella fase esagonale compatta stabile a temperature più basse, si forma, dopo un rapido raffreddamento e attraverso un collasso parziale o totale di due piani (111) adiacenti della struttura cubica a corpo centrato, una fase metastabile trigonale o esagonale (fase ω). La causa di questa e di altre trasformazioni è la stabilità precaria della struttura cubica a corpo centrato. In presenza di pure forze centrali questo reticolo è instabile rispetto allo scorrimento su piani (110), ma viene stabilizzato a temperatura sufficientemente alta a causa dei maggiori contributi entropici. Anche la trasformazione atermica più importante, quella dell'austenite rapidamente raffreddata in martensite, ha la sua causa in un'instabilità che, tramite l'impedimento della diffusione degli atomi estranei in soluzione (in particolare C) e la forte soprasaturazione legata a ciò, porta a un ribaltamento coordinato di tutta una porzione del reticolo.
Plasticità dei materiali metallici
La deformazione plastica di materiali cristallini ha luogo prevalentemente tramite il movimento delle dislocazioni, talvolta anche tramite formazione meccanica di geminati o trasformazioni indotte da tensione. I metalli amorfi hanno un'elevata resistenza e scarsa deformabilità plastica poiché vengono meno i meccanismi di deformazione legati alla simmetria di traslazione del cristallo.
Nell'uso pratico i materiali metallici sono soggetti a sollecitazioni meccaniche molteplici, complicate e non sempre comprensibili in ogni particolare, combinate con influssi termici ed effetti di superficie. Nello sviluppo e nelle prove dei materiali alcuni metodi standard hanno dato dei buoni risultati. Un metodo di prova semplice, per quanto poco chiaro nei dettagli, per determinare la resistenza di un materiale alla deformazione plastica è la prova di durezza: un piccolo penetratore molto duro viene premuto con una forza nota sul materiale da esaminare e le dimensioni dell'impronta sono misurate eventualmente al microscopio. Come numero di durezza viene stabilito il quoziente tra il peso di prova F e la superficie dell'impronta che ne risulta (in MPa, ma spesso anche in kg/mm2). A seconda della forma del penetratore si distingue tra durezza Vickers (HV, penetratore piramidale, angolo di apertura 136°), durezza Rockwell (HRc, penetratore conico, angolo di apertura 120°) e durezza Knoop (HK, penetratore a forma di scalpello). Con una miniaturizzazione adatta si può misurare la durezza con una buona risoluzione locale (≤100 μm: microdurezza).
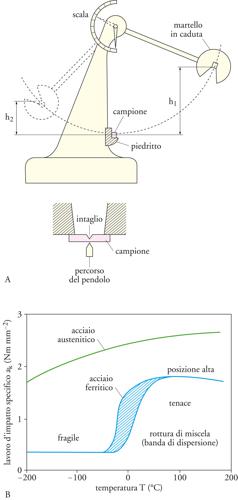
Un'altra prova, che parimenti interessa la massa del materiale e che fornisce una misura del lavoro di deformazione assorbito fino alla frattura è la prova di resilienza. A questo scopo si utilizza un pendolo-maglio, che colpisce un campione intagliato in modo standardizzato. In base all'altezza iniziale h1 e all'altezza di oscillazione del maglio h2 (fig.6), si determina l'energia ricevuta dal campione, la quale, riferita alla sezione del campione A, viene definita come resilienza specifica (J/m2). La fig. 6 mostra risultati tipici per l'acciaio, in particolare la temuta fragilità degli acciai ferritici a temperature intorno allo 0 °C, che dipende sensibilmente dal contenuto d'idrogeno.
Per lo studio del comportamento a frattura si è affermata, nell'ambito della meccanica della frattura, una certa standardizzazione. Durante l'allargamento di una cricca vengono rotti dei legami atomici stabili, cosicché si formano delle nuove superfici. In dipendenza dal comportamento plastico viene accumulato nelle vicinanze della cricca anche lavoro di deformazione. L'energia necessaria all'allargamento della cricca viene procurata in parte attraverso l'energia elastica accumulata, in parte attraverso lavoro esterno.
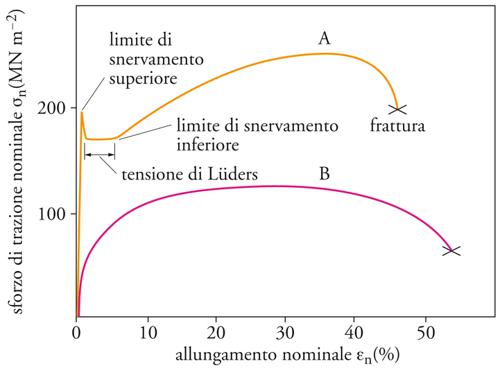
Particolarmente diffusi sono i procedimenti per la comprensione delle proprietà plastiche sotto un carico (ideale) uniassiale (trazione o compressione anche alternate). Nella prova di trazione uniassiale una provetta di forma allungata con sezione costante viene fissata in appositi afferraggi su una macchina di prova. Mentre un'estremità viene tenuta ferma, l'altra è vincolata, mediante una traversa mobile, a un meccanismo motore che dà la velocità di allungamento. Un dispositivo dinamometrico e un estensimetro registrano il carico istantaneo F e la variazione di lunghezza istantanea del campione. Da ciò si possono determinare l'allungamento (nominale) εn=Δl/l0 (l0 è la lunghezza iniziale) e la tensione (nominale) σn=F/A0 (A0 è la superficie della sezione trasversale). Per una comprensione più esatta della plasticità bisogna riferire allungamento ε e tensione σ alla rispettiva lunghezza l e alla rispettiva sezione A. Poiché il volume di un campione non varia grandemente durante la deformazione plastica, vale Al=A0l0, con il che ε=ln(1+εn), σ=F/A. Per una velocità di allungamento costante εn si registrano nella prova di trazione dinamica F e Δl e si ottengono curve di deformazione di cui nella fig. 7 è riprodotto l'andamento schematico per provette policristalline tipiche. La ripida ascesa iniziale è elasticamente reversibile e segue la legge di Hooke. Quando si raggiunge il pianerottolo di snervamento σ0 comincia il campo plastico, spesso (e in particolare negli acciai ferritici) con un'instabilità (limite di snervamento superiore) in presenza della quale comincia una deformazione plastica locale che si allarga a mo' di bande per tutto il campione (bande di Lüders). Si osserva poi un pianerottolo di snervamento con carico (unitario) al limite di snervamento superiore σh e un carico al limite di snervamento inferiore σu. Un'ulteriore significativa deformazione è possibile solo con un innalzamento della tensione, poiché la provetta diventa più resistente (più dura) a causa della deformazione plastica già subita. Questo incrudimento, misurato attraverso dσ/dε, non può però continuare a piacimento. Per dσn/dεn=0 la deformazione a trazione diventa instabile, il campione subisce una strizione e alla fine si giunge alla rottura.
Per la valutazione tecnica di un materiale sono importanti σ0, σu, la tensione nominale massima σUTS (UTS, Ultimate tensile strength) e l'allungamento totale fino a rottura εB. L'integrale ∫σdε dà il lavoro di deformazione accumulato per unità di volume, che è importante come misura della deformabilità di un materiale (costi di lavorazione, sicurezza in servizio). Nello studio dei materiali si esamina in dettaglio l'influsso di diversi parametri sulla curva di incrudimento. Di importanza del tutto particolare è l'influsso dei bordi di grano nei materiali policristallini. Per eliminarlo vengono deformati anche dei monocristalli che, soprattutto all'inizio della curva di incrudimento, presentano differenze caratteristiche a seconda dell'orientazione, della composizione e della microstruttura. Questo comportamento può essere compreso sulla base del tipo di processo plastico elementare cristallograficamente definito (scorrimento delle dislocazioni).
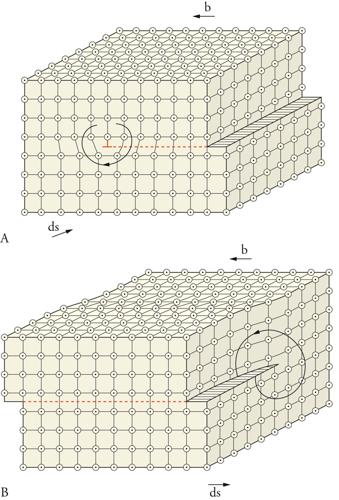
Nella deformazione plastica regioni cristalline subiscono uno spostamento reciproco. Nei monocristalli deformati in modo plastico si osservano sezioni spostate tangenzialmente. La variazione di forma può essere ricondotta perciò a processi di scorrimento microscopici. Se questi processi fossero spostamenti rigidi di parti di cristallo perfetto, l'una rispetto all'altra, allora si otterrebbero per la tensione di scorrimento di materiali duttili dei valori simili a quelli della tensione di rottura (resistenza teorica alla sollecitazione di taglio secondo Frenkel, circa il 10% del modulo di elasticità tangenziale GS). Le dislocazioni già costituite nella crescita del cristallo e altre prodotte durante la sollecitazione meccanica sono ora proprio i veicoli adatti alla deformazione plastica. Una dislocazione si caratterizza per il suo vettore di Burgers b e per un elemento lineare ds. La fig. 8 mostra ambedue i tipi di dislocazione chiaramente tra loro distinguibili, a spigolo e a vite, da cui si possono ottenere per combinazione altri casi. Dalla definizione di dislocazione segue che una dislocazione nel cristallo può cambiare la sua direzione, ma non il suo vettore di Burgers e, dunque, non può neanche terminare all'interno del cristallo. Essa deve andare fino alle superfici o deve chiudersi su se stessa ad anello. Nelle ramificazioni (nodi) resta costante la somma vettoriale dei vettori di Burgers.
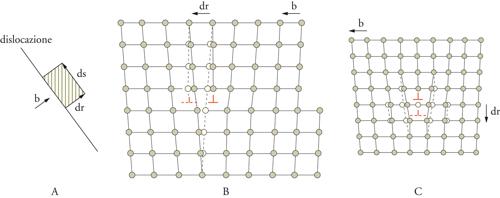
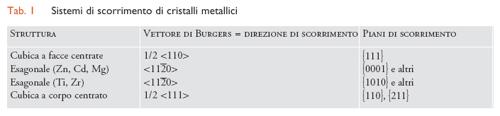
Dalla teoria dell'elasticità lineare risulta che, attraverso tensioni sia interne sia esterne, sulle dislocazioni vengono esercitate forze che agiscono sempre perpendicolarmente all'elemento lineare ds. In una dislocazione a vite b e ds sono paralleli, la dislocazione procederà anche su quel piano che è cristallograficamente ammissibile e in cui opera la maggiore componente della forza. Nelle dislocazioni a spigolo è particolarmente evidente il piano che contiene b e ds. Se si considera infatti (fig. 9 A) lo spostamento dr di un segmento di dislocazione ds orientato a piacere, allora entrambe le parti del cristallo al di sopra e al di sotto del piano definito da ds e dr vengono spostate l'una rispetto all'altra di b. Se i tre vettori sono linearmente indipendenti, allora si verifica una variazione di volume dV=b(ds×dr)=dr(b×ds); dV≠0 indica emissione di vacanze o di atomi interstiziali oppure assorbimento di atomi interstiziali presenti o di vacanze. Un tale movimento provoca un trasporto di materia controllato dalla diffusione. Solo quando (b×ds) è perpendicolare a dr, cioè la dislocazione si muove nel piano che è definito da b e ds, dV risulta uguale a 0 e la dislocazione si può muovere conservativamente. Questo movimento si chiama scorrimento (fig. 9 B), mentre la forma di movimento non conservativa si chiama risalita (climbing). Proprio per questa distinzione fondamentale, ha senso scomporre dF in una componente nel piano di scorrimento, la cui normale è data da n=b×ds, e una componente perpendicolare a questo. La forza di scorrimento per unità di lunghezza KG operante nel piano di scorrimento (perpendicolarmente alla direzione della dislocazione) ha il valore KG=τb, dove b è il modulo di b e τ è il modulo delle componenti della tensione di scorrimento operanti sul piano di scorrimento nella direzione di b. Si mostra, inoltre, che anche su una dislocazione a vite con lo stesso vettore di Burgers nello stesso piano agisce la stessa forza KG e così anche per tutte le situazioni intermedie. La forza di scorrimento in un dato piano è dunque data, indipendentemente dal carattere della dislocazione (angolo tra ds e b), solo da τb e agisce sempre perpendicolarmente alla linea di dislocazione (tab. 1).
Poiché l'energia delle dislocazioni è proporzionale al quadrato del vettore di Burgers, i più brevi vettori di traslazione della struttura corrispondente si comportano di preferenza come vettori di Burgers che giacciono nei piani atomici più compatti e le dislocazioni che giacciono in questi piani sono anche le più mobili. Ci si aspetta, dunque, che siano direzioni di scorrimento le direzioni cristallografiche corrispondenti a piccole distanze interatomiche e che siano piani di scorrimento i piani con indici di Miller semplici. È questo il caso dei metalli cubici a facce centrate (Cu, Ag, Au, Al, Ni, Feγ, ecc.) ed esagonali con grande interdistanza tra i piani di base (Zn, Cd, Mg). Nei metalli cubici a corpo centrato (Feα, V, Nb, Mo, Ta, W, Na, K), i piani {110} e {211} si presentano ambedue come piani di scorrimento (tab. 1).
La deformazione plastica dei metalli puri viene determinata essenzialmente attraverso l'interazione delle dislocazioni tra loro e con i bordi di grano. Nelle leghe entrano in gioco, a seconda del tipo e della distribuzione dei diversi atomi, ulteriori meccanismi d'interazione. In tutte le leghe tecniche c'è da attendersi un'aumentata resistenza intrinseca del materiale omogeneo, cioè un contributo all'indurimento degli atomi estranei disciolti omogeneamente. Con ciò s'intende un aumento di resistenza attraverso l'interazione reciproca tra singoli atomi disciolti e dislocazioni mobili.
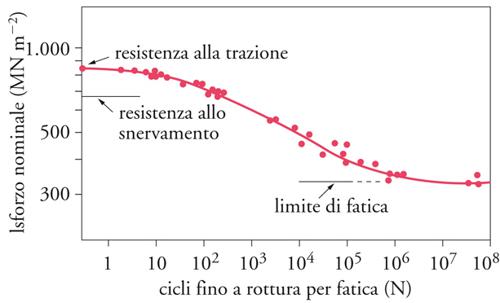
In seguito a sollecitazione ciclica si riscontra nei metalli e nelle leghe cristalline una serie di particolarità, che hanno la loro origine in speciali reazioni tra dislocazioni. Una conseguenza importante è la limitata durata di pezzi sottoposti a sollecitazione alterna con ampiezze di sollecitazione comprese fra il 50 e il 25% del carico di rottura nel saggio di trazione. Nella tecnica, il profilo della sollecitazione è spesso molto complicato, con ampiezze, frequenze e cicli di temperatura molto diversi. Una prova di trazione/compressione simmetrica, con frequenza costante, a temperatura costante e con ampiezza di sollecitazione costante, viene spesso utilizzata per la caratterizzazione della resistenza alle sollecitazioni alterne. Si determina il numero dei cicli di carico N fino alla rottura per fatica come funzione dell'ampiezza di tensione σ e si ottiene così la curva di Wöhler (curva S-N, stress vs number; fig. 10; N=1/4 corrisponde al carico di rottura nella prova di trazione). Il campo fino a N=104 si chiama fatica a basso numero di cicli o fatica oligociclica (LCF, Low cycle fatigue), al di sopra, fino a circa 106, fatica (fatigue). Per la maggior parte dei materiali (eccettuati, per es., Cu o Al puri) la curva di Wöhler decorre al di sopra di N≈106...107 quasi orizzontalmente, e si ottiene un limite di fatica (endurance limit) σe. Se si resta con i carichi al di sotto di questo valore, dovrebbe essere sopportato un numero qualsiasi di cicli di carico senza rottura per fatica.
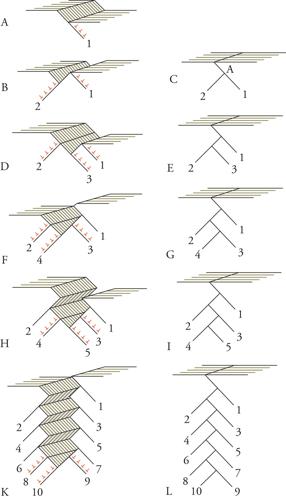
Le reazioni tra dislocazioni, l'inizio e l'allargamento della cricca nella sollecitazione alterna sono processi molto complicati. È fondamentale che una deformazione plastica provocata da una sollecitazione a trazione produca una disposizione delle dislocazioni che non è stabile rispetto all'inversione di tensione (effetto Bauschinger). Una parte delle dislocazioni può effettuare grandi percorsi anche sotto minime tensioni di segno contrario. Nelle numerose alternanze del carico si ottengono, infine, disposizioni delle dislocazioni completamente nuove, soprattutto dipoli e multipoli. Per una data ampiezza dell'allungamento plastico si raggiunge un valore di saturazione dell'ampiezza della sollecitazione. Lo scorrimento si concentra spesso in regioni nettamente delimitate di alta attività delle dislocazioni, dove i processi di incrudimento e di addolcimento all'incirca si equilibrano (bande di scorrimento persistenti) dando origine a occasionali deformazioni a valanga (strain bursts), che, a loro volta, conducono a grossolani gradini di scorrimento sulla superficie. Dalla superficie partono la maggior parte delle cricche di fatica. La formazione e l'apertura di una cricca con partecipazione di due sistemi di scorrimento, secondo un modello di P. Neumann, sono rappresentate nella fig.11. L'apertura delle cricche è, come la fig. 11 lascia vedere, sensibilmente dipendente dallo stato delle superfici neoformate, così che mezzi fluidi e gassosi, in cui un materiale metallico viene collocato, possono fortemente influenzare l'espansione della cricca (come pure la sua formazione).
Materiali magnetici
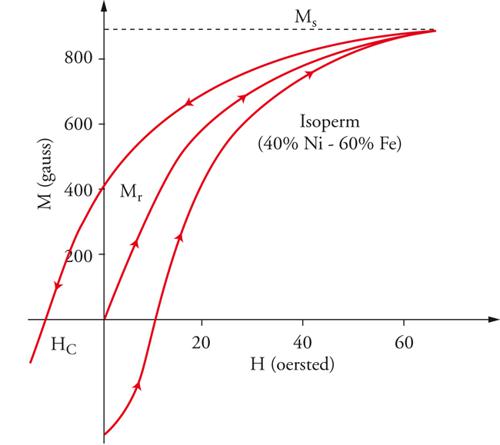
Le proprietà magnetiche e la superconduttività dei sistemi metallici sono di grande importanza nell'elettrotecnica. Particolare valore tecnico hanno le proprietà ferromagnetiche dei metalli e delle leghe. Il ferromagnetismo è caratterizzato da un forte aumento della densità di magnetizzazione M=(B−B0)/μ0 (dove B è l'induzione magnetica nel materiale, B0 è l'induzione magnetica nel vuoto, μ0 la permeabilità magnetica del vuoto) in funzione di B0 (=μ0H, misurata in tesla=104 gauss; H è il campo magnetico), nonché da un'isteresi e da una rimanenza (magnetica), cioè una magnetizzazione persistente allo scomparire del campo esterno. La fig. 12 mostra schematicamente l'andamento di M(H) per la curva di prima magnetizzazione di un ferromagnete inizialmente non magnetizzato e la seguente curva di isteresi in confronto con le sostanze diamagnetiche e paramagnetiche. La magnetizzazione di saturazione del ferromagnete è raggiunta quando tutte le regioni del campione hanno allineato i loro vettori di magnetizzazione parallelamente al campo applicato.
Premessa per il presentarsi del ferromagnetismo è l'esistenza di momenti magnetici atomici (elettroni non accoppiati) e un'interazione degli atomi magnetici che conduce a un accoppiamento di singoli momenti parallelamente l'uno all'altro. Questo accoppiamento ferromagnetico (campo molecolare) conduce a una magnetizzazione spontanea a cui si oppone, tuttavia, l'agitazione termica, così che la magnetizzazione di saturazione (identica a essa) decresce all'aumentare della temperatura per scomparire alla temperatura di Curie TC.
Il ferro è l'elemento di partenza più comune anche per la realizzazione di materiali magnetici. Proprietà magnetiche dolci si ottengono con leghe contenenti il 2-3% di atomi di silicio e decarburate per ricottura in idrogeno, per rendere inefficace il carbonio che causa l'isteresi. In queste leghe possono essere inoltre prodotte, dopo una deformazione appropriata e un trattamento di ricristallizzazione, delle tessiture speciali (per es., la tessitura di Goss nei lamierini per trasformatori), in cui prevalgono le direzioni di magnetizzazione facile. Le leghe di nichel e ferro (Permalloy, Hypemik, Hymu) hanno suscettibilità magnetiche particolarmente alte con basse isteresi e vengono utilizzate nella tecnica delle comunicazioni (schermatura). Aspettative particolari si pongono nel maggiore impiego dei metalli amorfi (Fe-Ni-B, ecc.) quali materiali magneticamente dolci. Poiché in questo caso viene a mancare l'anisotropia caratteristica dei cristalli, e quindi i bordi di grano, e, se si tratta di materiali di buona qualità, non esistono nemmeno altri ostacoli al movimento delle pareti di Bloch, si ottengono forze coercitive di meno di 1/30 di quelle delle leghe Fe-Si. Accanto all'impiego come nuclei di trasformatori, sono particolarmente utili per la loro flessibilità le lamine di schermatura intrecciate da nastri amorfi sottili.
Per materiali magneticamente duri (in uso per magneti permanenti) vengono ricercati un alto magnetismo residuo e un'elevata forza coercitiva. Per una grande forza coercitiva è favorevole un'elevata anisotropia dei cristalli (vengono resi più difficili i processi di rotazione) e la mobilità delle pareti di Bloch deve essere ridotta attraverso ostacoli appropriati. Nel caso estremo di pareti di Bloch completamente immobili, sono ancora possibili solo processi di rotazione. Ciò vale particolarmente per piccole particelle ferromagnetiche in una matrice: per diametri delle particelle di meno di ∼100 nm, non ci sono più all'interno pareti di Bloch (particelle a un solo dominio), cosicché a un'alta anisotropia del cristallo segue un'elevata forza coercitiva. Classici materiali magneticamente duri sono ‒ oltre agli acciai al carbonio con Cr e Co ‒ soprattutto leghe di Al-Ni-Co di diversa composizione, che mostrano indurimento per precipitazione. I precipitati fini e coerenti appaiono per smescolamento di una fase cubica a corpo centrato omogenea a elevate temperature. Negli ultimi anni si sono messi in evidenza soprattutto composti intermetallici di cobalto con metalli delle terre rare (per es., samario e ittrio) come materiali magneticamente duri. Essi permettono, a causa dei loro alti valori per il massimo del prodotto BH ‒ che serve come termine di paragone per magneti permanenti ‒ una miniaturizzazione dei componenti attivi negli apparecchi elettromeccanici (per es., stampanti, motori passo-passo, e così via).
Sollecitazione e durata dei metalli
Gli influssi dell'ambiente e del contatto con altri materiali ai quali sono esposti hanno una grande importanza nella valutazione della stabilità e della durata dei materiali metallici, accanto alle sollecitazioni meccaniche già trattate.
Eccetto l'oro e il platino, tutti i metalli sono chimicamente instabili in presenza di ossigeno (o altre sostanze ossidanti). Tuttavia, oggetti metallici massivi restano inalterati a lungo, poiché l'ossidazione incomincia alla superficie e un partner di reazione deve diffondere attraverso l'ossido per reagire ulteriormente con il resto del metallo. Sono perciò necessarie energie di attivazione maggiori rispetto ai semplici metalli. Uno strato superficiale continuo di ossido offre, dunque, a temperature non troppo alte, una buona protezione contro un'ulteriore ossidazione. All'inizio, sotto l'influenza dei campi elettrici tra le superfici limite metallo-ossido e ossido-superficie esterna, la crescita, controllata dalla diffusione, dello strato di ossido segue una legge temporale logaritmica e poi parabolica. A temperature più elevate, quando la diffusione può risultare accelerata, ci si aspetta che lo spessore dello strato dipenda linearmente dal tempo, quando la reazione di ossidazione, indipendentemente dallo spessore dello strato, determina essa stessa la velocità. Si osserva un analogo comportamento in funzione del tempo quando l'ossidazione comporta un forte cambiamento di volume, cosicché la scaglia di ossido (gli ossidi sono fragili), dopo aver raggiunto un piccolo spessore, si rompe e perciò altro metallo fresco viene esposto all'ambiente ossidante. La grande differenza nel comportamento all'ossidazione dell'alluminio e del ferro si spiega solamente così, sebbene in pratica agiscano anche processi elettrochimici. In presenza di acqua (in ambiente umido o liquido), diventano attive differenze nel potenziale elettrochimico in posti diversi della superficie e si giunge all'ossidazione anodica (corrosione elettrochimica). Già nei metalli puri i bordi di grano sono attivi come anodi locali, poiché gli atomi lì giacenti possiedono un più alto potenziale chimico. Un vantaggio dei metalli amorfi è la loro migliore resistenza alla corrosione a causa dell'assenza di bordi di grano. Altre cause della corrosione, come tensioni interne (variazioni della densità di energia elastica), fluttuazioni di concentrazione e presenza di fasi diverse (precipitati, impurezze), conducono tuttavia, anche indipendentemente dalla struttura dei grani, a processi di corrosione. Riguardo al corso del processo di corrosione in presenza di diversi elementi, decide la posizione dei metalli nella serie delle tensioni (nell'elenco dei potenziali di elettrodo), il cui punto zero è stato fissato arbitrariamente per la reazione: H2 → 2H++2e− .
L'acciaio inossidabile viene ottenuto nel modo più facile attraverso aggiunta di cromo. Sebbene il cromo sia anodico rispetto al ferro, viene ridotta fortemen-te la velocità di corrosione, poiché sulla superficiemetallica si formano ioni CrO32− che impediscono l'ulteriore corrosione (passivazione). La passivazione e la galvanizzazione (introduzione di uno strato più nobile attraverso immersione in bagno metallico fuso o attraverso deposizione elettrolitica) proteggono i metalli dalla corrosione. Anche i rivestimenti con materiali chimici inerti (lacche organiche, smalti, ecc.) servono a questo scopo. Attualmente, un grande numero di processi chimici a umido e a secco (per es., CVD, Chemical vapor deposition) e fisici (per es., PVD, Physical vapor deposition) vengono applicati per il rivestimento di metalli e sottoposti a ulteriori studi. Accanto alla rottura e ai processi di corrosione, la cui azione viene accelerata attraverso sollecitazione meccanica alternata (per es., per tensiocorrosione) anche processi di erosione e di usura sono responsabili della limitazione della durata dei materiali metallici (e dei non metallici). Oltre a lubrificanti adatti (che ugualmente possono influenzare la corrosione), sono opportuni, per limitare l'usura, o modificazioni speciali delle proprietà superficiali del materiale oppure strati protettivi, che possono essere applicati saldamente (nitruro di titanio, carburo di titanio).
Prospettive
L'umanità, dunque, possiede un'esperienza lunga e ampia dei materiali metallici; tuttavia la molteplicità delle loro proprietà e delle loro caratteristiche non è stata ancora adeguatamente compresa e utilizzata. La consapevolezza sempre più approfondita dell'ambiente, lo scarseggiare dell'energia e delle materie prime e la crescente concorrenza in campo mondiale stimolano a sviluppare sempre più le possibilità che i materiali offrono in tutti i campi e a ricercare soluzioni nuove. Per questo è necessario il pieno impiego delle conoscenze della ricerca di base e del potenziale insito nei più moderni metodi di ricerca. I metalli saranno sostituiti, non solo occasionalmente, dai non metalli, dei quali subiranno la concorrenza, ma troveranno ulteriori possibilità di applicazione adatte alle loro specifiche proprietà.
Bibliografia
Barrett, Massalski 1980: Barrett, Charles S. - Massalski, Tadeusz B., Structure of metals, 3. ed., Oxford, Pergamon, 1980.
Buckel 1984: Buckel, Werner, Supraleitung, Weinheim, Physik-Verlag, 1984.
Cahn, Haasen 1983-1992: Physical metallurgy, 2. ed., edited by Robert W. Cahn, Peter Haasen, Amsterdam, North-Holland, 1983-1992.
Haasen 1984: Haasen, Peter, Physikalische Metallkunde, Berlin-New York, Springer, 1984.
Heck 1974: Heck, Carl, Magnetic materials and their applications, London, Butterworths, 1974.
Hornbogen 1987: Hornbogen, Erhard, Werkstoffe, 4. ed., Berlin-New York, Springer, 1987.
Hull, Bacon 1984: Hull, Derek - Bacon, David J., Introduction to dislocations, 3. ed., Oxford, Pergamon, 1984.
Smallman 1985: Smallman, Raymond E., Modern physical metallurgy, 4. ed., London, Butterworths, 1985.
Van Vlack 1980: van Vlack, Lawrence H., Elements of ma-terials science and engineering, 3. ed., Reading (Mass.), Addison-Wesley, 1980.