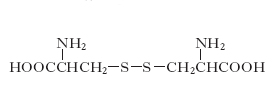cistina
Composto chimico solforato costituito dall’interazione dei gruppi SH di due molecole di cisteina e conseguente formazione di un ponte disolfuro S–S. Ha formula (
acido di-α-ammino-β-tiolpropionico). Entra nella costituzione di molte proteine. La quantità dei ponti S–S di c. si trova con la massima frequenza nella cheratina, mentre alcune proteine dei Vertebrati ne sembrano del tutto prive, e le proteine globulari, compresi gli enzimi, ne contengono quantità variabili. In genere, nei tessuti degli organismi viventi, la c. è tra gli amminoacidi meno frequenti (1-2% dei residui totali) a eccezione della pelle e dei peli che ne contengono fino al 5%. La c. si trova inoltre come amminoacido libero in quasi tutti i fluidi biologici. La c. è un amminoacido non essenziale per l’uomo e gli animali (può essere sintetizzato dalla metionina). Per riduzione reversibile dà origine a due molecole di cisteina: pertanto i due amminoacidi seguono nell’organismo le stesse vie metaboliche. I legami disolfuro sono in grado di unire catene polipeptidiche diverse o creare ponti tra zone distanti di una stessa catena, determinando così la forma della molecola e la posizione relativa nello spazio dei gruppi che la costituiscono.
La cistinosi è una malattia ereditaria connessa a un’alterazione del metabolismo degli amminoacidi e segnatamente della c., che si deposita in vari organi e viene abbondantemente eliminata con le urine (cistinuria). La c., poco solubile, tende ad accumularsi nelle cellule reticolo-istiocitarie del rene (oltreché del fegato, della milza, dei linfonodi e della congiuntiva), provocando alterazioni della funzione tubulare renale. Se la malattia non è tempestivamente diagnosticata e trattata, la prognosi è severa. La cistinuria si riscontra in vari quadri morbosi e anche in un’altra affezione ereditaria per lo più benigna (a volte addirittura asintomatica), ma talora accompagnata dalla formazione di calcoli renali di cistina.