vapore
vapore Lo stato gassoso di una sostanza.
Fisica
Propriamente, un aeriforme ha il nome di v. quando la temperatura a cui si trova la fase gassosa è inferiore alla temperatura critica (in caso contrario ha nome di gas). Di conseguenza, a differenza di un gas, un v. può trovarsi in presenza del suo liquido in condizioni di equilibrio stabile con esso (e, a temperature più basse, anche con la fase solida, come nel caso del v. di mercurio o del v. di zolfo). Quando ciò si verifichi il v. si dice saturo o in condizioni di saturazione.
La pressione del v. saturo (o tensione di v.) dipende unicamente dalla sua temperatura, crescendo rapidamente al crescere di questa; a differenza di ciò che si verifica nei gas, essa è indipendente dal volume, i cui eventuali aumenti o diminuzioni sono, per così dire, compensati da evaporazioni del liquido o da condensazioni del vapore. Da sostanza a sostanza, a parità di temperatura, la tensione di v. saturo generalmente varia, risultando tanto più alta quanto maggiore è la volatilità della sostanza in esame (per l’acqua a 20 °C la pressione di v. saturo è di 23,2 mbar; alla stessa temperatura, per il mercurio è di 1,6∙10-3 mbar e per l’etere di 577 mbar).
Se si riscalda un v. saturo umido, cioè un v. saturo in presenza del suo liquido (➔ stato), senza peraltro raggiungere la temperatura critica, il liquido va progressivamente evaporando sino alla sua totale scomparsa: si ha v. saturo secco. Continuando a riscaldarlo, ma sempre in modo che la sua temperatura resti al disotto della temperatura critica, si ha quel che si chiama v. surriscaldato. Il comportamento dei v. surriscaldati è del tutto diverso da quello dei v. saturi, avvicinandosi piuttosto a quello dei gas, dai quali principalmente si distinguono per il fatto che si riesce a liquefarli isotermicamente semplicemente comprimendoli. Oltre che con una compressione un v. può essere condensato con raffreddamento: la condensazione si produce non appena si sia raggiunto il punto di condensazione. Se però si opera con grande rapidità su vapori accuratamente depurati di particelle elettrizzate o di pulviscolo, si riesce a oltrepassare il punto di condensazione senza che questa si produca: si determina una situazione di equilibrio estremamente instabile detta soprasaturazione.
Il v. si produce per evaporazione (o vaporizzazione) o per sublimazione nel caso, rispettivamente, di una sostanza allo stato liquido o allo stato solido.
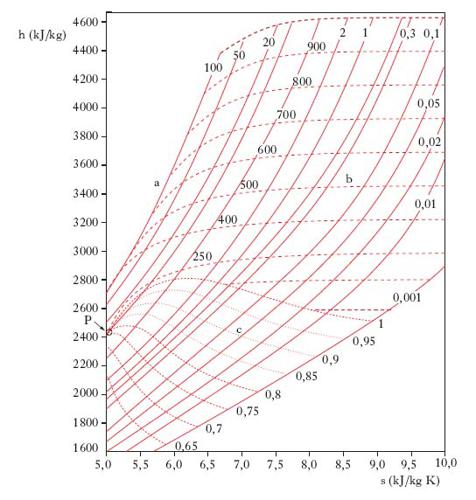
Il vapore acqueo è il v. di gran lunga più diffuso in natura e più usato nelle applicazioni pratiche: in particolare, prodotto in appositi generatori o caldaie, serve per azionare motrici alternative o turbine, per riscaldare ambienti o altre sostanze, nonché come reagente chimico o come fluido per lo spurgo di ambienti. In natura è disponibile in particolari zone vulcaniche. Di grande utilità per i calcoli connessi agli impieghi tecnici del v. acqueo è il diagramma di Mollier, di cui la fig. rappresenta la regione più significativa dal punto di vista applicativo. In ascisse è l’entropia specifica s (cioè riferita all’unità di massa del fluido), in ordinate l’entalpia specifica h; pertanto le trasformazioni isoentalpiche sono rappresentate da linee orizzontali, quelle adiabatiche da linee verticali. Sul diagramma di Mollier sono tracciate: a) le curve limite del v. e del liquido, che si congiungono nel punto critico P (cui corrispondono una temperatura di 375 °C e una pressione di 22,1 MPa); b) le curve isobare a, che sono rettilinee nella zona del diagramma all’interno delle curve limite (cioè là dove coesistono liquido e v.), mentre nel campo del v. surriscaldato presentano andamento esponenziale con inclinazione progressivamente crescente; c) le curve isoterme b, che sono rettilinee e coincidenti con le corrispondenti isobare nella zona in cui, coesistendo liquido e v., il sistema è monovariante, mentre nel campo del v. surriscaldato sono linee con inclinazione molto minore delle isobare; d) le curve a titolo in v. costante c, che nella zona del diagramma all’interno delle curve limite intersecano le isobare dividendole in parti proporzionali al valore del titolo, in quanto questo varia in relazione alla quantità di calore somministrata e, quindi, alla variazione di entropia. Sul diagramma di Mollier sono talvolta tracciate anche le curve isocore, che sono rette con inclinazione maggiore delle isobare. Il diagramma di Mollier per il v. acqueo consente, pertanto, di determinare entalpia ed entropia di 1 kg di fluido, noti che siano pressione, temperatura e titolo; in tal modo è possibile calcolare le variazioni entalpiche ed entropiche connesse a trasformazioni che intervengono in numerosi problemi di termodinamica e di meccanica dei fluidi.
Tecnica
Vaporizzatura Nell’industria tessile, operazione di rifinitura sia dei filati sia dei tessuti che si esegue attraverso un trattamento ad alta temperatura, in presenza di v. d’acqua saturo. L’effetto riproduce quello che potrebbe realizzarsi in acqua calda, senza però sottoporre il semilavorato all’azione diluente e dilavante di quest’ultima. Per i filati la vaporizzatura ha lo scopo di fissare la torsione; nel caso dei filati composti da fibre retrattili, sotto l’azione del v. le fibre si arricciano in maniera permanente e il filato risulta voluminizzato con particolari caratteristiche di gonfiezza e sofficità. Nel caso dei tessuti la vaporizzatura ha obiettivi diversi in relazione al tipo di fibra: per i tessuti di lana ha lo scopo di eliminare il lucido eccessivo eventualmente presente nella stoffa dopo il decatissaggio o la pressatura e di rendere più dolce la mano del tessuto; per i tessuti di cotone o composti da fibre cellulosiche, pure o in mischia con fibre sintetiche, la vaporizzatura fissa il colorante, o serve per polimerizzare sul tessuto le resine o altri prodotti ausiliari precedentemente distribuiti.
Nell’industria della seta, il trattamento con v. dei bozzoli che si effettua dopo la bagnatura per facilitare l’operazione di trattura.
Nella lavorazione del legno, il procedimento a cui sono sottoposti alcuni legnami per renderli plastici e poterli così agevolmente curvare o tranciare, oppure per prepararli a un successivo trattamento: consiste nel trattare con v. i tronchi, non ancora scortecciati, ma tagliati nella lunghezza adatta; la vaporizzatura può essere effettuata anche per modificare il colore di alcune essenze legnose e per impedire la formazione di muffe. Vaporizzazione Generazione di v. per la produzione di forza motrice o per riscaldamento o per utilizzazione in processi industriali. (➔ caldaia). Vapor lock Formazione di un tampone di v. fra il carburatore e la camera di scoppio che ostacola il regolare deflusso del carburante. L’inconveniente, che può provocare anche l’arresto del motore, è dovuto a un’eccessiva volatilità della benzina.