indicatore
Chimica
Sostanza che, al variare della natura della soluzione in cui è contenuta, subisce modificazioni percepibili all’occhio, in particolare il viraggio del colore e la formazione di un precipitato. Gli i. sono usati particolarmente in chimica analitica per rendere visibile il punto finale o punto di equivalenza di una titolazione.
L’indicatore universale di pH è costituito da una miscela di i. opportunamente scelti, che può assumere una decina di differenti tonalità di colore a seconda del pH della soluzione; è corredato da una scala cromatica che fornisce la corrispondenza fra colorazione e pH.
Gli indicatori per reazioni di neutralizzazione sono coloranti organici che si comportano da acidi o da basi deboli e che hanno la caratteristica di essere diversamente colorati a seconda che siano prevalentemente nella forma dissociata o indissociata. Un i., acido debole, di formula generica HIn (dove In indica la parte acida) in soluzione acquosa si dissocia secondo lo schema
HIn ⇄ H+ + In–.
Si supponga che le molecole HIn e gli ioni In– diano luogo a colori diversi. Il colore che tale i. impartisce alla soluzione in cui è posto dipende dal rapporto In–/HIn che a sua volta dipende dalla concentrazione degli ioni H+ della soluzione. Perché si abbia la percezione del colore di una delle due forme, occorre che il rapporto In–/HIn raggiunga un certo valore limite (in generale ciò avviene quando la concentrazione di una specie è almeno 10 volte quella dell’altra) e quindi il passaggio da una colorazione all’altra non avviene a un determinato valore del pH, bensì entro un certo intervallo di pH dipendente dalla natura dell’indicatore.
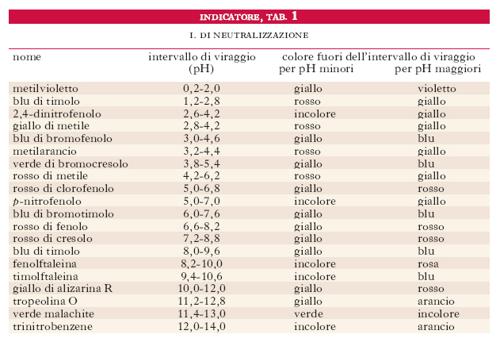
Si dicono indicatori dicromi quelli nei quali sia gli ioni sia le molecole indissociate sono colorati, sia pur diversamente (per es., dimetilarancio) e indicatori monocromi quelli per i quali solo gli ioni o solo le molecole indissociate sono colorati (per es., fenolftaleina). Nella tab. 1 è riportato un elenco degli i. più usati. Gli i. di questo tipo possono anche essere impiegati per determinare il pH di una soluzione e quelli la cui zona di viraggio è compresa intorno a 7 permettono di stabilire se una soluzione è acida o basica. Fra gli i. per reazioni di neutralizzazione sono da includere anche gli indicatori di fluorescenza; essi alla luce solare o, meglio, alla luce ultravioletta riescono a mettere in evidenza la variazione di pH di una soluzione attraverso la comparsa della fluorescenza; questo tipo di i. è assai utile per soluzioni colorate o torbide con le quali è impossibile l’uso dei normali indicatori.
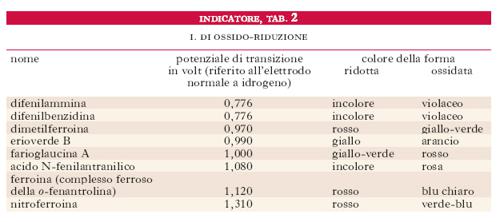
Gli indicatori per reazioni di ossido-riduzione si suddividono in due gruppi: quelli che reagiscono con un composto presente nella soluzione e quelli che nella forma ossidata hanno un colore diverso da quella ridotta. Esempi di i. appartenenti al primo gruppo sono l’amido, usato per rivelare lo iodio elementare come ossidante, e il solfocianuro di potassio usato per rivelare gli ioni ferrici. Gli i. del secondo gruppo sono coloranti organici (difenilammina, difenilbenzidina, ferroina e derivati ecc.) che hanno la proprietà di essere diversamente colorati a seconda che siano nella forma ridotta od ossidata. Il passaggio da una forma all’altra avviene a un certo potenziale, detto potenziale di ossido-riduzione, dipendente dalla natura dell’indicatore. Poiché nelle titolazioni basate su reazioni di ossido-riduzione al punto di equivalenza corrisponde un determinato potenziale di ossidazione della soluzione, questo potrà essere apprezzato visivamente facendo la titolazione in presenza di un i. che al potenziale suddetto subisca variazioni di colore. Nella tab. 2 sono riportati alcuni i. di ossido-riduzione.
Gli indicatori per reazioni con formazione di complessi o di precipitati si distinguono in i. di adsorbimento e in i. che, al punto di equivalenza, formano complessi (o anche precipitati) colorati.
Gli indicatori di adsorbimento sono composti organici che in determinate condizioni vengono adsorbiti dalla superficie di un precipitato facendone variare il colore (per es., la fluoresceina impiegata nella titolazione degli ioni cloro con nitrato di argento). Via via che alla soluzione di un cloruro si aggiunge nitrato di argento, precipita cloruro di argento bianco che adsorbe in superficie un eccesso di ioni cloro. Poiché questi sono adsorbiti di preferenza rispetto alla fluoresceina, il colore del precipitato resta invariato finché nella soluzione sono presenti ioni cloro. Al punto di equivalenza, aggiungendo un piccolo eccesso di nitrato d’argento, gli ioni argento sono adsorbiti dalla superficie del precipitato che, caricandosi positivamente, adsorbe dalla soluzione la fluoresceina colorandosi in rosa. A questo punto se si aggiunge un eccesso di ioni cloro la fluoresceina viene desorbita e il precipitato diventa nuovamente bianco.
Ecologia
Indicatori ecologici (o bioindicatori)
Organismi appartenenti a specie sia animali sia vegetali (specie chiave) sensibili alle variazioni ambientali, quelli cioè la cui presenza (o assenza, o abbondanza relativa) riflette con accuratezza il grado di variazione delle condizioni ambientali e quindi può essere considerata una misura della variazione ambientale stessa. Vengono utilizzati per studi di inquinamento ambientale: così, per es., la ricchezza in specie di una comunità, che esprime il numero di specie presenti per unità di area o di volume, fornisce una efficace valutazione della ‘buona qualità’ dell’ambiente. L’uso di i. ecologici è di grande interesse per studi di valutazione dell’eutrofizzazione delle acque. Sono considerati i. anche gli i. di esposizione, che si basano su variazioni biochimiche o fisiologiche degli organismi (➔ biomarker).
Economia
Indicatori economici
Variabili economiche che si ritiene siano più significative ai fini della valutazione dell’andamento dell’economia del paese considerato. Per es.: tasso di disoccupazione, tasso d’inflazione, utilizzo degli impianti, produzione industriale, inchieste sulla fiducia ecc. (➔ anche indicatóri econòmici).
Tecnica
L’i. generalmente non è uno strumento o un dispositivo a sé stante, ma fa parte di un sistema di misurazione: esso, propriamente, è quel componente che serve specificamente a indicare il valore della grandezza misurata oppure a indicare particolari condizioni legate alla grandezza in questione. In genere si tratta di uno strumento a indice e scala graduata (indicatore analogico), o a visualizzazione numerica (indicatore digitale). Se non interessa conoscere il valore di una grandezza quanto piuttosto il fatto che quest’ultima superi un certo valore o sia inferiore a un certo valore, invece che da uno strumento a indice l’i. può essere costituito da un semplice avvisatore luminoso, acustico o meccanico. L’indicatore di livello è un dispositivo per misurare il livello dell’acqua (o di altri liquidi) in un recipiente; nella sua forma più semplice, è basato sul principio dei vasi comunicanti ed è costituito da un tubo di vetro in comunicazione con il recipiente. L’indicatore di pressione è invece un apparecchio per tracciare il diagramma della pressione nel cilindro di una macchina alternativa (motrici a vapore, motori a combustione interna, compressori o pompe) in funzione della posizione dello stantuffo, cioè in funzione del volume del cilindro; da tale diagramma, che costituisce il ciclo di funzionamento della macchina, è possibile dedurre il lavoro compiuto in un ciclo e quindi, noti che siano la frequenza dei cicli e il tipo di macchina, risalire alla potenza.
Molti strumenti di bordo di un aeromobile sono denominati i.; la presentazione può essere meccanica o elettronica. Per quest’ultimo tipo vengono impiegati pannelli a cristalli liquidi o tubi a raggi catodici, sui quali compaiono contemporaneamente le funzioni di due o più i. e strumenti convenzionali (➔ strumento). L’RMI (radio magnetic indicator) costituisce l’i. della bussola giromagnetica e indica due rilevamenti magnetici rispetto alle stazioni a terra dei sistemi di radionavigazione.
In radiotecnica, indicatore panoramico è un apparato radioricevente atto a rivelare visualmente sullo schermo di un tubo a raggi catodici la presenza di segnali radio compresi in una data gamma di frequenza. L'indicatore di gamma è un dispositivo meccanico od ottico che in un radioricevitore plurigamma indica la gamma su cui questo è in funzione.
Nell’ingegneria gestionale, strumento che organizza l’informazione disponibile (dati, parametri ecc.) e misura una situazione o un fenomeno che caratterizzano un’organizzazione, un gruppo o una società nel suo insieme. La complessità dell’i. varia notevolmente a seconda dei casi considerati, in ragione di ciò che deve essere misurato e degli obiettivi che ci si pone con il processo di misurazione. Solitamente, la costruzione di un sistema di i. è funzionale alla necessità di controllare, governare e programmare un insieme di attività complesse, che proprio grazie a tale sistema possono essere in qualche modo sintetizzate, comprese e gestite. Per quanto riguarda gli strumenti concreti utilizzati per rappresentare gli i., parte importante giocano l’informatica e i sistemi informativi, che offrono applicazioni adatte alla rappresentazione degli i., spesso utilizzando interfacce grafiche in grado di permettere una visualizzazione agevole e intuitiva dei valori degli indicatori. In tale contesto, si sono sviluppate teorie, metodologie e discipline che hanno cercato di fornire un fondamento concettuale all’introduzione di i. come misuratori dell’andamento di un’organizzazione e, in particolare, di un’azienda. Per es., i cosiddetti cruscotti aziendali o cruscotti di un’organizzazione sono insiemi di i. più o meno omogenei, ordinati in modo da poter tenere sotto controllo l’intero andamento dell’azienda o dell’organizzazione, facilitarne il governo e la gestione e permetterne una programmazione che tenga conto dell’andamento reale fotografato dagli i., che molto spesso analizzano le situazioni in tempo reale. I sistemi di i. possono anche fornire un comodo approccio alla valutazione delle organizzazioni, alle quali viene attribuito un punteggio in una determinata scala, proprio in virtù dei valori che una serie di opportuni i. assumono in un determinato contesto.