ormone
Sostanza che, prodotta da una cellula endocrina, cioè a secrezione interna, viene liberata nel circolo sanguigno, provocando risposte funzionali in cellule localizzate a varia distanza dalla sua sede di produzione. Per l’espletamento dell’azione ormonale sono necessari, oltre alla sintesi e alla secrezione, il trasporto nel circolo sanguigno e la destinazione nei tessuti bersaglio dove sono presenti i recettori, strutture specializzate che riconoscono lo stimolo specifico e ne traducono il messaggio.
Classificazione
La comunicazione affidata agli o. avviene per la maggior parte attraverso il circolo ematico (azione endocrina), ma, in parte minore, anche mediante altre modalità. Alcuni o. agiscono infatti sulle cellule immediatamente circostanti la cellula che li produce (azione paracrina); in altre evenienze, invece, interagiscono con la stessa cellula secretrice (azione autocrina); altri o., infine, sono prodotti dai neuroni del sistema nervoso (azione neurocrina, che in realtà rappresenta una forma specializzata di azione paracrina).
Presentano grande importanza biologica le citochine, i fattori di crescita, le endorfine (oppioidi endogeni) e le endoteline, le cui modalità di produzione e azione sono, per molti aspetti, assimilabili a quelle ormonali; tali principi, in via diretta o indiretta, sono in grado di influenzare, generalmente in piccola misura, le secrezioni endocrine e gli effetti ormonali.
Sono stati identificati più di 50 o., le cui caratteristiche funzionali sono determinate dalla diversa struttura molecolare. In base a questa, essi sono suddivisi in quattro grandi categorie: proteine e peptidi; steroidi; derivati dagli amminoacidi; derivati dagli acidi grassi polinsaturi (fig. 1).
O. proteici e peptidici
Comprendono peptidi di piccole dimensioni, polipeptidi e glicoproteine di grandezza molecolare maggiore. Sono idrosolubili e pertanto circolano liberi nel plasma; di solito non penetrano all’interno delle cellule ed esplicano i loro effetti grazie al legame con i recettori localizzati in superficie sulla membrana cellulare. La sintesi degli o. peptidici avviene in modo identico a quella di tutte le altre molecole proteiche non ormonali. Gli o. proteici provengono invece da precursori più grandi e complessi, che subiscono processi proteolitici successivi fino al formarsi dell’o. finale; su tale base, essi possono essere suddivisi in vari gruppi: vi sono polipeptidi che già prima di essere trasformati in prodotto finale possono essere immessi in circolo sotto forma di pre-pro-ormoni e svolgere una qualche attività biologica, come è il caso dell’insulina, mentre per altri i complessi molecolari sono rappresentati da sequenze che non sono poi riscontrate nell’o. finale, oppure danno luogo a diversi prodotti biologicamente attivi. Un altro gruppo di o. proteici più complessi è caratterizzato dal fatto di essere sintetizzato in due pre-subunità che successivamente si uniscono: questo meccanismo di secrezione avviene, per es., per gli o. ipofisari TSH (thyroid stimulating hormone), FSH (follicle stimulating hormone), LH (luteinizing hormone) e per la gonadotropina corionica (HCG, human chorionic gonadotropin), che hanno un contenuto elevato di carboidrati, e pertanto appartengono alla classe delle glicoproteine.
Gli o. peptidici si accumulano all’interno della cellula nei granuli secretori con un processo sintetico continuo; sono liberati in seguito a stimoli specifici attraverso la cosiddetta esocitosi. Una volta secreti, gli o. proteici circolano in forma libera nel plasma, in quanto, a eccezione delle somatomedine, non contraggono legami con le proteine plasmatiche. Le loro concentrazioni nel plasma sono nell’ordine di 10-10 mol; la loro emivita plasmatica, e quindi la loro presenza in circolo, varia a seconda del tipo di o.: da 3 a 10 min (ADH, antidiuretic hormone; PTH, parathyroid hormone; TRH, thyrotropin-releasing hormone; GnRH, gonadotropin-releasing hormone), da 50 a 80 min (LH, TSH), fino a 4 ore (FSH e HCG). Gli o. glicoproteici sono metabolizzati a livello epatico, mentre quelli non glicoproteici sono metabolizzati e degradati prevalentemente a livello delle cellule bersaglio. Solo piccole quantità di o. peptidici sono escreti direttamente con le urine.
O. steroidei
Sono liposolubili, diffondono liberamente all’interno della cellula ed esercitano la loro azione dopo essersi legati a recettori localizzati nel nucleo. La loro struttura chimica, che è policiclica, deriva dal colesterolo. Sono suddivisi, in base alla sede di produzione, in steroidi gonadici e surrenalici; questa categoria include anche la vitamina D e i suoi analoghi. La steroidogenesi passa attraverso una serie di tappe enzimatiche, in massima parte catalizzate dagli enzimi citocromo P450 (cP450) localizzati all’interno delle cellule, e inizia dalla trasformazione del colesterolo in pregnenolone.
Questa tappa enzimatica è la più importante in quanto controlla la sintesi di tutti gli o. steroidei; anche in presenza di notevoli quantità di colesterolo, la possibilità di proseguimento della via biosintetica appare limitata, poiché dipende dall’attività degli enzimi cP450. Il pregnenolone formato fuoriesce dal mitocondrio e viene trasferito sul reticolo endoplasmatico, dove subisce le successive modificazioni enzimatiche da parte dei cP450. Il pregnenolone è quindi il precursore comune dei principali o. steroidei.
I glicocorticoidi sono sintetizzati nella zona fascicolata e, in minor misura, nella zona reticolare del surrene. L’o. più importante del gruppo è il cortisolo. I mineralcorticoidi sono sintetizzati nella zona glomerulare del surrene; l’aldosterone è l’o. fondamentale del gruppo. Gli androgeni sono sintetizzati dalle cellule di Leydig del testicolo, dalla zona reticolare del surrene e dalle cellule della teca del follicolo e dall’interstizio dell’ovaio. Gli estrogeni e il progesterone, i principali o. femminili, sono gli steroidi prodotti in maggiore quantità dall’ovaio e sono coinvolti nella regolazione del ciclo mestruale e nella gravidanza. La vitamina D e i suoi analoghi sono sintetizzati a partire dal colesterolo e gli enzimi biosintetici sono localizzati nella cute, nel rene e nel fegato.
Al contrario degli o. peptidici, la secrezione degli steroidi in circolo non procede attraverso un loro immagazzinamento all’interno delle cellule ma segue immediatamente la sintesi. Essi viaggiano nel plasma legati a proteine di trasporto specifiche, dotate di alta affinità, quali la globulina legante il cortisolo (CBG, cortisol binding globulin), le globuline leganti gli steroidi sessuali (SHBG, sex hormone binding globulin) e la proteina legante la vitamina D (DBP, vitamin D binding protein). La CBG è una glicoproteina in grado di legare con uguale affinità cortisolo e progesterone. Le SHBG sono globuline che legano con elevata affinità il testosterone, mentre l’estradiolo è legato in prevalenza all’albumina. Il 98% degli steroidi gonadici, il 95% del cortisolo e il 50% dell’aldosterone circolano legati alle rispettive proteine di trasporto. Poiché solo l’o. libero è in grado d’interagire con i recettori, e quindi di esprimere l’attività biologica, il legame plasmatico costituisce un’importante fase di riserva nel metabolismo di questi ormoni. Gli steroidi sintetici impiegati in terapia solitamente non contraggono legame con le proteine di trasporto e sono quindi in grado di esercitare effetti biologici immediati.
O. derivati da amminoacidi
Questo gruppo comprende gli o. tiroidei, le catecolammine e i derivati dal triptofano. Gli o. tiroidei prodotti dalle cellule follicolari della tiroide sono le iodotironine, derivate dall’unione di due nuclei di tirosina con lo iodio proveniente dall’alimentazione. Le catecolammine dotate di effetti ormonali sono l’adrenalina e la noradrenalina, sintetizzate, oltre che dai neuroni del sistema nervoso simpatico, anche a livello della midollare del surrene. Dal punto di vista chimico, sono derivati dell’amminoacido tirosina. Le catecolammine sono immagazzinate all’interno della cellula e secrete in risposta alla liberazione locale di acetilcolina. Hanno un’emivita brevissima (20 s) e vengono inattivate con due diversi meccanismi: la degradazione, che avviene nel fegato, e il recupero all’interno delle cellule da cui sono state secrete. I derivati dal triptofano sono la serotonina e la melatonina.
O. derivati da acidi grassi polinsaturi
Gli eicosanoidi sono molecole derivanti da un acido grasso polinsaturo a 20 atomi di carbonio, l’acido arachidonico. In base alla loro struttura chimica vengono distinti in tre gruppi: prostaglandine (fra le quali un posto a parte merita la prostaciclina), trombossani e leucotrieni. Queste sostanze hanno effetti biologici notevoli similormonali od ormonostimolanti molto diversificati e il più delle volte agiscono con azione eminentemente locale. Non sono immagazzinate all’interno delle cellule, ma immediatamente secrete secondo le necessità del momento; la loro produzione dipende dalla disponibilità di acido arachidonico. Hanno un’emivita di pochi secondi e sono degradate dagli enzimi tessutali.
Recettori ormonali
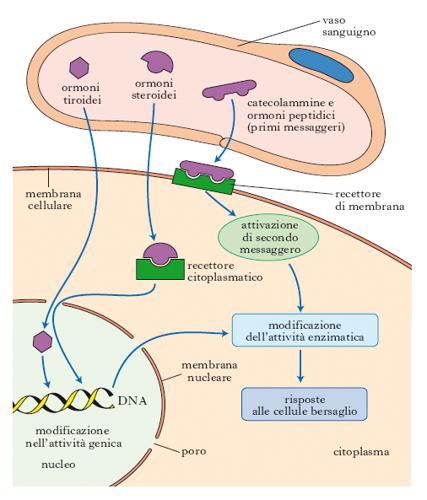
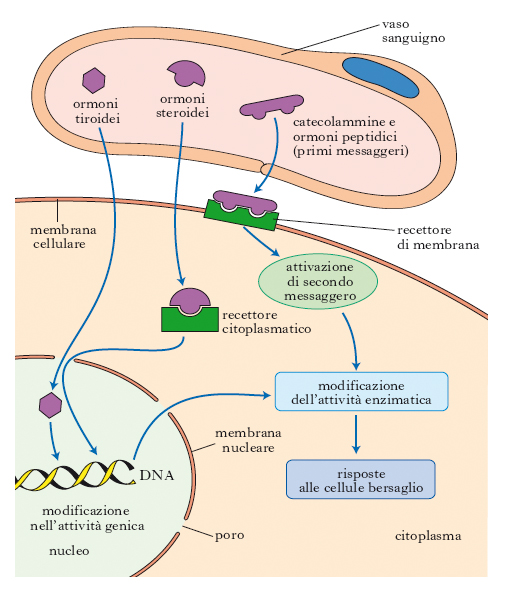
Nel corpo umano vi sono all’incirca 200 tipi di cellule di cui solo una minoranza produce o.; tuttavia, quasi tutte le cellule dell’organismo sono il bersaglio di uno o più ormoni. La caratteristica del sistema di comunicazione endocrino risiede nel fatto che gli o. circolano nel plasma a concentrazioni bassissime e, pertanto, le cellule bersaglio devono essere stimolate selettivamente. La capacità di riconoscimento selettivo è garantita dalla presenza nelle cellule bersaglio di strutture specializzate, cioè i recettori, i quali legano gli o. e ne mediano le azioni.
I recettori possono essere sulla membrana della cellula o all’interno di essa; l’o. che non può attraversare la membrana (per es. un peptide) si lega a recettori localizzati sulla membrana plasmatica, mentre quello che diffonde attraverso la membrana plasmatica all’interno della cellula (steroidi, iodotironine) si lega a recettori intracellulari (in genere situati nel nucleo). Indipendentemente dalla struttura e dal tipo di o., i recettori hanno caratteristiche comuni: tutti presentano una regione in grado di riconoscere e legare l’o. e un’altra deputata alla generazione di un segnale intracellulare che traduce il messaggio ormonale in risposte funzionali della cellula bersaglio; anche le proprietà che regolano il legame dell’o. (affinità, specificità, saturabilità, capacità di trasduzione, cioè di evocare effetti specifici) sono comuni per tutti i recettori. I rapporti fra o. e recettore sono in molti casi tali da consentire un aumento dei recettori (regolazione anterograda, o up-regulation) o una loro riduzione (regolazione retrograda, o down-regulation).
L’interazione o.-recettore è regolata da una complementarità stereochimica e da affinità di legame fra l’uno e l’altro. Questa affinità strutturale non riguarda necessariamente tutta la molecola del recettore e dell’o., ma può essere limitata solo a una porzione di uno o di entrambi. Pertanto, il legame di un o. al rispettivo recettore è garantito da specifici gruppi chimici dislocati in modo da poter interagire con definite regioni del recettore; di conseguenza, qualsiasi molecola, anche non ormonale, ma con le stesse caratteristiche strutturali, può, interagendo con il recettore, evocare una risposta ormonale.
In relazione alla capacità di evocare una risposta recettoriale, esistono nell’organismo principi biologici capaci di influenzare l’azione ormonale; questi principi si distinguono in agonisti, superagonisti e antagonisti. Gli agonisti sono molecole in grado di associarsi al recettore con la stessa affinità dell’o. naturale, provocando la medesima risposta cellulare. I superagonisti si comportano come gli agonisti, ma si legano ai recettori con migliore affinità rispetto all’o. naturale ed evocano un’azione maggiore e di più lunga durata. Gli antagonisti, invece, non evocano risposte biologiche in quanto, pur legandosi al recettore, non sono in grado di attivarne il meccanismo; la loro azione consiste perciò nel competere con l’o. naturale per il legame al recettore e, di conseguenza, se l’antagonista è presente insieme all’o. naturale, la risposta delle cellule bersaglio viene in qualche modo compromessa.
Azioni degli ormoni
Sviluppo e crescita. - L’influenza degli o. sullo sviluppo appare evidente fin dalla vita fetale, come dimostrato, per es., dalle alterazioni del sistema nervoso centrale dovute alla carenza di o. tiroidei o dalle anomalie della differenziazione sessuale legate alle alterazioni secretorie degli steroidi gonadici, con conseguente ermafroditismo o pseudoermafroditismo maschile o femminile. Nel periodo postnatale gli o. che risultano prevalentemente deputati al controllo della crescita sono il GH (growth hormone, od o. somatotropo) e le somatomedine; contribuiscono in maniera importante anche la vitamina D, necessaria per la maturazione scheletrica, gli steroidi sessuali, che inducono la saldatura delle epifisi, e gli o. tiroidei.
Produzione di energia e utilizzazione di substrati metabolici. - L’insulina, il glucagone, il GH, le catecolammine, gli o. tiroidei e i glicocorticoidi regolano il metabolismo dei carboidrati, come pure quello dei grassi, delle proteine e degli acidi nucleici, e sono responsabili della conversione dei composti che sono introdotti con la dieta in energia utilizzabile immediatamente (per es., produzione di calorie) oppure in processi sintetici (per es., impalcature dei tessuti, depositi ecc.).
Mantenimento dell’omeostasi. - Gli o. controllano il mantenimento e la regolazione delle condizioni ottimali di tutti gli organi e apparati anche in rapporto alle modificazioni ambientali. Tutti i maggiori sistemi omeostatici, cioè la pressione arteriosa, la frequenza cardiaca, il bilancio idroelettrolitico, l’equilibrio acido-base, la temperatura corporea, la composizione dei tessuti corporei (massa ossea, tessuto muscolare, tessuto adiposo), sono sotto il diretto controllo ormonale.
Riproduzione. -Gli o. svolgono un’azione di controllo relativa allo sviluppo e alla funzione delle gonadi; inoltre, contribuiscono in modo determinante alla differenziazione anatomica, funzionale e comportamentale dei due sessi. Gli estrogeni, il progesterone e gli androgeni, regolati dagli o. ipofisari, e in collaborazione con questi, consentono la maturazione sessuale, l’acquisizione e il mantenimento della capacità riproduttiva, nonché la gravidanza, l’espletamento del parto e la lattazione.
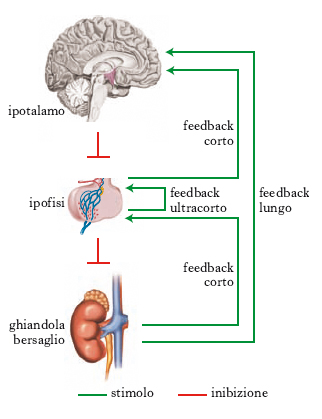
Sistema di feedback (o di regolazione retrograda). - Il feedback, o meccanismo di retroregolazione, è un sistema mediante il quale gli o. controllano gli effetti biologici che essi stessi determinano (fig. 2); tali effetti, a loro volta, regolano la secrezione dell’ormone. Il sistema consiste in un flusso bidirezionale continuo di informazioni tra la sede di produzione dell’o. e il tessuto bersaglio. Il feedback è definito positivo o negativo, a seconda che provochi una stimolazione oppure un’inibizione dell’azione ormonale, e lungo, corto o ultracorto, a seconda della distanza che intercorre tra l’o. e il tessuto bersaglio. II feedback pertanto risulta fondamentale per mantenere l’omeostasi. L’esistenza dei meccanismi di feedback riveste una grande importanza clinica e diagnostica; infatti, la maggior parte dei test dinamici si basa sulla valutazione dell’integrità di questi sistemi, che sono alterati in numerose malattie endocrine. Un feedback lungo è quello che si verifica tra l’ipotalamo, l’ipofisi e la ghiandola bersaglio e viceversa, con effetto sia stimolatorio sia inibitorio; un feedback corto si verifica tra gli o. ipofisari e i loro releasing hormones ipotalamici, con effetto sia stimolatorio sia inibitorio; infine, un feedback ultracorto è quello che si verifica con meccanismo paracrino e con effetto inibitorio sulle stesse cellule che producono l’o. o sulle cellule circostanti.
Bioritmi
Il sistema endocrino è regolato in modo dinamico con oscillazioni temporali variabili (da pochi minuti a un anno) delle secrezioni ormonali. Queste oscillazioni sono quantificate mediante alcuni parametri fondamentali. Il periodo di un ritmo è l’intervallo di tempo che intercorre tra due episodi identici; in sostanza rappresenta una misura della frequenza delle variazioni dei livelli ormonali. A seconda della loro ampiezza, i ritmi si dividono in infradiani, con durata inferiore alle 24 ore, circadiani, con durata compresa tra 20 e 28 ore, e ultradiani, con durata superiore alle 24 ore. L’ampiezza del ritmo viene definita come la differenza tra il valore massimo (acrofase) e quello minimo; il valore medio dei livelli ormonali durante il ritmo è denominato mesor. I ritmi biologici e quelli endocrini necessari a mantenere l’omeostasi rappresentano l’espressione delle capacità adattative dell’organismo alle variazioni ambientali (ciclo buio/luce) e alle esigenze fisiologiche (sonno/veglia, flussi mestruali, ovulazione); essi costituiscono una sorta di orologio interno che regola la sequenza temporale degli eventi fisiologici.
In condizioni patologiche, i ritmi endocrini essenziali per la normale funzione della maggior parte degli o. sono invece alterati. Il riconoscere queste alterazioni del ritmo è importante dal punto di vista clinico e diagnostico, perché permette una corretta interpretazione delle variazioni dei valori ormonali. La secrezione dell’o. della crescita (GH) è caratterizzata dalla presenza di livelli basali bassi e picchi improvvisi, specie nella prima fase del sonno; si riduce con l’età, in modo più marcato nella femmina. Nell’asse ipofisi-surrene la secrezione di ACTH (adrenocorticotropic hormone), o. stimolante il surrene, e di cortisolo risulta caratterizzata da un ritmo circadiano: è massima al mattino, si riduce gradualmente durante il resto del giorno per raggiungere livelli minimi nella notte. Non è influenzata significativamente dai ritmi sonno/veglia e non mostra differenze nei due sessi. La secrezione di prolattina (PRL) presenta un ritmo circadiano, contraddistinto da valori minimi intorno a mezzogiorno, un lieve incremento nel corso del pomeriggio e una fase di massima secrezione nelle prime ore del mattino. Oltre alle fluttuazioni circadiane, la PRL presenta brusche elevazioni dei livelli plasmatici in seguito allo stress, a stimolazione del capezzolo oppure ad attività fisica. Il ritmo di secrezione del TSH (o. tireotropo) presenta variazioni circadiane con picchi di secrezione notturna; tali picchi, nella donna, si verificano nelle prime ore del mattino, mentre nell’uomo si riscontrano in tarda serata.
Nell’asse ipotalamo-ipofisi-gonade il ritmo della secrezione di gonadotropine (FSH e LH) costituisce un esempio di ritmo ultradiano: nella fase prepuberale esso mostra, in entrambi i sessi, oscillazioni di bassa ampiezza durante l’arco delle 24 ore; la comparsa di picchi di secrezione notturna precede l’inizio della pubertà e diventa più evidente con il progredire dell’età, associandosi a un aumento dell’estradiolo nella femmina e del testosterone nel maschio. Uno spiccato aumento delle gonadotropine si può osservare nella donna a ogni ovulazione.
Ormonoterapia
La somministrazione, a scopo terapeutico, di o. naturali o sintetici (ormonoterapia) può essere attuata con scopi diversi: come terapia sostitutiva, quando la produzione di determinati o. è deficiente (somministrazione di insulina nel diabete pancreatico, di o. ipofisari in alcune forme di nanismo endocrino ecc.); come terapia stimolante (somministrazione di ACTH per migliorare la funzionalità dei surreni); come terapia sintomatica (iniezioni – nei casi più gravi intracardiache – di adrenalina, in alcune forme di collasso circolatorio); nel trattamento di alcuni tumori maligni (testosterone contro i carcinomi della mammella e le loro metastasi; estrogeni nel carcinoma della prostata ecc.).