biotecnologie
Tecnologie che controllano e modificano le attività biologiche degli esseri viventi per ottenere prodotti a livello industriale e scientifico.
Tecniche di controllo e modifica degli organismi viventi sono note sin dall’antichità, per es. la fermentazione; ma il grande impulso alle b. è avvenuto nel sec. 20°, soprattutto a partire dagli anni 1980, quando le acquisizioni scientifiche di discipline quali microbiologia, biochimica, biologia molecolare e ingegneria genetica sono state messe a frutto per elaborare metodiche sofisticate che consentono di ottenere industrialmente, da microrganismi o da parti di essi, prodotti utilizzabili nella diagnosi, prevenzione e terapia di numerose patologie, nel settore agroalimentare e zootecnico, nell’industria chimica e dell’ambiente.
Applicazioni in campo biomedico
Tecnologie del DNA ricombinante
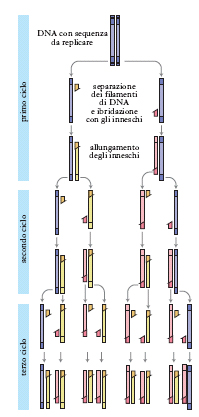
- Permettono di analizzare la struttura e la funzione dei geni, di manipolarli e di reintrodurli all’interno della cellula originaria o di una nuova cellula (fig. 1). Consistono nel clonare i geni, nell’amplificarli a piacimento, nel costruire geni sintetici, nell’inserire i geni in animali o piante superiori in modo che questi organismi acquisiscano nuove funzioni utili, nell’inserire geni nell’uomo per la cura di malattie ereditarie e di tumori. Mediante questi metodi è stato inoltre possibile usare frammenti di DNA come sonde per identificare la posizione di geni nel genoma, produrre nuove combinazioni di geni mediante la variazione delle sequenze nucleotidiche, causare specifiche mutazioni in specifici punti del gene, porre un gene sotto il controllo di differenti sistemi di regolazione. Le più importanti tecnologie genetiche sono la clonazione di geni, la produzione di oligonucleotidi sintetici, il metodo della reazione a catena della polimerasi (fig. 2).
Clonazione di geni Una delle applicazioni più notevoli dell’ingegneria genetica è la produzione di grandi quantità di proteine particolari che sarebbe altrimenti difficile ottenere. Il principio è relativamente semplice: il gene che codifica la proteina desiderata è accoppiato a un vettore che contiene un promotore batterico e sono effettuate analisi per accertare che il filamento codificante del gene sia orientato in maniera corretta rispetto all’orientamento del promotore. Il vettore nel quale il frammento di DNA da studiare viene inserito è un plasmide o un batteriofago che può normalmente replicarsi in un ospite batterico. L’inserimento del gene nel vettore avviene mediante il taglio del DNA del gene e del vettore con il medesimo enzima di restrizione e la successiva riunione dei due frammenti di DNA. Il gene legato al vettore viene inserito in un microrganismo di facile coltivazione, come un batterio, che acquisisce la capacità di esprimere una proteina che normalmente non produce. In tal modo, per es., il gene che codifica l'insulina o l’ormone della crescita nelle cellule di mammifero, inserito in un vettore opportunamente modificato (vettore di espressione), è in grado di codificare le stesse proteine in una cellula batterica. Altri vettori possono trasferire geni in cellule eucariotiche, quali il lievito, o in cellule vegetali. È possibile inoltre programmare opportune alterazioni del materiale genetico introducendo in esso mutazioni di specifiche coppie di basi.
Oligonucleotidi sintetici Le tecniche di preparazione di questi geni sintetici si basano sulla crescita della catena oligonucleotidica su una fase solida inerte. Alla fase solida viene inizialmente legato il primo residuo nucleotidico opportunamente protetto sui gruppi funzionali, che non devono essere coinvolti nella reazione. La polimerizzazione ha poi luogo attraverso la successione ripetuta di due passaggi: il primo consiste nella deprotezione del gruppo funzionale presente sull’ultimo residuo attaccato alla resina, che deve partecipare al legame fosfodiesterico; il secondo è l’aggancio del nucleotide successivo adeguatamente protetto per evitare reazioni collaterali. Mediante sintesi chimica si produce DNA a singolo filamento e la resa di ciascuna reazione permette la sintesi sia di brevi sequenze pure di 20 basi sia di sequenze più lunghe (200 basi). Questi oligonucleotidi sintetici, oltre ai tratti di DNA clonato delle genoteche, costituiscono sonde utili per molti processi biotecnologici, soprattutto per l’identificazione dei geni nel genoma e la diagnosi di malattie genetiche.
Reazione a catena della polimeras. Viene chiamato PCR (polymerase chain reaction) un metodo che utilizza le reazioni sequenziali della DNA-polimerasi per amplificare enormemente una singola copia di un gene o di un frammento di DNA. Questo metodo è risultato molto utile sia per avere grandi quantità di DNA sia per la diagnosi di alcune malattie virali, dove la quantità di DNA virale era tanto piccola da non poter essere identificata.
Tecnologie cellulari
- Consistono nella coltivazione massiva di cellule di mammifero e nella fusione di cellule diverse, per formare ibridi contenenti le informazioni genetiche di entrambi i ceppi originari. In particolare, la coltivazione di ibridomi ha reso possibile la fabbricazione in serie di anticorpi specifici per un determinato antigene, chiamati anticorpi monoclonali perché ottenuti attraverso la moltiplicazione di un’unica cellula (clone). Essi si ottengono fondendo cellule di mieloma di topo (cellule tumorali in grado di crescere in vitro ma incapaci di produrre anticorpi) con cellule normali ottenute dalla milza di un topo immunizzato contro uno specifico antigene, in grado quindi di produrre anticorpi contro di esso. Il prodotto della fusione, chiamato ibridoma, è in grado sia di crescere indefinitamente in vitro sia di produrre l’anticorpo specifico. Applicando questa tecnica si possono ottenere grandi quantità di anticorpi specifici per la sostanza che ha funzionato come antigene nel topo.
Diagnosi di malattie genetiche. - La tecnologia del DNA ricombinante e la PCR aprono consistenti prospettive per la diagnosi di malattie ereditarie. Il difetto biochimico di numerose malattie genetiche è sconosciuto, cioè è ignoto il difetto a carico della proteina o dell’enzima che è il risultato ultimo di un difetto a carico del DNA. Utilizzando le tecnologie genetiche sopra descritte è stato possibile identificare direttamente i difetti genetici (mutazioni) che sono la causa di malattie ereditarie, quali, per es., l’emofilia, le talassemie, l’anemia falciforme, la fibrosi cistica, o conoscere la base molecolare di malattie neurodegenerative, quali la corea di Huntington. Mediante la cosiddetta analisi diretta del DNA, una volta identificato il gene, o anche un frammento di DNA localizzato vicino al gene, è possibile identificare i portatori sani di malattie ereditarie (eterozigoti) o effettuare nel feto diagnosi di malattie genetiche. Tale analisi è applicabile sia in situazioni in cui sia noto il prodotto genico alterato di una determinata malattia, sia in situazioni in cui il prodotto genico sia sconosciuto. Per questa diagnosi si effettua una complessa analisi genetica familiare, basata sulla conoscenza della localizzazione cromosomica del gene mutato e di specifici marcatori a esso. Le associazioni tra gene mutato e marcatore permettono di ricostruire in una famiglia determinati schemi di eredità. In alcuni casi è inoltre possibile curare alterazioni geniche sostituendo il gene difettoso con procedimenti che nel loro complesso prendono il nome di terapia genica.
Industria farmaceutica
- I farmaci ottenibili per via biotecnologica sono antibiotici, vaccini, fattori di crescita, ormoni, farmaci antinfettivi e antitumorali, emoderivati, prodotti per la terapia enzimatica, anticorpi monoclonali con finalità terapeutiche e, infine, prodotti utili per la terapia genica. Molta attenzione viene posta anche alla possibilità di identificare, di isolare e di purificare le proteine prodotte da agenti patogeni. Si può in tal modo determinare la struttura tridimensionale delle proteine stesse mediante cristallografia a raggi X e progettare poi molecole che ne inibiscano la specifica funzione. La tecnologia del DNA ricombinante ha comportato vantaggi rispetto alle produzioni tradizionali e ha consentito di sviluppare vaccini di nuovo tipo con efficacia allargata al settore virale, come, per es., il vaccino contro l’epatite B. Per quello che riguarda le proteine del sangue è stato individuato e clonato il gene che codifica il fattore VIII, proteina responsabile della coagulazione del sangue e carente negli individui affetti da emofilia. Fra gli agenti capaci di combattere la formazione di coaguli ematici all’interno dell’organismo, che sono alla base di patologie quali l’infarto, l’embolia polmonare e la trombosi cerebrale, vengono prodotti, mediante tecnologie genetiche, l’urochinasi, la prourochinasi e il tPA (tissue plasminogen activator). Nel gruppo degli enzimi usati come farmaci sono da annoverare la superossidodismutasi, un enzima che contrasta la formazione dei radicali liberi, usato nell’artrite, nella colite e nell’infarto del miocardio; la lattasi, usata nei casi di intolleranza al lattosio; l’asparaginasi, l’arginasi e la ribonucleasi, usate nelle terapie antitumorali. Sostanze di particolare interesse prodotte mediante induzione di geni clonati in batteri sono le citochine, quali le interleuchine, l’interferone e il TNF (tumor necrosis factor). I cheratinociti in coltura massiva sono invece in grado di produrre fattori di crescita quali l’EGF (Epidermal Growth Factor), sperimentato nel trapianto di cornea e cristallino, nella cura di alcune forme di ulcera e negli innesti di porzioni di pelle nei grandi ustionati. Anche l’FGF (fibroblasts growth factor), che stimola la crescita dei capillari e viene impiegato per problemi muscolari e scheletrici, viene prodotto con sistemi biotecnologici.
Altri settori di applicazione
Agricoltura
- I principali campi di applicazione delle b. in agricoltura sono la difesa delle colture da stress biotici e abiotici, la nutrizione delle colture, la diversificazione dei prodotti e il miglioramento della loro qualità. Tra i processi e i prodotti in cui le b. offrono maggiore impiego vanno annoverate le piante geneticamente modificate (GM) o transgeniche, ottenute mediante tecniche d’ingegneria genetica. Tali tecniche consentono il trasferimento nel patrimonio genetico delle piante di informazioni che, una volta codificate, conferiscono loro caratteristiche nuove e vantaggiose rispetto a quelle originali. Le principali linee di sviluppo di piante GM sono finalizzate ad accrescere i rendimenti produttivi delle specie agrarie. Tale obiettivo può essere perseguito anche attraverso piante resistenti agli erbicidi, a patogeni e parassiti, a stress ambientali abiotici (aridità, salinità delle acque o del suolo, gelo) o con caratteristiche qualitative migliorate. Nel settore della difesa delle colture le b. hanno trovato campi di applicazione sia nella diagnostica sia nella profilassi. Per la prima si impiegano le sonde monoclonali per l’individuazione precoce e specifica di patologie altrimenti difficilmente individuabili. Per la profilassi sono stati sviluppati biopesticidi, ossia organismi (batteri, funghi, virus) capaci di parassitare le piante e di causare malattie nei parassiti. L’impiego delle b. è finalizzato, in questo caso, a trasferire nelle piante coltivate i geni dei biopesticidi, che codificano la struttura e la produzione delle proteine tossiche per gli insetti. Un altro settore di impiego dei microrganismi è quello della nutrizione delle colture, basato sui rapporti di simbiosi che si instaurano tra la pianta e alcuni microrganismi del terreno. Le principali forme simbiotiche riguardano i microrganismi azotofissatori del genere Rhizobium con le Leguminose, del genere Azospirillum con le Graminacee, dei cianobatteri con il riso. La tecnica consiste nella coltivazione di ceppi selezionati e nella inoculazione del terreno o delle sementi, in modo da esaltare le capacità di autofertilizzazione delle colture nei confronti dell’azoto e ridurre i costi e i rischi ambientali connessi all’impiego dei concimi. Le b. sono state impiegate anche per indurre miglioramenti della fase post-raccolta dei prodotti agricoli. È il caso, per es., dei pomodori GM, nei quali, al fine di allungare il tempo di maturazione e quindi di conservazione del prodotto, viene immesso un gene capace di bloccare la sintesi dell’etilene, ossia della sostanza responsabile del processo di maturazione.
Ambiente. - Le b. contribuiscono alla protezione dell’ambiente, intervenendo sia sui processi produttivi, sia sullo smaltimento finale degli scarichi, sia sul controllo e ripristino dei comparti ambientali inquinati. Per quanto riguarda il primo aspetto, le b. consentono di ottenere beni di largo consumo attraverso processi molto meno inquinanti dei corrispondenti processi chimici, in quanto non richiedono l’uso di sostanze potenzialmente pericolose per l’ambiente (solventi organici, catalizzatori a base di metalli pesanti ecc.) e sono capaci di introdurre selettivamente specifici gruppi funzionali nei composti chimici in condizioni blande di processo (temperatura bassa, pressione atmosferica, acqua come solvente, pH vicino alla neutralità ecc.). Inoltre, numerose produzioni biotecnologiche utilizzano materie prime di origine vegetale al posto del petrolio e del carbon fossile, la cui estrazione e movimentazione possono arrecare danni ambientali. Le b. forniscono anche vettori energetici (biocarburanti) a più basso impatto per l’ambiente rispetto ai carburanti in uso. Nell’ambito dei processi depurativi, il trattamento biologico delle acque di scarico consente non solo una rimozione delle sostanze organiche biodegradabili, ma anche l’abbattimento dell’azoto e del fosforo. Le b. intervengono nel trattamento delle emissioni gassose (con biofiltrazione) e nello smaltimento dei rifiuti solidi organici e dei fanghi di risulta degli impianti di depurazione delle acque (tramite digestione anaerobica con produzione di biogas o tramite compostaggio aerobico con produzione di ammendanti per uso agricolo, sostanze in grado di migliorare le proprietà e le caratteristiche di un terreno). Infine, le b. possono dare un contributo importante sia nel controllo degli ambienti naturali (tramite il monitoraggio continuo, anche in aree remote e di grande estensione, di contaminanti chimici presenti in concentrazioni anche molto basse) sia nel ripristino di condizioni di vivibilità ambientale di luoghi naturali contaminati (per es., suoli) attraverso processi di biorisanamento.
3 Industria agroalimentare
- Le b. avanzate migliorano i processi tradizionali di trasformazione e conservazione dei prodotti agricoli, come le fermentazioni, rendendoli sempre più selettivi e specifici o possono fornire nuovi metodi, come le trasformazioni biocatalizzate. Gli obiettivi sono la riduzione dei potenziali danni di tipo termico, meccanico e chimico durante le operazioni di trasformazione, la diversificazione e il controllo di qualità dei prodotti. Nel caso di processi tradizionali, la ricerca biotecnologica è orientata a selezionare le caratteristiche dei microrganismi che intervengono nelle biotrasformazioni (colture starters). L’impiego di starters riguarda l’industria lattiero-casearia, interessata a batteri lattici per controllare i processi di acidificazione e l’attività proteolitica; l’industria enologica, con l’impiego di lieviti selezionati in relazione alla capacità di fermentazione, alla produzione di alcol, alla capacità di flocculazione; la panificazione con l’uso di lieviti ingegnerizzati, per una lievitazione più rapida; la produzione di salumi e di birra. Tra gli enzimi, che possono essere ottenuti da estratti cellulari con processi di trasformazione o ancora trasferendo i geni che li codificano a microrganismi considerati più sicuri, i più usati sono la pectinasi per chiarificare i succhi di frutta, la lipasi e l’esterasi per ottenere formaggi con aromi differenziati, la β-galattosidasi per rendere il latte più digeribile, la lattoperossidasi e la rennina rispettivamente per una sorta di pastorizzazione a freddo e per la coagulazione del latte. Un altro settore di impiego delle b. è la produzione di additivi alimentari (dolcificanti, aromatizzanti, acidi organici, amminoacidi da usare come fortificanti nelle diete). B. sono utilizzate inoltre per il controllo di qualità, volto a individuare contaminanti di origine chimica o biologica. I metodi più diffusi sono i saggi immunoenzimatici o con sonde nucleotidiche e i biosensori.
4 Industria chimica
- Il settore in cui le b. forniscono i contributi più significativi è quello della chimica fine, dove il valore aggiunto dei prodotti è più elevato e maggiore è la necessità di prodotti mirati. Soprattutto di rilievo sono le applicazioni concernenti gli enzimi e i polimeri. Gli enzimi industriali (liberi o immobilizzati su adatti supporti o all’interno di cellule mantenute in stato stazionario) sono capaci di catalizzare, con elevata specificità e in condizioni molto blande di temperatura e pressione, quasi ogni tipo di reazioni organiche (ossidazioni, riduzioni, trasferimento intra- e intermolecolare di gruppi chimici, idrolisi, isomerizzazioni, addizione di molecole a doppi legami ecc.). Dal punto di vista applicativo gli enzimi più importanti sono le proteasi (largamente usate nel settore della detergenza), le amilasi (impiegate per l’ottenimento di derivati del mais) e le lipasi (utilizzate nei processi industriali di idrolisi di oli e grassi animali e vegetali. Molto spesso gli enzimi sono usati nella forma naturale; hanno trovato impiego anche forme modificate, ottenute per ingegneria genetica o per selezione di microrganismi termofili, che sono idonee a operare per lungo tempo in condizioni di processo avverse (elevata temperatura, condizioni estreme di pH o di salinità, presenza di solventi organici ecc.). L’interesse applicativo delle b. nel campo dei polimeri riguarda soprattutto i carboidrati di fonte microbica (cioè prodotti dalla fermentazione effettuata da microrganismi). Per es., lo xantano, prodotto da Xantomonas campestris, e lo scleroglucano, prodotto dai funghi del genere Sclerotium, trovano largo impiego come agenti ispessenti dell’acqua o di soluzioni acquose usate per veicolare farmaci o prodotti cosmetici, come ausiliari tessili, come fluidi per lo spostamento del grezzo nei giacimenti petroliferi in via di esaurimento. Il destrano, prodotto da Leuconostoc mesenteroides, è impiegato come costituente fondamentale del plasma sanguigno umano artificiale. Un altro biopolimero di natura polisaccaridica ottenuto ora in quantità industriali per via microbica (tramite fermentazione di batteri del genere Streptococcus) è l’acido ialuronico, che trova impiego in preparazioni cosmetiche e, soprattutto, farmaceutiche (in particolare, in chirurgia oftalmica e nella cura dell’artrite reumatoide). Infine, i biopolimeri (per es., poliidrossibutirrati) che si accumulano come materiali di riserva dentro le cellule di alcuni microrganismi hanno trovato, in ragione della loro biodegradabilità, applicazioni particolari in campo biomedico.
Risorse marine. - Le b. sono state utilizzate per ottenere materie prime, materiali e prodotti da organismi marini. Attraverso l’ingegneria genetica si può poi prospettare un miglioramento degli organismi viventi nell’habitat marino per una loro utilizzazione sempre più vasta. Le alghe, per es., rappresentano un materiale combustibile o possono divenire fonte di sostanze e principi attivi impiegati nelle industrie alimentare e cosmetica (acido alginico, alginati) e nell’industria farmaceutica (amminoacidi, pigmenti, enzimi, oli di fegato, chitina, chitosani).
2.6. Settore energetico. - Crescente è l’interesse per i biocarburanti in ragione del loro minore impatto ambientale e della rinnovabilità delle materie prime da cui sono prodotti. In prospettiva, anche i processi di biolisciviazione dei solfuri potrebbero consentire di disporre di combustibili fossili più ecocompatibili. Infine, in futuro potrebbe diventare di pratica attuazione il processo biotecnologico di produzione dell’idrogeno, che rappresenta un vettore energetico di grande interesse in quanto il suo prodotto di combustione è costituito da acqua e, di conseguenza, non ha effetti inquinanti.
7 Zootecnia
- L’applicazione delle b. in zootecnia risponde ai medesimi obiettivi di fondo esposti per l’agricoltura. In particolare, le b. possono rendere più efficienti la riproduzione, il controllo sanitario e l’alimentazione degli animali. Nel miglioramento genetico degli animali le b. possono essere impiegate per la valutazione genetica dei riproduttori, individuando caratteri che si ritiene utile trasmettere alla progenie, come, per es., la selezione del carattere che controlla la qualità del latte in relazione alla caseificazione. La selezione assume maggiore validità se associata alla fecondazione artificiale. La tecnica MOET (multiple ovulation embryo transfer) consente di aumentare l’intensità di selezione di individui di pregio nelle specie naturalmente monopare; essa consiste nell’indurre una poliovulazione in una femmina donatrice di alto valore genetico e nel fecondare gli ovuli con il liquido seminale di un maschio di provato valore genetico. Ulteriori potenzialità derivano dalla produzione di animali transgenici, nelle cui cellule germinali sono stati inseriti geni estranei provenienti da altri individui e che determinano caratteri trasmissibili alla progenie.